
- •Негосударственное образовательное учреждение
- •Общие методические указания
- •Правила оформления контрольной работы
- •Список литературы Основная
- •Дополнительная
- •Введение
- •Термодинамика и термохимия Основы термодинамики
- •Основные понятия и определения
- •Первый закон термодинамики
- •Основы термохимии
- •Второй закон термодинамики
- •Условия самопроизвольного протекания процессов
- •2. Процессы, протекающие при постоянном давлении и температуре.
- •Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Основные газовые законы Идеальный газ
- •Уравнение состояния идеального газа
- •Газовые смеси. Закон Дальтона
- •Вариант 1.
- •Двухкомпонентные системы Жидкие бинарные системы
- •Концентрации растворов
- •Осмотическое давление растворов
- •Давление пара разбавленных растворов. Закон Рауля
- •Температуры кипения и замерзания идеального бинарного раствора с нелетучим растворённым веществом. Эбуллиоскопия. Криоскопия.
- •Вариант 1.
- •Вариант 8.
- •Вариант 9.
- •Вариант 10.
- •Химическая кинетика Основные понятия
- •Зависимость скорости реакции от концентрации
- •Реакции нулевого порядка
- •Реакции первого порядка
- •Реакции второго порядка
- •Реакции третьего порядка
- •Зависимость скорости реакции от температуры
- •Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
- •Вариант 6.
- •Вариант 7.
- •Вариант 8.
- •Вариант 9.
- •Вариант 10.
- •Электрохимия Электрическая проводимость растворов электролитов
- •Вариант 1.
- •Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
- •Вариант 6.
- •Вариант 7.
- •Вариант 8.
- •Вариант 9.
- •Вариант 10.
- •Коллоидная химия Поверхностные явления
- •Классификация дисперсных систем по агрегатному состоянию
- •Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Коллоидное состояние вещества
- •Вариант 1
- •Вариант 1.
- •Вариант 1
- •Эбулиоскопические константы некоторых растворителей
- •Криоскопические константы некоторых растворителей
- •Константы диссоциации слабых кислот и оснований при 25ºС
- •Предельные подвижности ионов (См∙см∙моль-1) при 25ºС
- •Примерный перечень вопросов к зачету по дисциплине «Физическая и коллоидная химия»
Второй закон термодинамики
Второй закон термодинамики устанавливает критерии, позволяющие определить направление самопроизвольного протекания процессов.
Самопроизвольными называют процессы, которые протекают в системе без затраты энергии извне.
Процессы бывают обратимыми и необратимыми. Необратимые процессы идут самопроизвольно лишь в одном направлении. После протекания данных процессов, сопровождающихся изменениями в системе и окружающей среде, невозможно вернуть одновременно и систему и окружающую среду в исходное состояние.
Обратимымиявляются процессы, после которых систему и окружающую среду можно вернуть в исходное состояние.
Второй закон термодинамики имеет несколько формулировок, в варианте, предложенном Клаузиусом, он выглядит следующим образом: невозможен самопроизвольный переход теплоты от холодного тела к горячему.
Физический смысл второго закона термодинамики заключается в том, что любой самопроизвольный процесс протекает в направлении, при котором система из менее вероятного состояния переходит в более вероятное состояние. Другими словами, самопроизвольному протеканию процесса способствует увеличение неупорядоченности в системе.
Для характеристики меры неупорядоченности используется термодинамическая функция –энтропия S, которая связана стермодинамической вероятностьюсистемы формулой Больцмана:
S=k·lnW, (25)
где k– постоянная Больцмана.
Под термодинамической вероятностью Wпонимают число равновероятных микроскопических состояний, которыми может быть реализовано данное макроскопическое состояние системы. Для определения термодинамической вероятности системы необходимо найти число различных вариантов положений всех частиц системы в пространстве.
Энтропия является количественной мерой беспорядка в системе. Чем большеW, тем хаотичнее система, тем больше величина энтропии. Нагревание вещества приводит к увеличению энтропии, а охлаждение – к уменьшению. При приближении к абсолютному нулю (-273ºС) энтропия стремится к нулю, что позволяет определить абсолютные значения энтропии различных веществ, значения которых при стандартных условиях представлены в таблицах. Следует отметить, что в отличие от энтальпии образования, энтропия простого вещества, даже находящегося в кристаллическом состоянии, не равна нулю, т.к. при температуре, отличающейся от абсолютного нуля, макросостояние кристалла может быть реализовано не единственным макросостоянием, а большим числом равновероятных состояний.
Другая формулировка второго закона термодинамики выглядит так: полная энтропия всегда увеличивается в самопроизвольном процессе.
Увеличение энтропии ΔSпри протекании процесса должно превышать или быть равным отношению количества теплотыQ, переданного системе, к температуре Т, при которой теплота передаётся:
![]()
![]() .
(26)
.
(26)
Уравнение (26) является математической записью второго начала термодинамики. В данном уравнении знак неравенства относится к необратимым самопроизвольным процессам, а знак равенства – к обратимым процессам.
Согласно уравнению (26), изменение энтропии при обратимом переходе системы из состояния 1 в состояние 2 можно определить как:
ΔS=S2–S1=
![]() .
(27)
.
(27)
Фазовые переходы сопровождаются тепловым эффектом, называемымтеплотой фазового перехода ΔНф.п., и являются изотермическими процессами (Тф.п.=const). Для фазового перехода одного моля вещества изменение энтропии равно:
ΔSф.п.=![]() .
(28)
.
(28)
В процессах плавления, испарения жидкости или сублимации вещества энтропия увеличивается, так как разрушается упорядоченная кристаллическая решётка. Обратные процессы: кристаллизации, конденсации, десублимации сопровождаются уменьшением неупорядоченности в системе, и следовательно, уменьшением энтропии.
При изменении температуры вещества от Т1до Т2при постоянном давлении изменение энтропии определяется по формуле:
ΔS=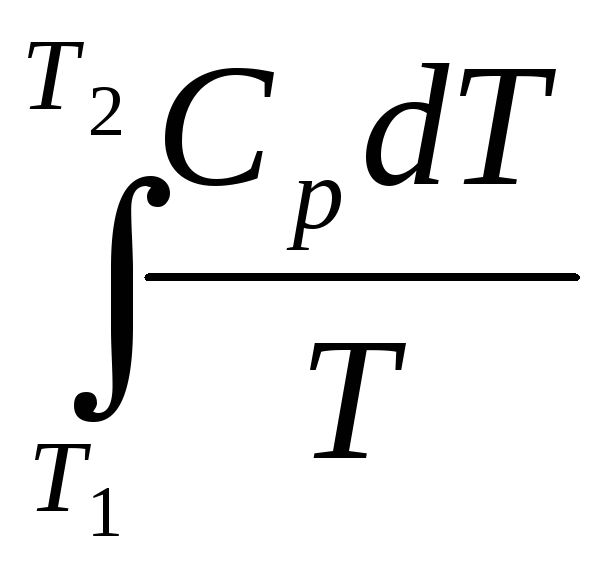 ,
(29)
,
(29)
поскольку Ср=const, то
ΔS= Ср·ln![]() .
(30)
.
(30)
Для изохорных процессов
ΔS=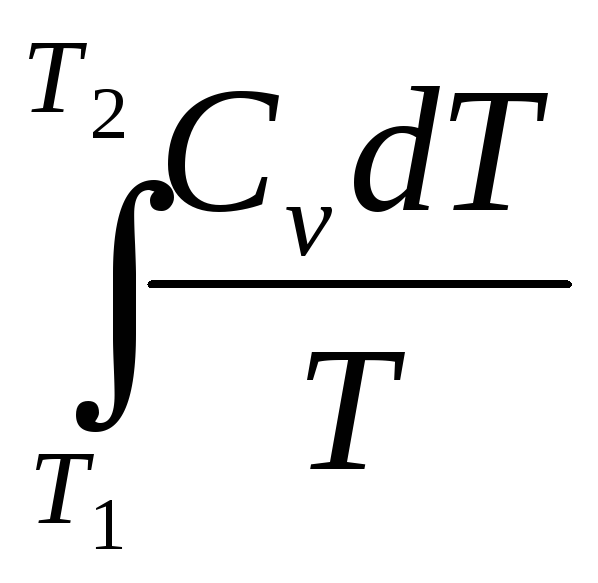 ,
(31)
,
(31)
при Сv=const
ΔS= Сv·ln![]() .
(32)
.
(32)
Стандартной
энтропией ΔS![]() называется энтропия 1 моля вещества в
стандартных условиях. Изменение
стандартной энтропии ΔS
называется энтропия 1 моля вещества в
стандартных условиях. Изменение
стандартной энтропии ΔS![]() при протекании химической реакции можно
рассчитать по уравнению, основываясь
на следствии из закона Гесса:
при протекании химической реакции можно
рассчитать по уравнению, основываясь
на следствии из закона Гесса:
ΔS![]() =
=![]() (33)
(33)
Наиболее хаотичной формой вещества является газообразное состояние, поэтому если в результате химической реакции число молей газа увеличивается, то хаотичность, а следовательно, и энтропия системы возрастает.
Обычно определяют не абсолютн6ое значение энтропии, а её изменение (S2–S1) в том или ином процессе. Для вычисления изменения энтропии при переходе одного моля идеального газа из одного состояния в другое используют формулы:
S2–S1 =R![]() (34)
(34)
S2–S1=R![]() (35),
(35),
где Сри Сv– постоянные величины. Изменение энтропии при нагревании единицы массы вещества, находящегося в твёрдом или жидком состоянии, рассчитывают по формуле:
S2–S1 =![]() ln
ln![]() (36),
(36),
где
![]() - удельная теплоёмкость вещества.
- удельная теплоёмкость вещества.
При переходе вещества из одного агрегатного состояния в другое изменение энтропии определяется по формуле:
S2–S1=![]() (37),
(37),
где L– скрытая теплота обратимого фазового перехода (испарения, плавления и др.); Т – температура фазового перехода.
