
- •Редактор Л.М. Тонкошкур
- •УДХТУ, 49005, Дніпропетровськ-5, просп. Гагаріна, 8.
- •Основні характеристики ковалентного зв’язку:
- •Таблиця 1.1
- •Характеристика ковалентних зв'язків
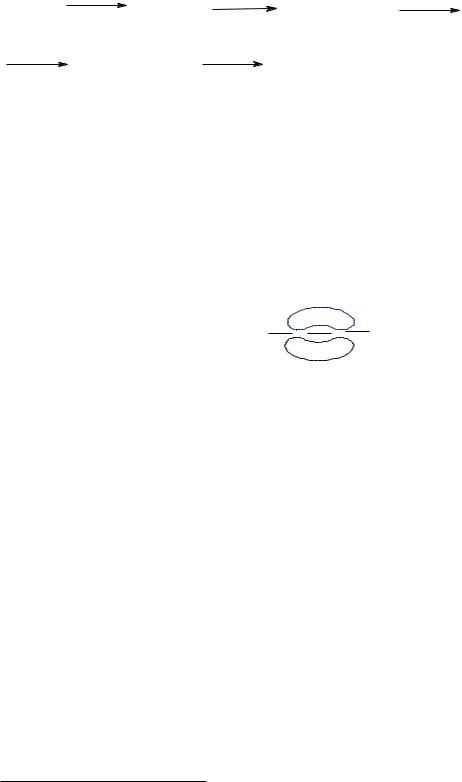
- •Нітроген, пірамідальна будова
- •Оксиген, кутова будова
- •Теорія хімічної будови органічних сполук О.М. Бутлерова
- •Класифікація в залежності від будови вуглецевого ланцюга
- •СПОСОБИ ОДЕРЖАННЯ АЛКАНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКАНІВ
- •СПОСОБИ ОДЕРЖАННЯ АЛКЕНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКЕНІВ
- •Швидкість приєднання галогеноводнів зменшується в ряду НI > НBr > НCl > НF відповідно із зменшенням міцності зв’язку Н-Hlg.
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКАДІЄНІВ
- •Природний каучук: цис-1,4-поліізопрен. Гутаперча: транс-1,4-поліізопрен
- •СПОСОБИ ОДЕРЖАННЯ АЛКІНІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ АЛКІНІВ
- •АЛІЦИКЛІЧНІ СПОЛУКИ
- •Циклоалкани. Класифікація, номенклатура та ізомерія
- •Сучасні уявлення про будову циклоалканів
- •СПОСОБИ ОДЕРЖАННЯ ЦИКЛОАЛКАНІВ
- •Спеціальні методи
- •ХІМІЧНІ ВЛАСТИВОСТІ ЦИКЛОАЛКАНІВ
- •АРОМАТИЧНІ ВУГЛЕВОДНІ
- •СПОСОБИ ОДЕРЖАННЯ БЕНЗОЛУ ТА ЙОГО ГОМОЛОГІВ
- •ХІМІЧНІ ВЛАСТИВОСТІ
- •ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
- •ПЯТИЧЛЕННІ ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
41
АЛКІНИ (АЦЕТИЛЕНОВІ ВУГЛЕВОДНІ)
Алкінами називають ненасичені вуглеводні, молекули яких містять між карбоновими атомами потрійний зв’язок C  C . Загальна формула CnH2n-2.
C . Загальна формула CnH2n-2.
СПОСОБИ ОДЕРЖАННЯ АЛКІНІВ
І.Промислові.
1.Окислювальний піроліз алканів:
6 CH4 + O2 1500 0C 2HC CH + 2 CO +10 H2
CH + 2 CO +10 H2
2. |
Піроліз алканів: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
2CH4 |
1500 0 |
C HC |
|
|
CH + |
3H2 |
|
||||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
t 0 |
|
CH2 + H2 |
|
|
t0 |
+ H2 |
|||||||||||||||
|
H3C |
|
CH3 |
|
H2C |
|
|
|
|
|
|
HC |
|
CH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
3. |
Карбідний метод: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
t 0 |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
CaCO3 |
|
|
|
|
CO2 + CaO |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
CaO + 3 C |
|
30000 |
C |
CaC2 + CO |
|
||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
CaC2 +2H2O |
|
|
|
|
|
|
HC |
|
CH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
- Ca(OH) |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
||
ІІ.Лабораторні:
1.Дегідрогалогенування віцинальних та гемінальних дигалогеналканів:
H2C |
|
|
|
CH2 + 2KOH спирт HC |
|
CH + 2 KCl + 2 H2O |
|||||||
|
|
|
|
||||||||||
|
|
|
|
||||||||||
|
|
|
|
||||||||||
Cl |
|
Cl |
|
|
|
|
|
|
|||||
|
|
|
H |
|
|
+ 2KOH |
спирт HC |
|
CH + 2 KCl + 2 H2O |
||||
H3C |
|
C |
|
Cl |
|
||||||||
|
|
|
|||||||||||
|
|
|
|
||||||||||
|
|
|
|
||||||||||
Cl
2. Алкілування ацетиленідів
|
|
|
NaNH2 |
|
|
|
|
|
CH3I |
|
|
|
|
42 |
|
|
|
|
CH3MgBr |
|||
HC |
|
CH |
|
HC |
|
CNa |
|
|
|
|
|
|
|
|
|
|
||||||
|
- NH3 |
|
|
- NaI |
|
H3C |
|
|
C |
|
|
CH |
- CH |
|||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
H C |
|
C |
|
CMgBr C2H5Br |
H |
C |
|
|
C |
|
|
C |
|
C H |
|||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
3 |
|
|
|
|
|
|
- MgBr2 |
3 |
|
|
|
|
|
|
|
|
2 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
БУДОВА АЛКІНІВ Потрійний зв’язок в ацетилені являє собою комбінацію σ- зв’язку, який
утворюється внаслідок перекривання двох sp-гібридних орбіталей атомів карбону та двох π- зв’язків, які утворюються внаслідок попарного перекривання чотирьох р- орбіталей.
+
H C C H
-
1.Довжина зв’язку C  C в ацетилені становить 0,121 нм, тобто коротша довжини подвійного зв’язку в етилені (0,134 нм); в етані (0,154 нм). Скорочення зв’язку
C в ацетилені становить 0,121 нм, тобто коротша довжини подвійного зв’язку в етилені (0,134 нм); в етані (0,154 нм). Скорочення зв’язку
обумовлено:
а) участю в утворенні σ- зв’язку двох sp-гібридних орбіталей з меншими власним радіусом; б) допоміжним скороченням зв’язку за рахунок утворення двох π- зв’язків.
2. Енергія зв’язку C  C в ацетилені набагато більша, ніж в етилені чи етані. Загальна
C в ацетилені набагато більша, ніж в етилені чи етані. Загальна
енергія зв’язку C  C 812 кДж/моль. Але якщо енергія зв’язку С-С в етані становить 344 кДж/моль то в середньому енергія π- зв’язку становить лише 234 кДж/моль, тобто на 110 кДж/моль менша енергії σ- зв’язку. Відповідно, для
C 812 кДж/моль. Але якщо енергія зв’язку С-С в етані становить 344 кДж/моль то в середньому енергія π- зв’язку становить лише 234 кДж/моль, тобто на 110 кДж/моль менша енергії σ- зв’язку. Відповідно, для
ацетилену будуть характерні реакції з розривом зв’язку C  C .
C .
3. Енергія іонізації зв’язку C  C (енергія, необхідна для вибивання електрону з π- зв’язку ) дорівнює 11,4 еВ, що значно більше ЕІ СН2=СН2 – 10,5 еВ та практично дорівнює ЕІ СН3–СН3 – 11,6 еВ. Отже, електрони π- зв’язків в ацетилені міцно утримуються атомами карбону і вони значно менш придатні для атаки електрофілом, ніж π-електрони алкенів. Це відповідає sp-гібридизації атому карбону. При цьому енергія іонізації ацетиленових вуглеводнів різко зменшується
C (енергія, необхідна для вибивання електрону з π- зв’язку ) дорівнює 11,4 еВ, що значно більше ЕІ СН2=СН2 – 10,5 еВ та практично дорівнює ЕІ СН3–СН3 – 11,6 еВ. Отже, електрони π- зв’язків в ацетилені міцно утримуються атомами карбону і вони значно менш придатні для атаки електрофілом, ніж π-електрони алкенів. Це відповідає sp-гібридизації атому карбону. При цьому енергія іонізації ацетиленових вуглеводнів різко зменшується

43
при введенні алкільних груп. Так для пропілену ЕІ становить лише 10,4 еВ. Отже, пропілен в реакціях електрофільного приєднання буде реагувати значно легше, ніж ацетилен. Тому, що потрійний зв’язок легко поляризується і заміщені ацетилени більш поляризовані, ніж алкени. Наприклад, дипольний момент пропілену становить 0,35D, тоді як пропіну – 0,75D.
4.Довжина зв’язку С-Н в ацетилені також менша, ніж в алкенах і алканах і відповідно становить 0,106, 0,108, 0,109 нм. Відповідно, енергія зв’язку С-Н в ацетилені більша. Тобто, sp-гібридизація атому карбону в ацетилені зашкоджує гомолітичному розриву зв’язку С-Н з утворенням вільних радикалів. Але внаслідок більшої поляризації зв’язку С-Н в ацетилені із-за більшої електронегативності spгібридизованого атому карбону (2,75, 2,62 та 2,50 для sp, sp2, sp3 - гібридизованих атомів карбону) полегшується гетеролітичний розрив зв’язку С-Н з утворенням йонів. КдисС2Н2 = 10-22, тоді як КдисС2Н6 = 10-40.
ХІМІЧНІ ВЛАСТИВОСТІ АЛКІНІВ
Алкіни вступають в реакції приєднання, які можуть відбуватися за радикальним, електрофільним та нуклеофільним механізмами, а також в реакції заміщення атомів водню, розміщених біля атому карбону з потрійним зв’язком.
І. Приєднання радикальних реагентів. Гідрування. Потрійний зв’язок гідрується легше, ніж подвійний зв’язок в алкенах.
а) Водень в момент народження:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Na + NH3 H3C |
|
|
|
|
|
H |
|
|
H C |
|
|
|
|
|
CH |
|||||||
H3C |
|
|
|
|
C |
|
|
|
C |
|
|
|
CH3 |
|
|
H |
C |
|
|
C (90%) |
+ |
|
3 |
|
|
C |
|
C |
3 (10%) |
|||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
H |
||||||
|
|
|
|
|
|
б) Каталітичне гідрування: |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
H3C |
|
|
|
C |
|
|
|
C |
|
|
|
CH3 |
|
H2 |
H3C |
|
|
|
|
H |
|
|
H C |
|
|
|
|
CH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ni |
C |
|
|
|
|
C |
(50%) |
+ |
|
3 |
|
|
|
|
|
|
|
|
3 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
(50%) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
CH3 |
|
|
|
H |
|
|
|
|
H |
|
|||||
H3C |
|
|
|
|
|
|
|
|
C |
|
|
|
CH3 |
|
H2 |
H3C |
|
|
|
|
H |
|
H3C |
|
|
|
|
CH3 |
||||||||||||
|
|
|
C |
|
|
|
|
|
|
C |
|
|
|
C |
(10%) |
+ |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
Pd/Pb |
|
|
|
|
|
C |
|
|
|
C |
|
(90%) |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
CH3 |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
44
Реакції, які переважно приводять до одного з кількох можливих стереоізомерів називають стереоселективними; реакції, які приводять до одного з кількох можливих – стереоспецифічними.
ІІ.Приєднання електрофільних реагентів.
1.Галогенування – може відбуватися, як за радикальним, так і електрофільним механізмом. Електрофільне галогенування відбувається транс-стереоселективно:
HC |
|
CH + Cl2 |
SbCl3 |
H |
Cl |
H |
|
|
|
H Cl2 |
|
|
|
||
|
C |
|
C |
|
|
|
|
Cl2HC |
|
CHCl2 |
|||||
|
|
|
|
+ |
C |
|
C |
|
|
||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
Cl |
H |
Cl |
|
|
|
Cl |
|
|
|
||
|
|
|
|
(90%) |
|
(10%) |
|
|
|
||||||
2.Гідргалогенування – відбувається також транс-стереоселективно, за правилом Марковнікова.
H3C |
|
|
|
|
C |
|
|
C |
|
CH3 + HCl |
|
|
H3C |
|
|
Cl |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
C |
(90%) |
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH + HCl |
H3C |
|
|
H |
H |
CH3 |
|
|
Cl |
||||||||||
H3C |
|
|
|
|
C |
|
|
|
|
|
|
HCl |
H3C |
|
|
|
|
|
||||||||||
|
|
|
|
|
Cl |
|
C |
|
C |
H |
|
C |
|
CH3 |
||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
CH + HCl |
HgCl2 |
|
|
|
|
|
|
|
|
Cl |
||||||||||||
HC |
|
|
|
H2C |
|
|
CHCl |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
ІІІ.Приєднання нуклеофільних реагентів.
1.В присутності каталізаторів, які збільшують електрофільність потрійного
зв’язку. Приєднання Н2О.
Реакція Кучерова
HC |
|
|
|
|
CH + H2O |
|
|
HgSO4, H2SO4 |
H3C |
|
|
C |
|
|
|
|
O + Hg 2+ |
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH + Hg |
2+ |
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
+ |
H2O |
|
+ |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
HC |
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
Hg + HC |
|
CHOH2 |
- H O+ |
Hg |
|
HC |
|
CH(OH) |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Hg 2+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
Hg + HC |
|
C |
|
O |
H3O+ |
H C |
|
C |
|
O |
+ |
Hg 2+ |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
3 |
|
|
H |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
H3C |
|
|
|
|
C |
|
CH + H2O |
|
HgSO4, H2SO4 |
H3C |
|
|
C |
|
CH3+ Hg 2+ |
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||
Правило Ельтекова: ненасичені спирти з групою ОН біля атому карбону з подвійним зв’язком нестійкі і самовільно ізомеризуються в стійкі карбонільні сполуки. Між енольною та карбонільною сполуками існує рівновага:

|
|
|
|
|
|
45 |
|
|
|
|
C |
C |
C |
C O |
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
C |
C |
C |
C |
H |
|
- |
O |
+ |
C C |
O |
O |
- |
C C |
H |
|
||||||
|
OH |
|
|
|
|
|
H |
|
||
Причина ізомеризації – висока полярність зв’язку ОН. При приєднанні протону знову до атому оксигену, він може знову відщеплюватися, при приєднанні до атому карбону
– значно гірше, тобто поляризація зв’язку С-Н значно менша. В результаті відбувається перегрупування, при якому сильніша кислота перетворюється на слабшу. Структурні ізомери, між якими в нормальному стані існує рівновага називаються таутомерами.
2.В присутності каталізаторів, які збільшують нуклеофільність реагентів. a. Приєднання спиртів з утворенням вінілових ефірів:
H3C C CH + CH3OH CH3ONa H3C C CH2 OCH3
CH + CH3OH CH3ONa H3C C CH2 OCH3
b. Приєднання синільної кислоти з утворенням нітрилів:
HC CH + HCN Cu2(CN)2, KCN H2C CH CN
CH + HCN Cu2(CN)2, KCN H2C CH CN
c. Приєднання оцтової кислоти:
AcONa
HC CH + CH3COOH
CH + CH3COOH  H2C
H2C CH OAc
CH OAc
ІV. Карбонолування алкінів
HC |
|
|
CH + CO + HX |
Ni(CO)4 |
H2C |
|
|
|
CH |
|
|
C |
|
|
|
X |
, X = OH, OCH3, NH2 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
HC |
|
|
CH + (CO)4Ni |
HC |
|
CH |
C |
|
O |
|
HC |
|
|
|
|
CH |
+ Ni(CO)3 |
HX |
H2C |
|
CH |
|
|
C |
|
X |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
Ni(CO)3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
V. |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Реакції заміщення:

46
HF > H2O > H3N > H4C
KF KOH KNH2 KCH3
1. |
H3C |
|
C |
|
CH + CH3MgBr |
|
H3C |
|
C |
|
CMgBr |
||||
|
|
|
|||||||||||||
|
|
|
|
||||||||||||
|
|
|
|||||||||||||
2. |
H3C |
|
|
C |
|
|
CH + NaNH2 |
|
H3C |
|
|
C |
|
|
CNa |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|||||||||
3. H3C |
|
|
C |
|
|
CH + KOH |
|
H3C |
|
|
C |
|
|
CK |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||
+
+
+
CH4
NH3 H2O
|
HF > H2O > HC |
|
CH > H3N > H4C |
|
|
|
|
|
CAg + 2NH3 |
|||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
||||||||||
4. |
H3C |
|
|
C |
|
|
CH + Ag(NH3)2OH |
H3C |
|
|
C |
|
|
|||
|
|
|
||||||||||||||
|
|
|
|
|||||||||||||
|
|
|
||||||||||||||
5. |
H3C |
|
|
C |
|
|
CH + Cu(NH3)2OH |
H3C |
|
|
C |
|
|
CCu + 2NH3 |
||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||||
+
+
H2O
H2O
VІ. Реакції приєднання до альдегідів та кетонів:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH + CH3COCH3 |
|
|
KOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
1. Фаворський: |
|
|
HC |
|
|
|
|
|
HC |
|
|
|
C |
|
|
|
|
C |
|
|
|
OH |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH + CH2O Cu( C |
|
|
|
CH)3 HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
2. Реппе: HC |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
C |
|
|
C |
|
|
CH2 |
OH |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
HOCH2CH2CH2CH2OH |
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
|
|
|
CH |
|
|
|
|
CH |
|
|
|
CH2 + 2 H2 |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
3. Добування карбонових кислот: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
HC |
|
CMgBr + CO2 |
|
|
|
|
|
|
|
|
HC |
|
|
C |
|
|
C |
|
|
|
O |
|
MgBr |
|
HBr |
|
|
|
HC |
|
|
C |
|
|
O |
+ MgBr2 |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
OH |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
VІІ. Реакції заміщення атому гідрогену біля потрійного зв’язку на галоген: |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
C |
|
|
|
|
CH + NaOCl |
|
|
|
|
|
|
|
|
H C |
|
|
C |
|
|
|
|
|
CCl |
|
+ NaOH |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
VІІІ. Реакції полімеризації: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
1. |
HC |
|
|
CH + HC |
|
CH |
Cu2Cl2 |
H C |
|
|
|
CH |
|
|
|
|
|
|
|
|
CH |
|
|
|
HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
CH |
|
CCl |
CH2 |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HgCl2 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Ni(CO) .Pr P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хлоропрен |
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
2. |
3 HC |
|
|
CH |
|
|
|
|
|
3 |
3 |
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3
3 HC CH H2SO4 !
CH H2SO4 !
H3C 
 CH3
CH3
3. 4 HC CH Ni(CN)2
CH Ni(CN)2
4. |
n HC |
|
CH |
R |
|
[ |
CH |
|
CH |
]n |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
ROMe |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
5. |
n HC |
|
|
CH |
|
O2 |
HC |
|
|
C |
|
|
|
C |
|
CH |
|
|
[ |
C |
|
C |
|
C |
|
C |
]n |
карбін |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
ІХ. Реакції окиснення:
