
- •Ресурсосберегающие технологии в нефтегазохимическом комплексе
- •Санкт-Петербург
- •Содержание
- •I. Общие положения
- •II. Методические указания к практическим занятиям
- •1.1. Элементы расчетов химико-технологических процессов (хтп)
- •1.1.1. Рекомендуемые обозначения и единицы измерения
- •1.1.2. Массовый, объемный и мольный состав
- •1.1.3. Характеристики газовых смесей
- •1.1.4. Термодинамические расчеты в энергосбережении
- •1.1.5. Энерготехнологические установки (на примере синтеза аммиака)
- •1.1.6. Элементы расчета химических реакторов в нефтепереработке
- •1.1.7. Элементы расчетов процессов переработки нефти
- •II. Определение основных технико-экономических показателей (тэп) процессов нефтегазопереработки
- •Расходный коэффициент и степень превращения сырья
- •Выход продукта и селективность
- •Производительность, мощность и интенсивность аппарата
- •III. Расчет материальных балансов процессов и аппаратов
- •IV. Расчет энергетического (теплового) баланса процессов и аппаратов
- •V. Примеры расчетов
- •5.1.Определение основных тэп
- •5.2. Расчёт материальных балансов
- •5.3.Расчёт тепловых балансов
- •5.4. Энерго- и ресурсосбережение в переработке топлив
- •5.5. Элементы расчетов реакторов
- •5.6. Переработка нефти
- •III. Примерные задачи для самостоятельной работы
- •IV. Требования к оформлению домашних работ
- •V. Список литературы Основная литература
- •Дополнительная литература
- •Лист регистрации изменений
IV. Расчет энергетического (теплового) баланса процессов и аппаратов
В основу энергетического баланса положен закон сохранения энергии, согласно которому в замкнутой системе сумма энергий всех видов постоянна. Частным и наиболее распространенным в химическом производстве видом энергетического баланса является тепловой баланс: приход тепла в данной технологической операции равен расходу тепла в ней, что записывается в форме уравнения теплового баланса.
∑Qприход=∑Qрасход
Статьями прихода и расхода в тепловом балансе являются тепловые эффекты реакций ΔН, теплоты фазовых переходов (Q1), теплосодержание веществ, участвующих в процессе (Q2), теплота, подводимая в аппарат извне и выводимая из аппарата (Q3), тепловые потери (Q4) в данной технологической операции:
ΔН+ Q1+ Q2+ Q3+ Q4= ΔН1+ Q11+ Q21+ Q31+ Q41,
где индекс (1) относится к статьям расхода.
Тепловые вклады в баланс рассчитывают по известным формулам. Тепловой эффект химической реакции по формуле:
ΔН= ∑ΔНпродукты реакции - ∑ΔНисходные вещества,
в которой значения энтальпии продуктов реакции и исходных веществ берутся из таблиц.
Теплосодержание веществ рассчитывают по формуле:
Q2=m*c*t,
где m – масса вещества,
c – его теплоемкость,
t – температура.
Теплоту фазовых переходов рассчитывают по формуле:
Q1=m*q,
где q – удельная теплота соответствующего фазового перехода (испарения, конденсации, растворения, кристаллизации),
m – масса вещества.
Подвод и отвод теплоты в систему рассчитывают по потере тепла теплоносителем по формуле:
Q3=m*С(tн-tк),
где m – масса вещества,
С –теплоемкость теплоносителя,
tн,tк – начальная и конечная температура теплоносителя,
и по формуле теплопередачи через стенку:
Q3=Кт*F(tт-tпр)*τ,
где Кт – коэффициент теплопередачи,
F –поверхность теплообмена,
tт –температура теплоносителя, обогревающего аппарат
tпр – температура подогреваемого продукта
τ – время.
Тепловой баланс составляется по результатам материального баланса на единицу производимого продукта или на цикл работы аппарата. Данные теплового баланса используются для определения расхода теплоносителя и хладагента, расчета поверхности греющих и охлаждающих элементов и подбора оптимального теплового режима процесса.
V. Примеры расчетов
5.1.Определение основных тэп
Пример 1. Определите расходные коэффициенты в производстве карбида кальция, содержащего 90% СаС2 если сырье — антрацит марки АК с содержанием углерода 96%, известь (негашеная) с содержанием СaО 85%.
Решение. Карбид кальция получают по реакции выражаемой уравнением:
СаО + ЗС = СаС2 + СО,
Мг (СаС2)=64; Мг (СаО)= 56в; Аг(С)=12.
По условию в 1 т продукта содержится 900 кг СаС2.
Определим сколько оксида кальция требуется на образование 900 кг СаС2:
-
Ат =
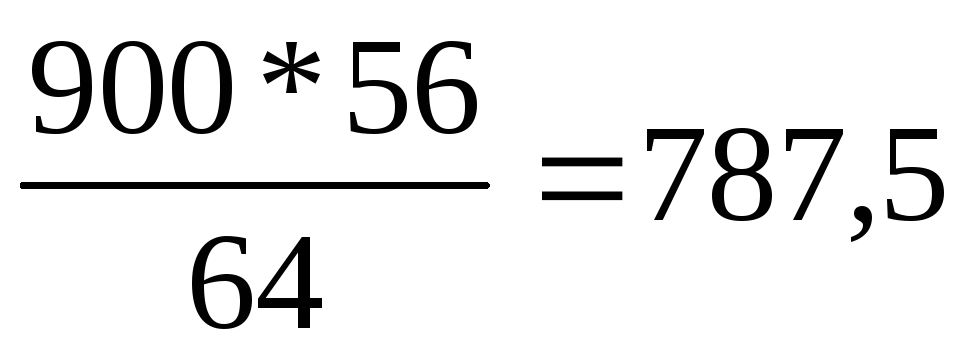
кг
С учетом чистоты СаО рассчитаем практический расходный коэффициент по извести:
-
Апр =
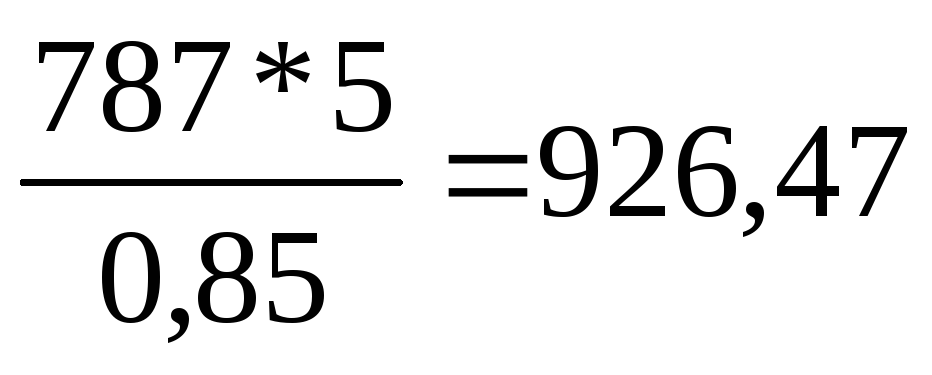
кг
Находим, сколько углерода требуется на образование СаС2:
-
Ат2 =

кг
Определяем расходный коэффициент по антрациту:
-
Апр2 =
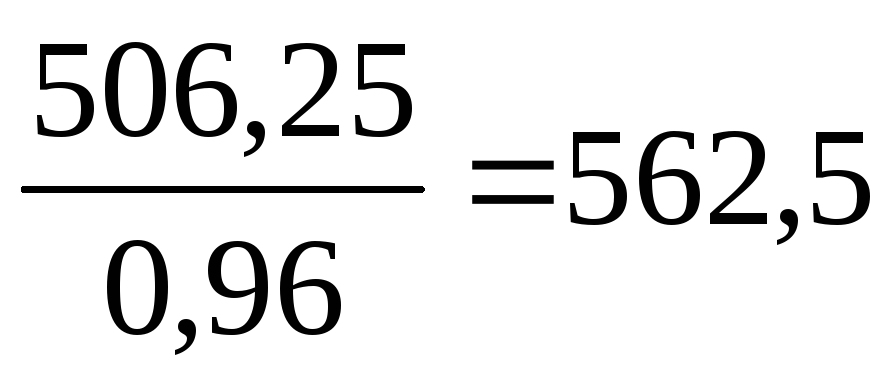
кг
Пример 2. Рассчитайте теоретический расходный коэффициент 18%-ного раствора едкого натра для мерсеризации 1 т целлюлозы, содержащей 5% влаги и 4% примесей.
Решение. Процесс мерсеризации целлюлозы можно выразить уравнением реакции:
[C6H7О2(OH)3]n + nNaOH→[C6H7O2(OH)2OH∙NaOH]n
Мг целлюлозы = n∙162; Мг едкого натра = 40, Найдем, сколько чистого гидроксида натрия потребуется на мерсеризацию 0,91 т целлюлозы:
-
Ат =
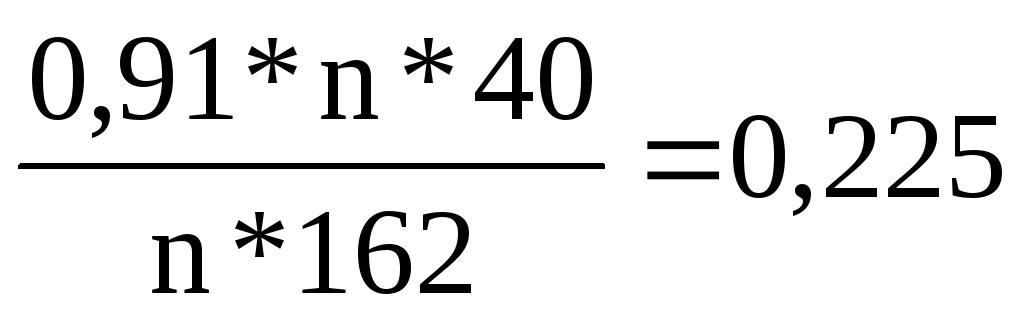
т
18%-ного раствора требуется:
0,225/0,18 = 1,248 т.
Пример 3. Рассчитайте выход этилового спирта на пропущенный этилен при условии многократной циркуляции этилена, если практический расходный, коэффициент этилена 0,69 т на 1 т этилового спирта.
Решение. Этиловый спирт получается при взаимодействии этилена с водой:
С2Н4+Н2О↔С2Н5ОН
Молекулярные массы:
Мг (С2Н4)= 28; Мг (С2Н5ОН)=46.
Теоретический выход этилового спирта из 690 кг этилена:
mT=![]()
Практическая масса этанола mпракт=1000кг. Находим практический выход этилового спирта:
ή![]()
