
- •Періодичні культури
- •Спиртове бродіння
- •Молочнокисле бродіння
- •Види молочнокислих бактерій, які мають важливе значення для промисловості
- •Мікрофлора і процеси, які використовують для виробництва кисломолочних продуктів
- •Пропіоновокисле бродіння
- •Маслянокисле бродіння
- •Мурашинокисле бродіння
- •Алостеричне регулювання
- •Ковалентна модифікація ферментів
- •Інгібування кінцевим продуктом
- •Індукція і репресія
- •Механізм індукції та репресії
- •Будова лактозного оперону
- •Будова триптофанового оперону
- •Позитивний контроль оперону і катаболітна репресія
- •Тема: генетика мікроорганізмів
- •Фотореактивація (світлова репарація)
- •Темнова реактивація (репарація)
- •Види генетичних рекомбінацій
- •Мікрофлора шкіри
- •Мікрофлора діхальних шляхів
- •Мікрофлора порожнини рота
- •Мікрофлора шлунково-кишкового тракту
- •Кількісний вміст мікроорганізмів у різних відділах шлунково-кишкового тракту
- •Мікрофлора сечостатевих органів
- •Мікрофлора очей і вух
- •Роль аутофлори в життєдіяльності організму людини
- •Мікрофлора ґрунту
- •Мікрофлора води
- •Мікрофлора повітря
- •Кругообіг елементів у природі
Алостеричне регулювання
Як правило, регуляторні ферменти є алостеричними. Такі ферменти місять активний (каталітичний) і алестеричний (регуляторний) центри. Вони відрізняються місцем розміщення і конфігурацією.
Речовини, які впливають на активність алостеричних ферментів, називаються ефекторами або модуляторами. Якщо вони підвищують активність ферменту, їх відносять до активаторів, якщо знижують – до негативних ефекторів. В якості ефекторів можуть виступати субстрати, проміжні та кінцеві продукти, АТФ, АДФ, ацетилкофермент-А, НАДН2 тощо.
Регуляторний вплив ефектора на алостеричний фермент відбувається на рівні утворення фермент-субстатного комплексу. Приєднання ефектору до алостеричного центру змінює конформацію каталітичного центру і, відповідно, спорідненість ферменту до субстрату. Вплив негативного ефектора зображений на рис. 1.
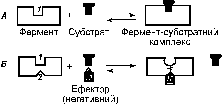
Рис. 1. Схема взаємодії простого (А) і алостеричного (Б) ферментів зі субстратом і ефктором: 1 – активний центр; 2 – алостеричний центр
BOX
|
Кінетичні характеристики нерегуляторних ферментів показують, що константа Міхаеліса (Кm) – це концентрація субстрату, необхідна для того, щоб фермент працював вполовину своєї максимальної швидкості. Вона дійсна тільки для процесів, які описуються гіперболою. Залежність швидкості протікання реакцій від субстрату у алостеричних ферментів описується сигмоїдальною кривою. Концентрація субстрату для половини від максимальної швидкості в даному випадку називається К0,5. Один з найбільш вивчених алостеричних регуляторних ферментів у E.coli – аспартаткарбомоїлтрансфераза (АКТаза). Він каталізує конденсацію карбамоїлфосфату і аспартату з утворенням карбамоїласпартату, який далі іде на біосинтез піримідинів. Фермант має більше, ніж один активний центр. Приєднання молекули субстрату до одного активного центру збільшує спорідненість субстрату до іншого. Цитідин трифосфат (ЦТФ) – кінцевий продукт піримідинового біосинтезу - інгібує фермент, а АТФ – активує його. Обидва ефектори змінюють значення К0,5, але не змінюють максимальної швидкості роботи ферменту. Коли присутній ЦТФ – фермент гальмується. В присутності активатору АТФ фермент максимально активний у широких межах концентрацій субстрату. Таким чином, коли шлях дуже активний, то концентрація ЦТФ швидко зростає, АКТ-азна активність зменшується, і рівень кінцевого продукту падає. В протилежність цьому, АТФ стимулює синтез ЦТФ. Аспартаткарбомоїлтрансфераза E.coli – це великий білок, який складається з двох каталітичних і трьох регуляторних субодиниць. Каталітичні субодиниці містять тільки каталітичні центри, на них не впливає ні ЦТФ, ні АТФ. Регуляторні центри не каталізують реакцію, однак до них приєднуються або ЦТФ, або АТФ. Коли приєднується ефектор, від спричинює конфірмаційні зміни в регуляторному центрі і, відповідно, в каталітичному. Фермент перетворюється з менш активної Т-форми на більш активну R-форму. |
