
- •Лекція №1. Предмет і завдання біохімії
- •Загальні уявлення про обмін речовин
- •Хімічний склад живого організму
- •Клітина – основа структури живих систем
- •Історія розвитку біохімії
- •Лекція № 2 Білкові речовини
- •Функції білків
- •Класифікація амінокислот
- •Властивості амінокислот
- •Кольорові реакції на амінокислоти
- •Методи визначення амінокислот
- •Будова білків
- •Фізико-хімічні властивості білків
- •Шляхи виділення та розділення білків
- •Методи визначення білка
- •Класифікація білків
- •Природні пептиди
- •Лекція № 3 Нуклеїнові кислоти
- •Властивості і будова днк
- •Будова і функції рнк
- •Нуклеозиди і нуклеотиди
- •Назви нуклеозидів та нуклеотидів
- •Лекція № 4 Вітаміни
- •Жиророзчинні вітаміни
- •1(138), 10(245) Вітаміни групи а (антиксерофтальмічний фактор).
- •Водорозчинні вітаміни
- •1(162), 10(277) Вітамін с (аскорбінова кислота)
- •Вітаміноподібні речовини
- •Антивітаміни, антиметаболіти, антибіотики
- •Лекція № 5 Вуглеводи
- •Моносахариди
- •10(216), 11Окремі представники моносахаридів
- •Дубильні речовини
- •Полісахариди
- •Лекція № 6 Ліпіди
- •Характеристика промислових жирів
- •Лекція № 7. Ферменти
- •Будова ферментів
- •Теорія ферментативного каталізу
- •Кінетика ферментативних реакцій
- •Властивості ферментів
- •Класифікація і номенклатура ферментів
- •Номенклатура ферментів
- •Класифікація ферментів
- •Характеристика окремих класів ферментів та їх промислове використання Оксидоредуктази
- •Трасферази
- •Гідролази
- •Ізомерази
- •Локалізація ферментів у клітині
- •Лекція № 8 Обмін речовин
- •Способи живлення організмів
- •Теорія біологічного окислення
- •Анаеробний розклад вуглеводів
- •Гліколіз
- •Види бродіння
- •2.Пропіоновокисле бродіння.
- •3.Маслянокисле бродіння
- •4.Ацетонобутилове бродіння.
- •5.Метановебродіння.
- •7.Спиртове бродіння.
- •Аеробний розклад вуглеводів
- •Енергетичний ефект повного розщеплення глюкози
- •Пентозний цикл (пентозофосфатний або гексозомонофосфатний шлях)
- •Гліоксилатний цикл
- •Фотосинтез
- •Біосинтез вуглеводів
- •Обмін ліпідів Розпад ліпідів
- •Окислення гліцерину
- •Окислення насичених жк
- •Енергетика -окислення жк
- •Α-окислення жк
- •Біосинтез ліпідів Біосинтез гліцерину
- •Біосинтез жк
- •Біосинтез тригліцеридів
- •Зміна жирів при зберіганні
- •Основні перетворення ліпідів
- •Обмін нуклеїнових кислот Розпад нк
- •Синтез нк
- •Обмін білків Розпад білків
- •Перетворення амінокислот
- •Нейтралізація і виведення аміаку з організму
- •Орнітиновий цикл
- •Біосинтез амінокислот
- •Біосинтез білків
- •Взаємозв’язок процесів обміну речовин у живому організмі
- •Література
Обмін нуклеїнових кислот Розпад нк
10(389), 11 НК під впливом рибонуклеаз або дезоксирибонуклеаз каталізують розпад РНК та ДНК на мононуклеотиди. Далі під дією фосфатази від них відділяється фосфорна кислота, утворюються нуклеозиди. Потім фосфорилаза каталізує розщеплення на азотисті основи та вуглеводи.
Розпад пуринових основ починається з дезамінування з утворенням з аденіну – гіпоксантину, а з гуаніну – ксантину, які в подальшому окислюються до сечової кислоти, яка виводиться з організму з сечею.
Піримідинові основи (наприклад, урацил) шляхом декількох ферментативних реакцій перетворюються в β-аланін.
Синтез нк
10(394), 11 Починається з біосинтезу рибонуклеозид-5-трифосфатів для РНК та дезоксирибонуклеозид-5-трифосфатів для ДНК.
Обмін білків Розпад білків
10(349, 352), 11 Білки, які надходять з їжею, під час послідовної дії протеолітичних ферментів розщеплюються до структурних одиниць – амінокислот і невеликої кількості простих пептидів.
Найбільш поширені протеолітичні ферменти: пепсин – у шлунку; у тонкій кишці – трипсин, хімотрипсин, карбоксипептидази, амінопептидази, дипептидази (розщеплення дипептидів на амінокислоти).
Перетворення амінокислот
10(359), 1(337) В основі перетворення амінокислот лежать такі основні види реакцій:
1. Перетворення за аміногрупою включає дезамінування та переамінування.
Дезамінування – це процес відщеплення аміногрупи від амінокислоти з утворенням молекули аміаку. Розрізняють
– окислювальне дезамінування (під впливом дегідрогеназ):

– відновне дезамінування:

– гідролітичне дезамінування:

– внутрішньомолекулярне переамінування:

Переамінування – перенесення аміногруп з амінокислоти на кетокислоти під дією амінотрансфераз, коферментом яких є фосфорний ефір вітаміну В6:

2. Перетворення з карбоксильною групою – це реакції декарбоксилування, які поширені в тваринних і рослинних організмах та відбуваються під дією декарбоксилази:
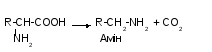
3. Реакції за радикалом, що специфічні майже для кожної амінокислоти.
Нейтралізація і виведення аміаку з організму
10(367) Кінцевими продуктами розщеплення амінокислот є аміак, вода і діоксид вуглецю.
Для людини та високоорганізованих тварин аміак є токсичною речовиною, яка особливо шкідливо впливає на центральну нервову систему, порушує процеси тканинного дихання. Тому аміак відразу є зв’язується з утворенням нетоксичних для організму сполук.
Одним з найважливіших методів знешкодження аміаку є взаємодія з аспарагіновою та глютаміновою кислотами. Обидві реакції відбуваються за участю енергії АТФ, їх каталізують синтетази, утворюються аміди:

Орнітиновий цикл
10(368), 1(351) В організмах людини і тварин основним методом знешкодження аміаку є утворення сечовини. На підставі досліджень І.П.Павлова, Г.А.Кребса тощо встановлено, що процес синтезу сечовини відбувається в кілька стадій (орнітиновийцикл):



Орнітин знову може включитись в орнітиновий цикл.
