
olymp_2014_task
.pdf
Факультет естественных наук |
Новосибирский государственный университет |
Новосибирский институт органической химии им. Н.Н. Ворожцова СО РАН |
ШЕСТАЯ ОЛИМПИАДА |
ПО ОРГАНИЧЕСКОЙ |
ХИМИИ ДЛЯ СТУДЕНТОВ |
1-3 КУРСОВ |
Новосибирск |
30 марта 2014 г. |

Задача 1. (30 баллов)
Бисфосфонаты представляют собой класс препаратов, предотвращающих потерю костной массы и используемых для лечения остеопороза и аналогичных заболеваний. При действии на бисфосфонат БФ йодистым метилом в присутствии гидрида натрия было выделено два основных продукта А и Б. При обработке того же бисфосфоната БФ йодистым метилом без гидрида натрия образуется продукт В, который при обработке водной щелочью даёт соединение Б. Изобразите структурные формулы соединений А, Б и В.
Задача 2. (30 баллов)
Производные бензопирана обладают широким спектром биологической активности (спазмолитики, антикоагулянты, противораковые средства и др.). Недавно была предложена удобная и высокопродуктивная однореакторная методика синтеза подобных соединений. Она базируется на трёхкомпонентной реакции, осуществяемой в ионной жидкости [bmim]OH, которая также служит катализатором. На схеме изображен один из примеров этого превращения.
∙Установите строение исходных участников реакции А и В;
∙Изобразите схему превращения с участием [bmim]OH.

Задача 3. (70 баллов)
В 1934 году французский химик Хок (Hoch) опубликовал результаты своего исследования о взаимодействии избытка фенилмагнийбромида с оксимом пропиофенона 1 при повышенной температуре с последующим гидролизом, которое приводило к двум продуктам. Одним из продуктов был азиридин 2, а другому была неверно приписана структура гидроксиламина 4. В 1939 году Кембелл (Cambell) определил структуру второго продукта, которым оказался β-аминоспирт 3. В настоящее эта реакция известна как азиридиновый синтез Хока-Кембелла (Hoch-Cambell aziridine synthesis)
Механизм этого превращения долгое время оставался неизвестным, поскольку существование основного интермедиата считалось невозможным. В 1970-х годах группе Лорента (Laurent) удалось надежно установить путь превращения. Одним из ключевых свидетельств в пользу установленного механизма реакции было выделение индола 6 с выходом 3%, как одного из продуктов реакции оксима 5 с реактивом Гриньяра.
∙Предложите механизм реакции, приводящей к азиридину; (0.60)
∙Как вы думаете, почему взаимодействие оксимов с реактивами Гриньяра не приводит к
продуктам присоединения по двойной связи по аналогии с карбонильными соединениями. (0.10)
Механизм реакции Коха-Кембелла в значительной степени совпадает с механизмом перегрупировки Небера (Neber) – превращения тозилатов оксимов 7 в α-аминокетоны 8 под действием спиртового раствора этилата натрия с последующим гидролизом промежуточного продукта.
R |
|
R' |
|
NH2 |
|
|
1. EtONa, EtOH |
||
|
|
|
R' |
|
|
N |
|
|
|
O |
|
+ |
R |
|
|
|
|||
|
|
|
||
|
|
|
2. H3O |
O |
Ts |
|
|
|
|
|
|
|
|
|
7 |
|
|
|
8 |
∙Предложите механизм этого превращения. (0.20)
∙В случае R` = H протекает другая хорошо известная перегруппировка. К какому продукту она приводит? (0.10)

Задача 4. (50 баллов)
Роберт Робинсон стал лауреатом Нобелевской премии 1947 года за его исследования растительных пигментов (антоцианов) и алкалоидов. Он также предложил изображать структурную формулу бензола с кружочком в середине, использовать круглые стрелочки для обозначения движения электронов, а также установил структуры пенициллина и морфина и помог основать журнал
Tetrahedron.
Помимо этих замечательных достижений он смог получить тропинон– предшественник кокаина и атропина. Первый синтез тропинона был осуществлен Рихардом Вильштеттером. Он, начиная с цилогептанона, получил тропинон с выходом 0.75% в 15 стадий. Робинсон же, исходя из трех простых соединений, получил его с выходом 17% посредством тандемной one-pot реакции (это первая реакция такого рода, приведшая к бициклической системе – в этом случае [3,2,1] ) в 1917, а улучшенные впоследствии методики позволили поднять выход выше 90%.
∙Предложите структуру тропинона (0.4 балл) и механизм реакции, использованной Робинсоном (0.5 баллов), если один из трех исходных компонентов имел брутто формулу C5H6O5. Используйте 13C ЯМР спектр тропинона, приведеннй ниже и его брутто-формулу C8H13NO
∙Как переводится с греческого ἄνθος ? (0.1 балла)

Задача 5. (60 баллов)
Каркасные углеводороды привлекают внимание химиков в качестве интересных целей для направленного синтеза. Ниже приведена схема получения центрогексиндана Л. Восстановите схему синтеза, определите структуру углеводорода Л, молекула которого имеет группу симметрии тетраэдра (Td).
Задача 6. (30 баллов)
Бинарные соединения углерода с азотом вызывают большой интерес в качестве чрезвычайно мощных взрывчатых веществ. В 2011 году немецкими химиками было синтезировано органической соединение, содержащее только атомы углерода и азота. Ниже приведена схема его синтеза. Расшифруйте схему, предложите структуру полученного продукта, если по данным рентгеноструктурного анализа молекула продукта содержит один ароматический фрагмент.

Задача 7. (50 баллов)
В 1910 году Хинсберг (Hinsberg) описал реакцию между бензилом 1 и диэтилтиоацетатом 2. Реакция проводилась в условия конденсации Кляйзена и после гидролиза была получена дикарбоновая кислота 3.
|
|
EtO2C S CO2Et |
|
|
CO2H |
O |
O |
2 |
H3O |
+ |
Ph |
|
|
|
|
||
|
|
A |
|
|
S |
Ph |
Ph |
NaOEt, EtOH |
|
|
Ph |
|
|
|
|
|
3 CO2H
1
Больше полувека считалось, что первоначальный продукт реакции – A представляет собой диэфир, который гидролизуется при обработке кислотой. Однако в 1965 году Винберг (Wynberg) и Кореман (Kooreman) доказали, что это мнение было ошибочным. Исследователи ввели в реакцию 18О-обогащённый бензил и выделили промежуточный продукт после обработки водой. Его нагревание до 250° С привело к выделению газа, который содержал примерно половину исходного
18О.
∙Предложите структуру A (0.05) и механизм его образования (0.40);
∙Какой газ выделялся при нагревании A? (0.05)
∙Метод Хинсберга имеет ограничение на структуру синтезируемых тиофенов. О каком ограничении идет речь, какие тиофены возможно получать этим методом? (0.15)
∙Для этого метода были предложены различные модификации. Одна из них позволяет получать 3,4-дигидрокситиофены. Другая модификация позволяет получать 2-карбоксамид-5-циано тиофены. Предложите общие схемы этих методов и соответствующие механизмы. (0.35)
Задача 8. (51 баллов)
Однажды Гейзенберг был в ударе и придумал оригинальный способ получения (+)-лизергиновой кислоты – ключевого исходого соединения для получения одного известного психоактивного вещества. Увы, на утро он обнаружил лишь фрагменты записей, которые вы можете видеть ниже. Некоторые реагенты структуры промежуточных продуктов были безвозвратно утрачены.
Ребята, давайте поможем Гейзенбергу восстановить схему синтеза лизергиновой кислоты.
∙Восстановите правильную последовательность химических стадий.
∙Приведите структуры недостающих промежуточных соединений.
∙Предложите реагенты для осуществления превращения, изображенного в красном прямоугольнике.

- |
F |
|
Br |
H |
|
+ 3 |
T |
|
, |
||
PCH |
||
K |
||
|
O |
|
3 |
u |
|
B |
||
Ph |
||
- |
||
|
t |
I
BocN
MeO2C
MeO2C
|
NMe |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
I |
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
1. LiT |
|
|
|
|
|
|
ол |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ен |
|
|
|
|
|
|
|
|
|
|
|
|
ф |
|
|
|
|
|
|
|
|
|
|
|
|
u) |
|
|
|
|
|
|
|
|
|
|
|
|
-B |
|
|
|
|
|
|
|
|
|
|
|
и(t |
|
|
|
|
||
|
|
|
|
|
|
-д |
|
|
|
|
|
|
|
|
|
|
2. 2,6 |
|
|
|
|
|
|
|
|||
|
NBoc |
|
|
|
|
|
|
|
|
|
|
||
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
A |
|
|
|
A |
c |
|
|
|
|
|
|
|
|
g |
|
|
|
) |
P |
|
|
|
|
|
||
|
|
2C |
O |
|
2, |
P |
h |
|
|
|
|||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
3C |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
N,8 |
o |
|
|
|
|
|
|
||
NMeBoc |
|
|
|
|
|
0 |
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H
NMe
 H
H
I

 NBoc
NBoc
|
|
|
|
|
Ф |
М |
Д |
|
|
|
|
|
|
|
|
|
А |
|
|
|
|
|
|
||
|
|
|
, |
|
|
|
|
|
g |
A |
||
|
|
6 |
|
|
|
|
|
2 |
||||
|
0 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
, |
O |
|
|
|
С |
о |
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
||
|
|
|
|
|
|
3 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
I |
|
|
|
|
|
|
HO2C
 N
N MeH
MeH

 N H
N H
(+)-лизергиновая кислота
|
|
|
|
|
|
) |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
.5 |
|
|
|
|
|
|
|
H(0 |
|
|
|
|
|
||
O |
|
|
|
|
|
|
) |
||
K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
:1 |
|
|
|
|
/H O(1 |
|
|||||
|
|
H |
|
2 |
|
|
|
|
|
|
tO |
|
|
|
|
|
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
е |
|
|
|
|
|
|
|
ни |
||
|
|
|
|
|
|
че |
|
|
|
|
|
|
|
пя |
|
|
|
||
|
|
r, ки |
|
|
|
|
|
||
A |
|
|
|
|
|
|
|
||
CO2Me

 NHBoc
NHBoc
I

 NBoc
NBoc
|
|
|
|
|
|
MeHN |
|
|
|
|
|
|
I |
|
|
|
|
f |
н |
NBoc |
|
|
|
T |
и |
|
|
|
|
O |
|
д |
|
|
|
S |
|
и |
|
||
M |
|
|
т |
|
|
|
|
у |
|
|
|||
T |
|
л |
|
|
|
|
|
|
- |
|
l |
|
|
|
6 |
|
|
|||
|
, |
|
C |
2 |
|
|
2 |
|
|
|
|||
|
|
|
2 |
|
|
|
|
|
H |
|
|
|
|
|
C |
|
|
|
|
|
I
ДМСО, (COCl)2
BocN
CH2Cl2, -78oC
CO2Me
Br
|
|
|
3 |
|
|
|
O |
|
|
C |
|
N |
||
K |
|
|
|
|
|
|
C |
||
2 |
|
3 |
|
|
|
H |
|
||
C |
|
|
|
|
BocN
I
BocMeN



CO2Me

 NMe
NMe
I
 O
O
NMeBoc
N
Boc
MeO2C |
NMeBoc |
|
|
|
|
|
|
|
|
|
|
NBoc |
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
то |
|
|||
|
|
|
|
|
|
а |
|
|
|
|
|
|
|
|
|
з |
|
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
|
|
л |
|
|
|
II |
|
|
|
|
|
а |
|
|
|
|
|
|
||
I |
т |
|
|
|
|
- |
|
|
||
ка |
|
|
|
са |
|
|
|
|||
|
|
|
|
б |
|
|
|
|
|
|
|
|
|
б |
|
|
|
|
|
|
|
|
|
а |
|
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
H |
|
|
Г |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
|
|
|
|
,T |
|
|
||
|
|
|
|
|
e |
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
h |
|
|
|
|
|
|
|
|
P |
o |
|
|
|
|
|
|||
|
|
|
0C |
|
|
|
||||
|
|
5 |
|
|
|
|
|
|
||
LiBH4
ТГФ
O
I
NMeBoc
N
Boc
Me
N H
NBoc
MeO2C H
Задача 9. (50 баллов)
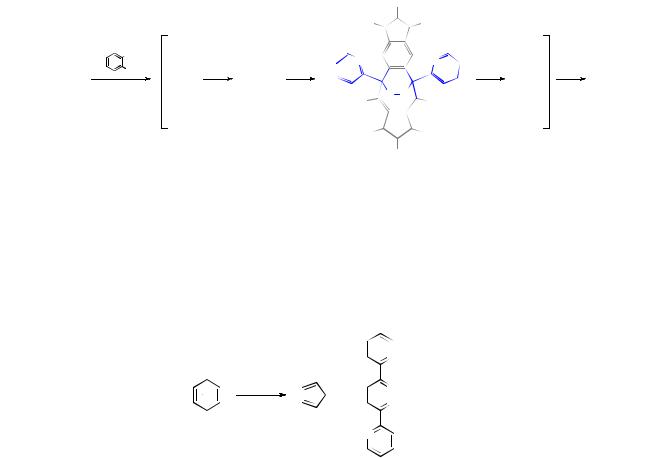
Соединения A и B впервые были введены во взаимодействие примерно 10 лет назад группой ученых из калифорнийского университета. Их изначальной целью был синтез легкомодифицируемого производного вещества B, содержащего связь N=N. Однако вместо предполагаемого продукта из реакции было выделено достаточно необычное соединение G, не содержащее этой связи. Для объяснения образования этого нетипичного продукта авторами была предложена цепочка превращений, которую мы предлагаем вам восстановить:
Известно, что соединение A и его аналоги широко используются как высокоактивные реагенты в различных реакциях Дильса– Альдера ([4+2]-циклоприсоединение), и нередко их использование приводит к протеканию цепочек тандемных превращений, сопровождающихся выделением азота:
.
Соединение B было впервые получено при лазерном облучении графита c последующей конденсацией образующихся паров. В дальнейшем был предложен более эффективный способ его синтеза, заключающийся в испарении графита в электрической дуге в атмосфере гелия. В настоящее время вещество B и его производные используются во многих научных областях и отраслях производства: от смазочных материалов до молекулярной электроники. Молекула B обладает очень высокой симметрией: в частности, имеет по несколько осей симметрии 2-го, 3-го и 5-го порядков. Соединение B обладает низкой растворимостью в большинстве органических растворителей, ввиду чего для реакций с его участием используют кипящий о-дихлорбензол (Ткип.
∙Установите строение продукта реакции G и промежуточных продуктов С, D, E, F.
∙Определите реагенты A и B
∙Что вы можете сказать о стабильности продукта реакции?
∙Определите брутто-формулу продукта реакции.

Задача 10. (39 баллов)
Безметальные нафталоцианины – фталоцианины, анелированные дополнительными ароматическими фрагментами, представляют интерес для использования в дизайне оптических материалов, материалов для органической электроники. Кроме того, недавно незамещенный нафталоцианин был использован в качестве объекта для
экспериментального изучения распределения электронной плотности в молекуле методом атомносиловой микроскопии. Серьезной проблемой при
использовании нафталоцианинов является их низкая растворимость. Одним из методов решения проблемы растворимости является добавление алкильных групп в ароматические фрагменты нафталоцианинов.
Подобные алкилированные нафталоцианины могут быть получены из алкилнафталоцианинов по схеме, изображенной справа. Ниже представлены несколько подходов к синтезу алкилированных нафталодинитрилов. Попробуйте воспроизвести схемы синтеза, выбрав необходимые реагенты из имеющихся.
Задача 11. (26 баллов)
Использование именных реакций – славная традиция органической химии, специфичная только для нашей области науки. Вам предлогается привести схемы широкоизвестных реакций, встечающиеся в заданиях олимпиады.
Название |
Схема реакции |
|
|
Бекман |
|
|
|
Виттиг |
|
|
|
Джонс |
|
|
|
Дильс-Альдер |
|
|
|
Кневенагель |
|
|
|
Кумада |
|
|
|
Михаэль |
|
|
|
Сверн |
|
|
|
Фаворский |
|
|
|
Фридель-Крафтс |
|
|
|
Хек |
|
|
|
Циглер |
|
|
|
Олефиновый |
|
метатезис |
|
|
|
