
seminar2
.pdf
Семинар 2. ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНЫХ МАСС ПОЛИМЕРОВ (продолжение)
Седиментационное равновесие в двухкомпонентной системе
В системе, подвергающейся действию сильного гравитационного-поля, гравитационный потенциал вносит заметный вклад в химические потенциалы различных компонентов. Для растворенного вещества с молекулярным весом М2, помещенного на расстоянии r от оси вращения в центрифугу, вращающуюся с угловой скоростью ω, химический потенциал имеет следующий вид:
μ2 = μ2o + RT ln(γ2c2 ) − M 2ω2 2r2
По условию химического равновесия μ2 должно быть инвариантно по всей системе, т. е.
dμ2 |
∂μ2 |
|
dP |
|
∂μ2 |
|
dc2 |
|
2 |
|
|
|
|
−M 2ω |
r = 0 |
||||||||
|
= |
|
|
|
+ |
|
|
|
|
||
dr |
∂P |
|
∂c2 |
dr |
|
||||||
|
c2 dr |
|
P |
|
|
|
|||||
Используя соотношения |
|
|
|
|
|
|
|
|
|
|
|
|
∂μ |
|
|
|
|
|
|
|
|
|
|
dP |
= ρω2r , |
2 |
=V |
= M |
|
v |
|
|
|||||||
|
|
|
2 |
2 |
, |
|
|||||||
|
|
|
|||||||||||
|
∂P |
c |
2 |
|
|
|
|
dr |
|
||||
2 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
где ρ — плотность раствора, V2 – парциальный мольный объем полимера, v2 – парциальный удельный объем
полимера, и подставляя их в уравнение, молекулярный вес растворенного вещества можно связать с его градиентом концентрации посредством уравнения
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
M 2 (1−v2 ρ)ω |
rc2 |
= 1 |
+c2 |
∂ln γ2 |
|
|
dc2 |
. |
||||||
|
||||||||||||||
RT |
|
|
|
∂c |
|
|
dr |
|||||||
|
|
|
|
|
2 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
Член (1−v2 ρ) отражает влияние подъемной силы среды, в которой суспендированы макромолекулы. Если этот член
положителен, молекулы будут оседать (т. е. перемещаться от центра вращения), а отрицательное значение (1−v2 ρ)
будет приводить к флотации в противоположном направлении.
Интерпретация данных достаточно проста, если эксперимент проводили при условиях, в которых приложим закон Рауля. В этом случае (дInγ2/дс2) = 0, и зависимость In c2 от r2 является линейной. После оценки парциального удельного объема v2 по угловому коэффициенту этой зависимости можно рассчитать молекулярный вес растворенного вещества. Если макромолекулы растворены не в Θ-растворителе, следует учитывать вклад второго члена, стоящего в скобках правой части уравнения. Из уравнения Дюгема — Гиббса можно показать, что (дInγу2/дс2)р связано с вириальными коэффициентами осмотического давления следующим образом:
|
∂ln γ2 |
|
|
|
|
|
= 2A2 M 2 +3A3M 2c2 +... |
||
|
||||
|
∂c2 |
|
||
|
P |
|
Таким образом, уравнение можно переписать в виде
|
|
2 |
|
|
|
|
|
|
|
|
|
|
rc2 |
RT |
|
|
|
|
|||
(1−v2 ρ)ω |
|
2 |
|
|||||||
|
|
|
|
|
= |
|
(1 |
+2A2 M2c2 |
+3A3M2c2 |
+...) |
|
|
dc2 |
|
|
M2 |
|||||
|
|
|
|
|
|
|
|
|
||
dr
Отсюда видно, что для неидеальных растворов зависимость Inc2 от r2 перестает быть линейной. Однако угловой коэффициент будет уменьшаться с увеличением значений r.
Метод седиментационного равновесия
В этом методе термодинамическое равновесие достигается путем выравнивания скоростей седиментации и диффузии. Для достижения равновесия центрифуга должна вращаться с меньшей скоростью в течение большего времени. Для того чтобы достичь равновесия, обычно требуется несколько дней. Скорость вращения при этом поддерживается около 15000 об/мин. Под действием центробежной силы, соответствующей этой скорости, достигается равновесный градиент концентрации вдоль кюветы и макромолекулы распределяются в соответствии со своими молекулярными массами, как показано на рис. 13.21.
При равновесии тенденция молекул к диффузии в зоны меньшей концентрации (т.е. к оси вращения) уравновешивается противоположной тенденцией молекул полимера к седиментации. Так как при этом седиментационные и диффузионные силы сбалансированы, молекулярная масса определяется по уравнению
1

Са и Сb — значения концентрации в клювете на расстояниях X1 и Х2 от оси вращения. Теоретически, поскольку макромолекулы распределяются в кювете центрифуги в
соответствии со своими молекулярными размерами, метод равновесной седиментации может быть использован для получения молекулярно-массового распределения. Однако эта процедура очень трудоемка и требует много времени.
На рис. 13.22 схематически показано устройство обычной аналитической центрифуги.
Рис. 13. 22. Схема устройства ультрацентрифуги 1 — камера; 2 — ротор; 3 — вакуумная камера; 4 — источник света (ртутная лампа) ; 5 — конденсирующие
линзы; 6 — отражающая призма; 7 — шкала; 8 — кварцевое окошко; 9 — кювета с раствором с кварцевыми окошками; 10 — электромотор.
Вращение центрифуги обеспечивает ротор из алюминиевого или титанового сплава, позволяющий достигать очень высоких скоростей вращения. Современная центрифуга дает от 2000 до 65 000 об/мин. Обычно ротор приводится во вращение электрическим способом, но иногда применяют также воздушные турбины и другие методы. Раствор полимера, молекулярная масса которого должна быть определена, помещают в кювету ротора. Фотокамера фиксирует вид кюветы в разные моменты времени, для того чтобы можно было рассчитать скорость седиментации, как было показано выше. Кроме того, в различных сечениях раствора измеряются показатели преломления. Для повышения точности эксперимента рекомендуется применять обеспыленные растворители, имеющие относительно низкую вязкость. Плотности и показатели преломления растворителя и раствора должны существенно различаться. Максимальная разница в плотностях растворителя и раствора обеспечивает наиболее эффективную седиментацию.
СВЕТОРАССЕЯНИЕ
Известно, что наиболее красивые явления природы, такие, как радуга, красочные рассветы и закаты, голубизна неба и моря, так или иначе связаны с явлением рассеяния света, которое происходит в том случае, когда луч света встречается с какими-либо материальными частицами.
Светорассеяние используют для измерения среднемассовой молекулярной массы Mw полимеров. Это возможно, потому что не только твердые частицы в воздухе, но и молекулы растворенного вещества в растворе способны рассеивать свет. На самом деле, светорассеяние в растворах и жидких смесях происходит в результате изменений плотности или показателя преломления в системе, связанных с ее композиционной неоднородностью.
Во всех случаях светорассеяния амплитуда рассеяния пропорциональна массе Μ частицы, рассеивающей свет. Однако экспериментально определяемой величиной является интенсивность рассеянного света, пропорциональная квадрату амплитуды. В 1944 г. Дебай вывел уравнение, связывающее молекулярную массу частиц растворенного вещества с интенсивностью рассеянного света. Это уравнение, известное как уравнение Дебая, справедливо только для частиц размера, меньшего длины волны падающего света, и выглядит следующим образом:
2

где В — второй вириальный коэффициент; c — концентрация раствора; R90 — так называемое отношение Рэлея при угле наблюдения 90°. Это отношение обозначается как Rθ и равно
где iθ — интенсивность рассеянного света на единицу объема V рассеивающей среды, наблюдаемая на расстоянии r и под углом Θ по отношению к падающему свету; Io - интенсивность падающего света.
В уравнении Θ = 90°, τ – мутность среды, возникающая в результате светорассеяния. Рассмотрим, как эта величина связана с интенсивностью падающего света. Если при прохождении луча света через слой среды толщины X интенсивность света уменьшается от Io до I, то мутность среды определяется как
К и Η в уравнении – калибровочные константы, определяемые как
где n — показатель преломления раствора; dn/dc — удельный инкремент показателя преломления, т.е. изменение показателя преломления с концентрацией; λ — длина волны падающего света; ΝΑ — число Авогадро.
Заметим, что в том случае, когда молекулы растворенного вещества имеют размеры, превышающие длину волны падающего света, уравнение должно быть модифицировано.
В случае раствора полимера полимерные молекулы имеют форму случайно свернутых набухших цепей, причем рассеяние происходит одновременно на разных частях макромолекулярного клубка (обозначенных как А и В на рис. 13.23).
Рис. 13.23. Рассеяние света молекулой полимера.
Поэтому световая волна, достигающая областей А и В в один и тот же момент времени, имеет разные фазы. В результате волны света, рассеянного разными частями одной частицы, интерферируют, что приводит к уменьшению интенсивности рассеянного света при наблюдении его под углом Θ. Другими словами, величина Rθ меняется при изменении Θ. Дебай показал, что в таких условиях уравнение переходит в
где Ρ(θ) — молекулярный фактор рассеяния, описывающий угловую зависимость рассеянного света в соответствии с
Ρ(θ) может рассматриваться как поправочный коэффициент, позволяющий учитывать
3
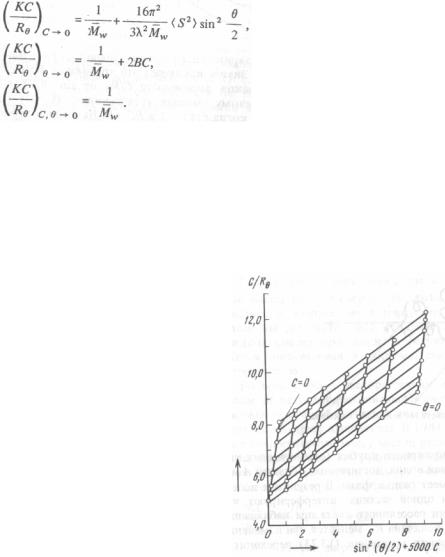
зависимость интенсивности рассеянного света от значения угла Θ, так что Ρ(θ) = 1 при θ = 0. Аналогично ВС = 0 при С = 0. Теперь уравнение может быть переписано следующим образом:
Существует два метода (а именно Дебая и Зима), которые позволяют с помощью уравнений, приведенных выше определить молекулярную массу полимера. Метод Дебая, включающий определение молекулярного фактора рассеяния Ρ(θ), требует предварительного точного знания формы макромолекулы в растворе. Метод Зимма исключает это требование благодаря двойной экстраполяции графиков зависимости с/Rθ от sin2(θ/2) + kс (k — некая константа) к нулевому значению угла рассеяния (θ = 0) и нулевой концентрации (с = 0), когда Ρ(θ) = 1 и ВС = 0. Начальный отрезок на оси ординат дает значение 1/KMW. Диаграмма Зимма для образца анионного полистирола в толуоле показана на рис. 13.24.
Рис. 13.24. Характерная диаграмма Зима.
Из диаграммы Зимма можно рассчитать молекулярную массу, второй вириальный коэффициент и среднеквадратичный радиус инерции.
Светорассеяние является удобным методом определения молекулярных масс полимеров в диапазоне от 10000 до 10000000. Этот метод требует экспериментального определения Rθ или τ с использованием нефелометра, n и dn/dc с использованием дифференциального рефрактометра. Схема нефелометра изображена на рис. 13.25.
4

Ρис. 13.25. Схема устройства установки для светорассеяния (нефелометра)
1 — подвижная фотоячейка; 2 — ячейка сравнения; 3 — калибровочный стандарт для определения мутности прозрачного стекла; 4 — ячейка с раствором; 5 — термостат; 6 — поляризатор; 7 — расщепитель светового пучка; 8 — ахроматор; 9 — щель: 10 — конденсирующие линзы; 11 — интерференционный фильтр; 12 — источник света (ртутная лампа) ; 13 — светонакопитель.
Свет, идущий от источника 12, проходит через конденсирующие линзы 10 и монохроматизирующий фильтр 11, затем он проходит через щель 7 и попадает в ахроматор 8. После расщепления в устройстве 7 и прохождения через поляроид 6 луч света попадает на образец, т.е. раствор полимера, помещенный в кювету 4. После прохождения через раствор свет попадает в накопитель 13, затем свет, рассеянный раствором и калибровочным эталоном 3, попадает на фотоэлементы 1 и 2 соответственно.
Теоретически мутность может быть определена из интенсивности рассеяния, но для этого нужна точная информация о геометрии нефелометра, расстояние от центра рассеяния до фотоэлемента и т.д. Измерение всех этих параметров достаточно сложно. Использование калибровочных эталонов позволяет решить эту проблему. Обычно используемыми эталонами являются органические жидкости, коллоидальные суспензии и даже хорошо откалиброванные полимерные системы. Значения рассеяния для этих веществ получают в условиях, идентичных условиям, в которых находится исследуемый образец. Сравнение этих результатов позволяет пренебречь деталями, упомянутыми выше.
Для определения Mw, кроме значений рассеяния, надо знать концентрации раствора полимера, показатель преломления растворителя и разницу в показателях преломления растворов разной концентрации и растворителя. Основной предосторожностью, которая должна быть предпринята при проведении экспериментов по светорассеянию, является полное обеспылевание растворов. Для этой цели обычно применяют высокоскоростную центрифугу. Кроме того, в ходе эксперимента необходимо поддерживать постоянную температуру раствора.
КРИВАЯ МОЛЕКУЛЯРНО-МАССОВОГО РАСПРЕДЕЛЕНИЯ (ММР)
В том случае, когда образец полимера расфракционирован на несколько фракций, для каждой из которых определена общая масса и средняя молекулярная масса, расчет кривой молекулярно-массового распределения не представляет трудностей. Заметим, что, чем больше число фракций, тем точнее построена кривая молекулярно-массового распределения. Теоретически, если бы можно было разделить образец на полностью монодисперсные фракции, т.е. каждая фракция содержала бы молекулы только одной степени полимеризации, мы получили бы точное воспроизведение молекулярно-массового распределения. Однако на практике такое фракционирование невозможно, и самое большее, что может быть сделано, это разделение образца на максимально возможное число фракций с последующим фракционированием каждой из них на более узкие. Таким путем получают наиболее однородные фракции.
Рассмотрим гипотетический случай, когда образец разделен на 10 фракций. Откладывая массовый процент (мас.%) каждой фракции от молекулярной массы можно построить кривую,
5

как показано на рис. 13.26.
Рис. 13.26. Простая кривая молекулярно-массового распределения. Рис. 13. 27. Зависимость Wi от Mi для гипотетического образца полимера.
Это очень простой способ построения кривой молекулярно-массового распределения, позволяющий в большей или меньшей степени представить характер истинного распределения в образце при условии, что разница в молекулярных массах последовательных фракций постоянна, как в приведенном примере. Однако на практике очень трудно получить такие фракции, и обычно разница в молекулярных массах соседних фракций – величина произвольная. В этом случае простая кривая зависимости не отражает истинного распределения в образце (рис. 13.27). Чтобы обойти эту трудность, рассчитывают кумулятивную массу Σwν (т.е. массу суммы всех фракций со средней молекулярной массой, не превышающей Мi) и строят график ее зависимости от Мi , как показано на рис. 13.28.
Рис. 13.28. Интегральная кривая молекулярно-массового распределения для случая, представленного на рис. 13.27.
Рис. 13.29. Дифференциальная кривая молекулярно-массового распределения, рассчитанная путем графического дифференцирования кривой, изображенной на рис. 13.28
Такая функция называется интегральной кривой молекулярно-массового распределения. Графическое дифференцирование этой кривой с определением тангенса угла наклона в как можно большем числе точек позволяет рассчитать дифференциальную кривую молекулярно-массового распределения (рис. 13.29),из которой легко найти процентное содержание в образце молекул данной молекулярной массы.
Применение техники ГПХ позволяет избежать громоздкой процедуры разделения образца на фракции, определения их молекулярных масс и расчета кривой распределения. С помощью ГПХ можно сразу получить кривую молекулярно-массового распределения.
ФРАКЦИОНИРОВАНИЕ ПОЛИМЕРОВ
Как уже говорилось выше, отдельные молекулы в образце полимера имеют разные молекулярные массы и образец в целом характеризуется определенной средней молекулярной массой. Однако образец можно разделить на несколько меньших образцов, имеющих более узкие ММР и характеризующихся своей собственной средней молекулярной массой. Каждый из таких меньших образцов называют фракцией исходного нефракционированного образца. Процесс разделения исходного образца на несколько фракций постепенно возрастающей (или
6

уменьшающейся) средней молекулярной массы называется фракционированием полимера. Зная массы отдельных фракций и соответствующие средние молекулярные массы, можно рассчитать кривую ММР исходного нефракционированного образца. Пример таких кривых для нефракционированного полимера и ряда его фракций приведен на рис. 13.1.
Ρ и с. 13.1. Кривые молекулярно-массового распределения ММР для нефракционированного образца (I) полимера и его фракций (II — VIII).
Пунктирные кривые соответствуют функциям распределения для полимера, остающегося в растворе после удаления каждой очередной фракции.
Однако, прежде чем обсуждать процедуру расчета кривой ММР, рассмотрим, как можно разделить исходный полимер на несколько фракций. Существует несколько экспериментальных методов, дающих такую возможность. Из них наиболее важными являются дробное осаждение, дробное растворение, проявительная и гельпроникающая хроматография.
ДРОБНОЕ ОСАЖДЕНИЕ
Если небольшое количество осадителя (совместимого с растворителем) добавить к раствору полимера в плохом растворителе (Плохой растворитель берут потому, что в этом случае осаждение полимера удается провести, используя меньшее количество осадителя), осадитель уменьшает растворяющую способность растворителя настолько, что молекулярные фракции самых больших молекулярных масс уже не могут оставаться в растворе и выпадают из него в виде набухшего геля. Если удалить этот гель и снова добавить к раствору некоторое количество осадителя, растворяющая способность растворителя снова уменьшится и из раствора выпадает еще одна порция полимера наибольшей молекулярной массы. Таким образом, при добавлении каждой порции осадителя к раствору полимера происходит его частичное осаждение. На этом принципе и основан метод дробного осаждения.
Основное различие между дробным осаждением и очисткой методом осаждения заключается в относительных количествах раствора полимера и осадителя. В первом случае к большому объему раствора добавляют небольшие порции осадителя, тогда как во втором случае небольшое количество раствора добавляют к большому объему осадителя.
Методически дробное осаждение проводят следующим образом. 1%-ный раствор полимера в плохом растворителе помещают в сосуд достаточно большой емкости с учетом необходимости перемешивания и постепенного добавления осадителя. Этот сосуд термостатируют, поддерживая температуру раствора постоянной с точностью ±0,01°. Так как растворение и осаждение — процессы обратимые, они чувствительны к небольшим изменениям температуры. Поэтому для эффективного проведения фракционирования необходим строгий температурный контроль. После того как достигнута требуемая температура, начинают по каплям добавлять осадитель при постоянном перемешивании. По мере добавления осадителя раствор мутнеет, что свидетельствует об осаждении фракций полимера наибольшей молекулярной массы. Когда мутность становится значительной, прикапывание осадителя прекращают и медленно подогревают содержимое сосуда до исчезновения мутности. При нагревании выпавший в осадок полимер снова растворяется. После этого перемешивание прекращают и дают раствору медленно остыть до исходной температуры. Мутность появляется снова. Такая процедура позволяет достичь истинного равновесия между растворенными низкомолекулярными фракциями и осажденными
7
высокомолекулярными. Систему выдерживают при постоянной температуре достаточно длительное время (8-10 ч) для того, чтобы высадившийся полимер образовал желеобразный осадок, который осторожно отделяют, не взбалтывая прозрачный раствор. После удаления геля к раствору добавляют новую порцию осадителя до появления мутности, и вся последовательность операций повторяется до получения второй фракции. Повторив процедуру несколько раз, можно выделить несколько фракций. Последнюю фракцию можно получить, просто выпарив полимер из раствора.
Существует несколько модификаций методики дробного осаждения. Один из методов заключается в охлаждении раствора полимера (в одном растворителе). Этот метод очень прост. Раствор приготавливают при повышенной температуре (например, 80°С), а затем медленно охлаждают, выдерживая его некоторое время при более низкой температуре (например, 75°С). При этом наиболее высокомолекулярная фракция выпадает из раствора и ее осторожно извлекают. Раствор продолжают медленно охлаждать и выдерживают его при следующей температуре (например, 70°С), когда выпадает в осадок вторая фракция. Процесс продолжают до получения нескольких фракций. Недостатком этого метода является то, что для осаждения некоторых полимеров одного охлаждения недостаточно.
Другой разновидностью дробного осаждения является метод испарения растворителя. Полимер растворяют в бинарной смеси растворитель-осадитель, которую подбирают таким образом, чтобы растворитель был более летуч, чем осадитель. Медленно понижая давление пара над раствором полимера, растворитель постепенно испаряют. При этом раствор оказывается обогащен осадителем, полимер начинает высаживаться, первыми выпадают в осадок высокомолекулярные фракции. Контролируя испарение растворителя и отбирая порции осаждающегося полимера, можно разделить его на фракции.
ДРОБНОЕ РАСТВОРЕНИЕ (ЭКСТРАКЦИЯ)
Метод дробного растворения основан на том, что растворимость полимера в растворителе ограничена его молекулярной массой. Плохой растворитель растворяет только низкомолекулярные фракции полимера, хороший растворяет также и высокомолекулярные фракции. Если есть серия растворителей с возрастающей растворяющей способностью, то, используя их по отдельности, начиная с растворителя с минимальной растворяющей способностью, можно растворять фракции с различными молекулярными массами одну за другой, начиная с самой низкомолекулярной.
Для проведения дробного растворения берется порошок или маленький кусочек твердого полимера. В качестве серии растворителей с возрастающей растворяющей способностью используют смеси растворителя с осадителем, взятых в разных пропорциях. Чем меньше относительное содержание растворителя в смеси, тем, естественно, меньше ее растворяющая способность. К порошку полимера добавляют смесь с наименьшей растворяющей способностью, дают ему набухнуть и затем хорошо перемешивают для ускорения растворения фракции с наименьшей молекулярной массой. В зависимости от природы полимера время перемешивания подбирают так, чтобы достичь полного растворения всех растворимых компонентов. После окончания перемешивания раствор фильтруют и выпаривают фильтрат. После полного испарения растворителя остается первая фракция. К набухшей массе, оставшейся не растворенной после добавления первой порции бинарной смеси растворитель-осадитель (т.е. твердого остатка фильтрования), добавляют следующую порцию бинарной смеси, обладающую большей растворяющей способностью, перемешивают и повторяют всю процедуру до получения второй фракции. Этим путем, применяя смеси со все возрастающей растворяющей способностью, получают серии фракций полимера с возрастающей молекулярной массой.
ФРАКЦИОНИРОВАНИЕ ЭЛЮИРОВАНИЕМ (ПРОЯВИТЕЛЬНАЯ ХРОМАТОГРАФИЯ)
Методика элюирования также основана на принципе частичного растворения, изложенном выше. По этой методике полимер помещают на стекловате в верхней части колонки, заполненной силикагелем или алюмогелем, как показано на рис. 13.2. Полимер последовательно элюируют смесью растворитель-осадитель постепенно возрастающей растворяющей способности. Фракция
8
наименьшей молекулярной массы элюируется первой, наибольшей — последней. Эффективность метода возрастает при поддержании градиента температуры в колонке. В верхней части колонки температура несколько выше, чем в нижней. Градиент температуры позволяет проводить серии растворений и осаждений каждой молекулярной фракции на различных уровнях колонки, что повышает эффективность фракционирования.
 Рис. 13.2. Схема лабораторной установки для фракционирования методом элюирования 1 — смесь растворителя с осадителем; 2 — стеклянная вата с порошком полимера; 3 — силикаили
Рис. 13.2. Схема лабораторной установки для фракционирования методом элюирования 1 — смесь растворителя с осадителем; 2 — стеклянная вата с порошком полимера; 3 — силикаили
алюмогелевый наполнитель; 4 — кран для регулирования протекания растворителя; 5 — коллектор фракций.
ГЕЛЬ-ПРОНИКАЮЩАЯ ХРОМАТОГРАФИЯ
Гель-проникающая хроматография (ГПХ) является довольно быстрым и эффективным методом фракционирования полимеров с одновременным расчетом кривой молекулярномассового распределения.
Принцип ГПХ заключается в следующем. В любой колоночной хроматографии при движении растворенного вещества от одного конца колонки к другому оно переходит из одной фазы (неподвижной) в другую (подвижную). В жидкоадсорбционной хроматографии неподвижной фазой является твердое вещество (силикагель, алюмогель или переплавленный стеклянный порошок, которыми набита колонка), а мобильной — жидкость (т.е. растворитель, элюирующий растворенное вещество). В жидкостной хроматографии обе фазы — жидкости, не смешивающиеся друг с другом.
Однако в ГПХ простая жидкость, а именно сам растворитель, действует и как неподвижная, и как подвижная фаза. Как это может осуществляться? Колонка в ГПХ наполнена материалом, который называется гелем (Термин "гель" используется здесь в смысле, отличном от того смысла, который вкладывался в него раньше), представляющим собой мельчайшие сферические частицы (обычно диаметра 100 мкм) сшитого сополимера стирола с дивинил бензолом или стекла, содержащие множество микропор одинакового размера. Частицы геля являются твердыми и несжимаемыми и обладают разной степенью пористости — размер пор меняется от 50 до 1000 А. Колонка может быть наполнена частицами одной или разных степеней пористости. Когда колонку наполняют подходящим растворителем, он заполняет не только объем, не занятый частицами геля (объем пустот), но и объем пор внутри этих частиц. Фаза растворителя, занимающая объем пустот, выступает в роли подвижной фазы, тогда как растворитель, занимающий поры, выступает в роли неподвижной фазы (рис. 13.3).
9

Рис. 13.3. Схематическое изображение частиц геля (1), неподвижной (объем пор) (2) и подвижной (объем пустот) (3) фаз в колонке ГПХ.
Метод ГПХ основывается на предположении о том, что разделение происходит только по размерам молекул полимера, без участия химических взаимодействий. Разделение происходит благодаря различию гидродинамических объемов полимерных молекул разных молекулярных масс в растворенном состоянии. Когда разбавленный раствор полимера (например, 0,5%-ной концентрации) вводят в верхнюю часть колонки, а затем элюируют растворителем, полимерный раствор вместе с растворителем начинает стекать по колонке сверху вниз. Подвижная фаза, находящаяся между частицами геля, содержит молекулы полимера, тогда как в неподвижной фазе, внутри этих частиц, молекул полимера нет. Благодаря разнице в концентрациях полимера между подвижной и неподвижной фазами молекулы полимера начинают диффундировать внутрь частиц геля, стремясь выравнять концентрацию. Однако размер пор ограничивает доступность частиц геля, позволяя проникать туда лишь молекулам, не превышающим определенный гидродинамический размер. Молекулы большего размера оказываются неспособными проникнуть внутрь геля и вымываются раство рителем из колонки. Таким образом, наиболее высокомолекулярная фракция элюируется из колонки первой.
Среди тех молекул, которые способны проникнуть в поры геля, быстрее всего туда проникают молекулы наиболее низкомолекулярных фракций, имеющие минимальные гидродинамические размеры, они же занимают большую часть объема пор, тогда как молекулы средних размеров проникают в поры медленнее и занимают лишь часть объема пор. Если после этого еще раз промыть колонку чистым растворителем, то подвижная фаза уже не будет содержать молекул полимера, а неподвижная будет обогащена ими, и градиент концентрации заставит молекулы полимера диффундировать в противоположном направлении — из пор.
В таком диффузионном процессе (внутрь и из объема пор) молекулы, имеющие наименьшую молекулярную массу, удерживаются в колонке дольше всего и элюируются последними. Молекулы промежуточных размеров занимают промежуточное положение и по времени элюирования.
Если обозначить объем пор как Vп, а объем пустот между ними как Vо, то самые большие молекулы, которые совсем не проникают в поры, элюируются из колонки сразу после впрыскивания образца, когда элюируется объем растворителя, равный Vо. Самые маленькие молекулы, занимающие максимальный объем пор, элюируются с объемом растворителя, равным Vо + Vп. Молекулы промежуточных размеров элюируются в интервале от Vо до Vо + Vп. Таким образом, объем элюата непосредственно дает оценку молекулярных размеров. Однако на практике величины Vо и Vп не рассчитывают, а строят калибровочные кривые в координатах logМ
— Vп, используя стандартные серии полимеров известных молекулярных масс с узким молекулярно-массовым распределением.
На хроматограммах таких стандартных образцов отмечают объемы элюата, соответствующие пику, полученному для каждого стандартного образца (рис. 13.4). Зная молекулярные массы стандартов и соответствующие им объемы элюата, строят калибровочную кривую (рис. 3.15). Такой способ калибровки дает хорошие результаты при условии, что ММР стандартов достаточно узкое (Mw/Mn < 1,2) и стандарты принадлежат к тому же химическому классу, что и исследуемый полимер.
10
