
- •Ответы на вопросы,
- •Распространенность атомов в ос
- •3. Круговорот кислорода в окружающей среде
- •4. Круговорот азота в окружающей среде
- •5. Круговорот углерода в окружающей среде
- •6. Солнечная радиация и ее преобразование. Энергетический баланс Земли. Распределение составляющих энергетического баланса.
- •7. Основные компоненты современной атмосферы. Температурный профиль атмосферы.
- •8. Неорганические, органические компоненты атмосферы. Аэроионы.
- •Аэроионы
- •9. Химические превращения соединений в атмосфере. Реакционноспособные частицы атмосферы. Озон. Молекулярный и атомарный кислород
- •10. Химические превращения соединений в атмосфере. Гидроксильный и гидропероксидный радикалы.
- •11. Химические превращения соединений в атмосфере. Оксиды азота. Диоксиды серы.
- •12. Фотохимическое окисление метана (схема превращений). Реакции гомологов метана. Атмосферная химия углеводородов. Алкены.
- •13. Химические превращения соединений в атмосфере. Бензол и его гомологи.
- •14. Фотохимия производных углеводородов. Альдегиды и кетоны.
- •15. Фотохимия производных углеводородов. Карбоновые кислоты и спирты. Амины и серосодержащие соединения.
- •16. Фотохимия загрязненной атмосферы городов. Фотохимическое образование смога.
- •17. Атмосферная химия галогенсодержащих соединений. Влияние окислов азота и галогенсодержащих органических соединений на слой озона.
- •18. Химия загрязненной атмосферы городов. Разрушение металлов, облицовки зданий, стекол. Проблема гибели лесов.
- •19. Основные виды природных вод. Классификация вод.
- •20. Группы, типы, классы, семейства, роды вод. Общая минерализация вод.
- •21. Ведущие и редкие ионы природных вод. Классификация природных вод по составу ионов.
- •22. Энергетическая характеристика ионов. Кислотно-основное равновесие в природных водоемах.
- •23. Окислительно-восстановительные условия природных вод.
- •24. Диаграмма стабильности воды ( ре-рН ).
- •26. Общая щелочность вод. Процессы закисления поверхностных водоемов.
- •27. Основные свойства воды. Газы природных вод
- •Газы природных вод
- •30. Загрязнения грунтовых, речных и морских вод органическими остатками.
- •31. Загрязнения грунтовых, речных и морских вод неорганическими остатками.
- •2 Кислотные выбросы.
- •32. Загрязнения грунтовых, речных и морских вод тяжелыми металлами.
- •33. Коррозия металлов в водной среде. Факторы, влияющие на интенсивность процесса коррозии.
- •34. Разрушение бетона и железобетона под действием воды.
- •35. Образование почвенного слоя. Классификация почвенных частиц по крупности и механическому составу.
- •Классификация почвенных частиц по их крупности
- •35. Элементный и фазовый состав почв.
- •37. Влагоемкость, водопроницаемость почв. Различные формы воды в почве.
- •38. Почвенные растворы.
- •39. Катионно-обменная способность почв. Поглотительная способность почвы. Селективность катионного обмена.
- •40. Формы соединений алюминия в почвах. Виды почвенной кислотности.
- •41. Соединения кремния и алюмосиликаты в почвах.
- •42. Минеральные и органические соединения углерода в почве. Значение гумуса. Диоксид углерода, угольная кислота и карбонаты
- •Органические вещества и их значение
- •43. Подразделение гумусовых веществ почвы.
- •44. Гумус. Специфические гумусовые соединения.
- •Фульвокислоты
- •45. Неспецифические гумусовые соединения. Негидролизуемый остаток.
- •46. Гумусовые кислоты почв.
- •47. Антропогенное загрязнение почв. Кислотное загрязнение.
- •48. Антропогенное загрязнение почв. Влияние тяжелых металлов на состояние почв и развитие растений.
- •49. Антропогенное загрязнение почв. Пестициды в почве.
- •50. Антропогенное загрязнение почв. Влияние водно-солевого режима на состояние почвы.
Фульвокислоты
Гуминовые кислоты
Гиматомелановые кислоты
Черные Бурые
(серые)
Рис. Номенклатурная схема подразделения гумусовых веществ почвы (по Орлову).
45. Неспецифические гумусовые соединения. Негидролизуемый остаток.
Неспецифические соединения – вещества, синтезируемые живыми организмами и поступающие в почву после их отмирания. Это источник фенольных соединений, пигменты, липиды, углеводы, азотсодержащие соединения, лигнин, целлюлоза, протеины, аминокислоты, моносахариды, воска, жирные кислоты. Неспецифические соединения присутствуют в почве в свободном состоянии или связаны с минеральными компонентами почвы.
Негидролизуемый остаток, почвенного гумуса включает ряд групп веществ: гумусовые кислоты, прочно связанные с минеральной частью, декарбоксилированные гумусовые вещества, утратившие способность растворяться в щелочах, неспецифические и нерастворимые органические соединения.
46. Гумусовые кислоты почв.
Гумусовые кислоты четко выделяются среди других групп по свойствам и составу; это азотсодержащие высокомолекулярные оксикарбоновые кислоты с интенсивной темно-бурой или красновато-бурой окраской. Гумусовые кислоты экстрагируются из почвы растворами щелочей, а затем по растворимости разделяются на гуминовые, гиматомелановые кислоты и фульвокислоты.
В кислой среде гуминовые и гиматомилановые кислоты выпадают в осадок, в растворе остаются фульвокислоты. Из полученного осадка можно выделить гиматомилановые кислоты; они растворяются при обработке осадка этанолом, образуя вишнево-красный раствор. Гиматомелановые кислоты долгое время включали в группу гуминовых кислот. Сейчас получено достаточно доказательств для выделения гиматомелановых кислот в особую группу.
Группа гуминовых кислот разделяется на две подгруппы: черные (серые) и бурые гуминовые кислоты. Обогащенные углеродом гуминовые кислоты (преимущественно черноземных почв) в отечественной литературе наз. черными, в зарубежной – серыми.
Фульвокислотами называют сумму кислоторастворимых органических веществ, выделяемых в ходе анализа группового и фракционного состава гумуса. Собственно фульвокислоты – специфические гумусовые кислоты, растворимые в водных, щелочных и кислотных растворах.
47. Антропогенное загрязнение почв. Кислотное загрязнение.
Наряду с закислением почв в результате образования сырого гумуса большой ущерб почвам наносят антропогенные кислотные загрязнения. В течение десятилетий кислотные загрязнения действуют на буферную емкость почвы. В отношении многих почв отмечается вымывание ионов, важных для питания растений. Попадающие в почву протоны замещают катионы, сорбционно связанные с коллоидными частицами почвы, и в результате эти катионы мигрируют в глубинные слои, становятся недосягаемыми для корней растений. Поэтому даже если рН почвы остается постоянным, плодородие почвы падает. Продолжающееся закисление почвы можно определить, например, по понижению концентрации ионов Fe 2+ и Mg 2+.
Ca2+
Ca2
+


Mg2+
H+
Коллоидная частица

+ H+ Mg2+
Коллоидная частица


Na+
Na+
K+ H+ К+



H+ H A - H
Fe
–OH Fe - O +
Fe - O+ A- 

H анион H


Fe
– OH - O
Fe – O

P
= O
P=O + 2 OH-

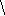

Fe – O -O OH Fe – O OH
Например, снижение рН препятствует развитию микроорганизмов, которые способствуют усвоению минеральных веществ корнями растений. Низкие значения рН способствуют присоединению анионов к железосодержащим коллоидным частицам в почве, так как протоны сообщают комплексам положительный заряд. У фосфатов возможен обмен их кислых остатков с ОН-группами на поверхности коллоидных частиц, при этом фосфатные остатки связываются и дальнейшее усвоение фосфата растениями становится невозможным.
Все изменения состава почвы, связанные с увеличением ее кислотности, подавляют рост растений.
