
Галоген- и кислородосодержащие производные
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Кузбасский государственный технический университет имени Т. Ф. Горбачева»
А. Л. Перкель Ю. В. Непомнящих С. Г. Воронина
Галоген- и кислородосодержащие производные углеводородов
Методические указания к контрольной работе № 2
Рекомендовано учебно-методической комиссией направления подготовки 240100.62 «Химическая технология» в качестве электронного издания для самостоятельной работы
Кемерово 2013
1
Рецензенты
Котельникова Т. С. - доцент кафедры технологии органических веществ и нефтехимии
Пучков С. В. - председатель учебно-методической комиссии направления подготовки 240100.62 «Химическая технология
Перкель Александр Львович. Галоген- и кислородсодержащие производные углеводородов. [Электронный ресурс]: методические указания к контрольной работе № 2 по дисциплине «Органическая химия» для студентов направления подготовки 240100.62 «Химическая технология», профили 240106.62 «Химическая технология органических веществ», 240103.62 «Химическая технология неорганических веществ», 240108.62 «Химическая технология природных энергоносителей и углеродных материалов», 240111.62 «Технология и переработка полимеров» дневной формы обучения / А. Л. Перкель, Ю. В. Непомнящих, С. Г. Воронина. – Электрон. дан. – Кемерово : КузГТУ, 2013. – Систем. требования : Pentium IV ; ОЗУ 8 Мб ; Windows 95 ; мышь. – Загл. с экрана.
Материал предназначен для оказания методической помощи студентам при самостоятельном выполнении контрольной работы 2 «Галоген- и кислородсодержащие производные углеводородов» по курсу «Органическая химия». Приведены варианты контрольных заданий и пример их решения.
©КузГТУ
©Перкель А. Л
©Непомнящих Ю. В.
©Воронина С. Г.
2
1. ВЫПИСКА ИЗ РАБОЧЕЙ ПРОГРАММЫ КУРСА
Бакалавры направления подготовки 240100.62 «Химическая технология» профилей 240106 «Химическая технология органических веществ», 240103 «Химическая технология неорганических веществ», 240108 «Химическая технология природных энергоносителей и углеродных материалов», 240111 «Технология и переработка полимеров» изучают дисциплину «Органическая химия» на 2 курсе (3 семестр).
Для изучения дисциплины отводится 288 часов, в том числе: лекции – 51 час; лабораторные занятия – 68 часов; самостоятельная работа – 133 часа. Формой промежуточной аттестации является экзамен.
Программа курса предусматривает выполнение следующих видов самостоятельной работы:
подготовка и оформление лабораторных работ;
проработка конспектов лекции;
самостоятельное изучение тем курса и решение задач;
выполнение домашних контрольных работ.
Методические указания к самостоятельной работе содержат рекомендации по выполнению домашней контрольной работы 2. Варианты заданий выдаются студентам после изучения следующих тем курса:
спирты;
простые эфиры;
альдегиды и кетоны.
2. ЦЕЛЬ РАБОТЫ
Оказание методической помощи студентам при самостоятельном выполнении домашней контрольной работы 2 «Галоген- и кислородсодержащие производные углеводородов» по курсу «Органическая химия». Приведены варианты контрольных заданий и пример их решения. Номер варианта
3
контрольного задания выдается преподавателем. Приведен список рекомендуемой литературы.
3. ПРИМЕР РЕШЕНИЯ ВАРИАНТА КОНТРОЛЬНОЙ РАБОТЫ
1.Напишите: а) метилбутилкарбинол; б) диизопропилкетон; в) 4,5-дибром-3-гексен-2-ол; г) 3,3-дихлорбутаналь. Первые два соединения назовите по систематической номенклатуре.
Решение.
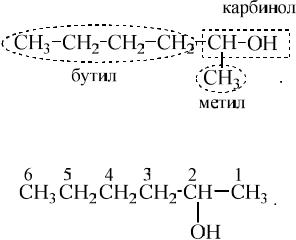
а) Соединение а названо по рациональной номенклатуре. В основе рациональной номенклатуры предельных спиртов лежит метиловый спирт (карбинол), а остальные спирты рассматриваем как производные карбинола, в котором один или несколько атомов водорода замещены на углеводородные радикалы.
Исходя из этого, можно написать формулу метилбутилкарбинола:
По систематической номенклатуре это соединение следует назвать 2-гексанол:
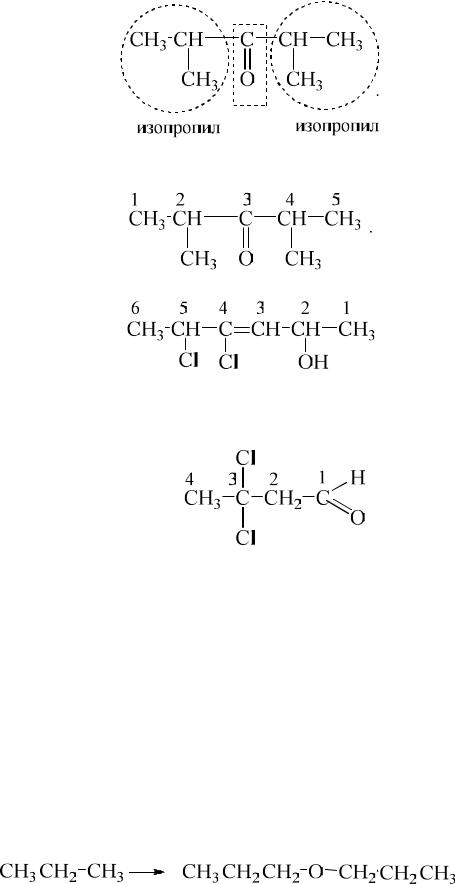
б) Соединение б названо по рациональной номенклатуре. По рациональной номенклатуре кетоны называют, перечисляя заместители при кетогруппе, добавляя затем слово «кетон». Поэтому формулу диизопропилкетона следует представить в виде:
4
По систематической номенклатуре это соединение называется 2,4-диметил-3-пентанон:
в) Соединение в названо по систематической номенклатуре:
4,5-дихлор-3-гексен-2-ол.
г) Название соединения г дано по систематической номенклатуре.
3,3-дихлорбутаналь.
2. Получите дипропиловый эфир из пропана.
Решение.
Задание 2 заключается в разработке многостадийной схемы синтеза более сложного органического соединения из менее сложного. Для его выполнения обычно используют два основных подхода: планирование от начального соединения к конечному и от конечного к исходному.
Первый подход обычно используют в более простых случаях, когда в структуре конечного продукта просматриваются структурные элементы исходного соединения.
Брутто схема превращения
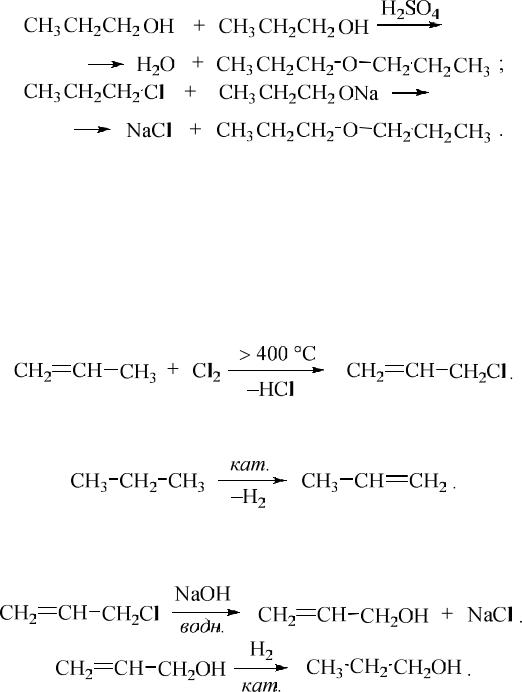
5
показывает, что для построения молекулы конечного соединения (простого эфира) требуется 6 атомов углерода, содержащихся в двух молекулах исходного вещества. Рассмотрение способов получения простых эфиров показывает, что эти соединения получают преимущественно двумя методами – межмолекулярной дегидратацией спиртов и(или) О-алкилированием соответствующих алкоголятов спиртов по Вильямсону:
Как в первом, так и во втором случаях необходимо заместить в пропане первичную связь СН на гидрокси-группу или галоген. Реакции радикального замещения, характерные для предельных углеводородов происходят преимущественно с третичными или вторичными связями СН. Рассмотрение химических свойств этиленовых углеводородов показывает, что первичную связь СН можно заместить на галоген в пропилене, например, путём высокотемпературного галогенирования:
Необходимый для этой реакции пропилен может быть получен каталитическим дегидрированием пропана:
В свою очередь образующийся при хлорировании пропилена хлористый аллил может быть превращён в аллиловый спирт, а затем и в 1-пропанол:
Общую схему получения дипропилового эфира из пропана можно представить в виде:

6
Метод планирования от конечного к исходному более универсален и связан с проведением, так называемого ретросинтетического анализа – разборки конечной молекулы с использованием ретросинтетических операций (обратных операциям синтеза). Для их обозначения обычно используется стрелка вида: .
.
Дипропиловый эфир может быть подвергнут ретросинтетической разборке с получением того же результата, что и при использовании первого подхода:
3.Напишите механизм реакции этерификации уксусной кислоты этиловым спиртом в кислой среде.
Решение.
Одной из наиболее известных реакций карбоновых кислот является их взаимодействие со спиртами (этерификация):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
|
OH |
|
|
R1OH |
|
|
|
H |
|
|
R |
|
C |
|
OR1 |
|
|
H2O. |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
||||||
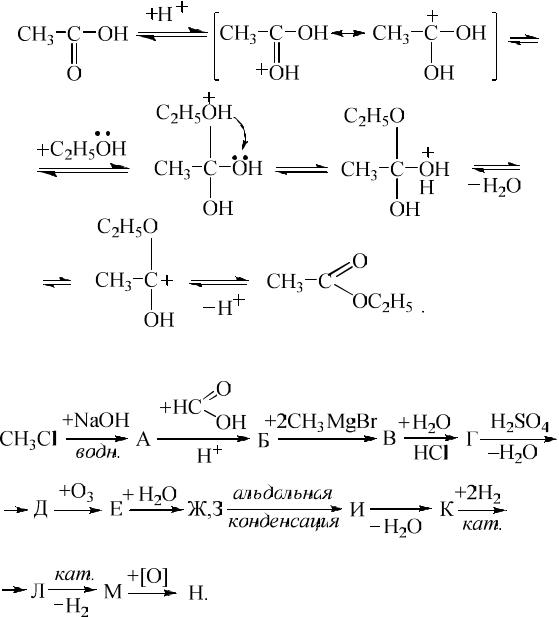
В большинстве случаев такое превращение требует кислотного катализа и протекает как нуклеофильное замещение по тетраэдрическому механизму, обозначаемому обычно ААС2 (катализируемое кислотой расщепление связи ацил-кислород, бимолекулярное):
7
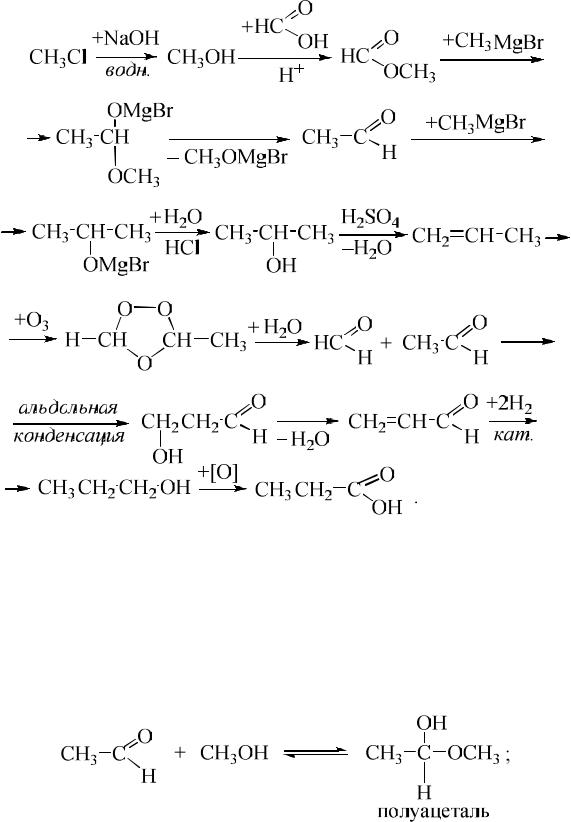
4. Осуществите превращения:
Решение.
Общий анализ схемы превращений показывает, что превращение хлорметана под действием водного раствора щелочи – это реакция замещения; продукта А в продукт Б – реакция этерификации; продукт Д – озонид, гидролиз которого приводит к образованию карбонильных соединений, вступающих затем в реакцию альдольной конденсации. С учётом этих обстоятельств схему превращений можно представить в виде:
8
5.Напишите и объясните механизм реакции образования диметилацеталя ацетальдегида в кислой среде.
Решение.
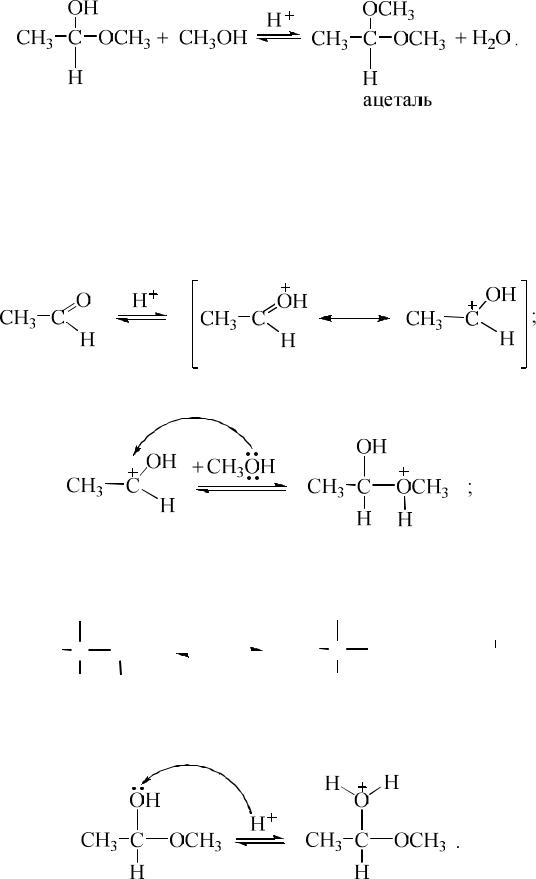
Спирты реагируют с альдегидами в две стадии: образование полуацеталя – продукта нуклеофильного присоединения по карбонильной группе 1 моля спирта и образование ацеталя – продукта О-алкилирования полуацетальной группы:
9
Первая стадия может осуществляться как без катализатора, так и в условиях кислотного катализа.
Механизм первой стадии в присутствии кислотного катализатора включает:
протонирование молекулы альдегида, которое увеличивает электрофильность атома углерода карбонильной группы:
присоединение молекулы спирта:
депротонирование продукта присоединения с образованием полуацеталя:
OH |
|
|
|
|
|
|
|
|
OH |
|||
CH3 C |
|
|
|
OCH3 |
|
|
|
CH3 C |
OCH3 + H |
|
. |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||||
H |
H |
|
|
|
H |
|
|
|
||||
Механизм образования ацеталя из полуацеталя включает:протонирование молекулы полуацеталя:
