
Коллоквиум1
.pdf
H |
|
H |
|
. |
. Cl |
H C . |
. |
H C . H |
+ H . Cl |
||
H |
|
H |
|
метан |
|
метильный радикал |
|
|
|
(NB! имеет плоское строение!) |
|
(NB! Надо иметь ввиду, что у атома хлора на внешнем уровне 7 электронов, а не 1, но для удобства здесь мы пишем только 1)
Стадия 3: Обрыв цепи. Атомы хлора или метильные радикалы взаимодействует друг с другом. Цепь ―обрывается‖:
Cl . |
+ |
Cl . |
Cl2 |
||||
CH3. + CH3. |
H3C |
|
|
CH3 |
|||
|
|
||||||
CH3. |
+ |
Cl . |
CH |
|
Cl |
||
3 |
|||||||
Взаимодействием метильных радикалов объясняется появление этана в продуктах реакции.
Напишите реакции бромирования пропана и опишите еѐ механизм.
h
H3C CH2 CH3 + Br2  H3C CH CH3 + HBr Br
H3C CH CH3 + HBr Br
В субстрате преимущественной радикальной атаке подвергаются атомы водорода у третичных атомов углерода, затем у вторичных, и, в последнюю очередь у первичных. Чтобы это показать в продуктах реакции пропана с бромом надо указать 2- бромпропан, а не 1-бромпропан, хотя последний также образуется.
Предпочтительное протекание реакции по одному из нескольких возможных реакционных центров называется региоселективностью.
Т.о. реакция галогенирования алканов протекает региоселективно.
Механизм.
Стадия 1: инициирование. При облучении хлора УФ светом образуются атомы брома:
|
h |
. Br |
Br Br |
Br . + |
Стадия 2: Образование и рост цепи. Атом брома атакует молекулу пропана, с образованием бромоводорода и изопропильного радикала, изопропильный радикал
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 21 |
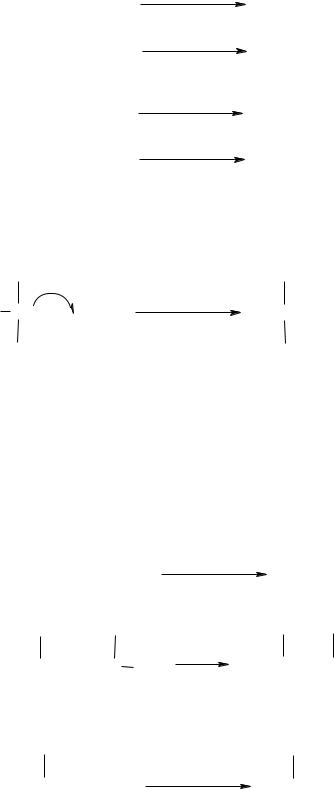
атакует молекулу хлора с образованием атакует молекулу пропана и т.д.
т.е. каждая стадия является звеном цепи.
Br . + |
|
H C |
|
CH |
|
|
|
CH |
|
||||
|
2 |
|
3 |
||||||||||
|
|
|
3 |
|
|
|
|
|
|
||||
H C |
|
CH |
|
CH |
3 |
+ Br |
|
|
Br |
||||
|
|
|
|
||||||||||
3 . |
|
|
|
|
|
|
|
|
|
|
|||
2-хлорпропана и атома брома, атом брома
HBr |
+ |
H C |
|
CH |
|
CH |
3 |
|||
|
|
|||||||||
|
|
|
|
3 |
|
. |
|
|
||
H C |
|
CH |
|
CH |
|
+ |
Br . |
|
||
|
|
|
|
|||||||
3 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Br
Br . |
+ |
|
H3C |
|
CH |
|
|
CH3 |
|||
|
2 |
|
|||||||||
H C |
|
CH |
|
CH |
3 |
+ Br |
|
|
Br |
||
|
|
|
|
||||||||
3 . |
|
|
|
|
|
|
|
|
|||
Механизм отдельной стадии:
CH3
. |
. Br |
H C . H |
CH3
пропан
HBr |
+ |
H C |
|
CH |
|
CH |
3 |
|||
|
|
|||||||||
|
|
|
|
3 |
|
. |
|
|
||
H C |
|
CH |
|
CH |
|
+ |
Br . |
|
||
|
|
|
|
|||||||
3 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Br
и т.д.
|
|
CH3 |
. |
|
|
C . |
|
H |
|
+ H . Br |
CH3
изопропильный радикал
(NB! имеем ввиду, что у атома брома на внешнем уровне 7 электронов, а не 1, но для удобства здесь мы пишем только 1)
Стадия 3: Обрыв цепи. Атомы брома или изопропильные радикалы взаимодействует друг с другом. Кроме того, изопропильный радикал может давать пропен. Цепь ―обрывается‖.
|
|
|
|
Br . + Br . |
|
|
|
Br2 |
|
|
|
|
||
|
|
CH3 |
CH3 |
|
|
CH3 |
|
CH3 |
||||||
H |
|
C . |
+ . C H |
H |
|
C |
|
C |
|
H |
||||
|
|
|
|
|||||||||||
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
CH3 |
|
|
CH3 |
CH3 |
|||||||
|
|
CH3 |
|
|
|
CH3 |
||||
H |
|
C . + Br . |
|
H |
|
C |
|
Br |
||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
CH3 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
http://norgchem.professorjournal.ru |
Нижник Я.П. |
|
|
|
|
|
Страница 22 |
|||

Аналогичным образом пишутся механизмы реакций бромирования и хлорирования других углеводородов.
Эти реакции являются реакциями радикального замещения — SR , идущими по цепному механизму.
Помним о региоселективности!
6. Приведите электронное строение этилена и бутадиена-1,3.
Этилен (этен) – самый простой алкен:
|
|
|
H |
|
|
|
H |
H |
|
|
H |
C2H4 |
H2C |
|
CH2 |
|
|
|
|
|
C |
|
C |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
H |
|
|
|
H |
H |
|
|
H |
Атомы углерода находятся в состоянии sp2-гибридизации, молекула является плоской, валентные углы близки к 120o.
Двойная связь образована одной -связью и одной -связью.
H |
H |
H |
H |
H |
H |
H |
H |
|
|
||
Атомные p-орбитали |
молекулярная -орбиталь |
||
Бутадиен-1,3 (1,3-бутадиен, бут-1,4-диен) — самый простой сопряжѐнный диен:
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
H |
|
H |
||
C4H6 |
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
C |
|
C |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
H2C |
|
CH CH |
|
CH2 |
|
|
|
|
|
|
|
|
H |
|
|
|
H |
||||
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
H |
H |
|
|
|||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
H |
|
H |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Двойные связи в бутадиене-1,3 сопряжены. Квантовая химия рассматривает сопряжение связей как взаимодействие между орбиталями отдельных фрагментов молекулы. -Сопряжение возникает тогда когда есть чередование простых и кратных (двойных или тройных) связей в структурной формуле.
Например:
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 23 |

C  C C
C C  C C
C C  C
C
C  C C
C C  C C
C C  C
C
C  C C
C C  C C
C C  C
C
При взаимодействии p-орбиталей образуются две двойные связи. Однако образующиеся орбитали сближены настолько, что могут перекрываться и взаимодействовать, образуя единую электронную систему:
H H
H H 






 H
H
H 












 H H
H H 


H H
H H
H H
H
H
H H
При этом электроны дополнительно делокализуются, что выгодно с энергетической точки зрения.
NB! Приведѐнная схема не означает, что вначале образуются связи, а только потом их электроны взаимодействуют и делокализуются.
Почему изолированные двойные связи не находятся в сопряжении?
-связи в данном случае находятся слишком далеко друг от друга, поэтому их - орбитали не перекрываются. Например, в пентадиене-1,4:
H2C CH CH2 CH
CH CH2 CH  CH2
CH2
CH2
Какие реакции по направлению и механизму характерны для алкенов?
Реакции электрофильного присоединения – AE.
Какие реагенты называются электрофильными?
Электрофильные ("любящие электроны") реагенты или электрофилы - это частицы (катионы или молекулы), имеющие свободную орбиталь на внешнем электронном уровне на которую они могут принимать электроны (практически это синоним кислот Льюиса).
Например, H+, Br+, Cl+, NO2+ (катион нитрония), карбокатионы, Br2, Cl2, SO3.
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 24 |
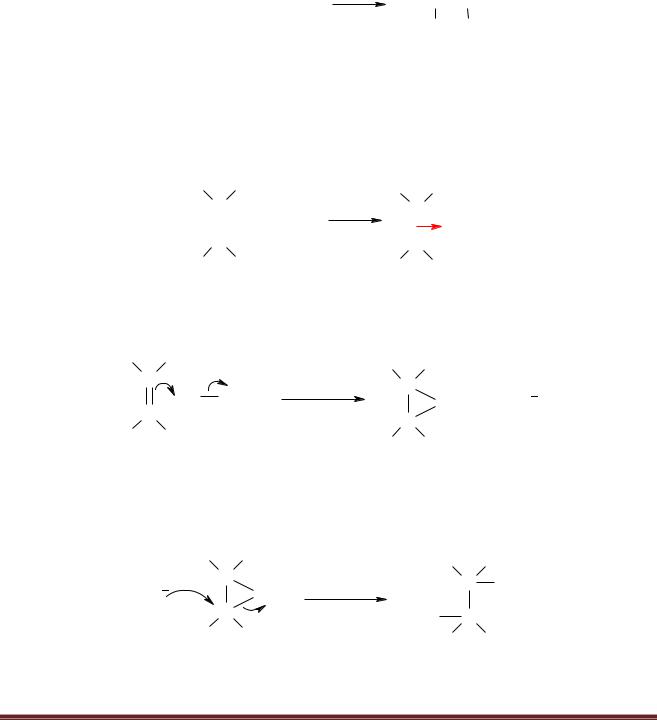
Напишите уравнения реакций электрофильного присоединения галогенов, галогеноводородов и воды к этилену. Опишите механизмы реакций присоединения.
Описанные механизмы на примере этилена имеют общий характер для всех алкенов.
Присоединение брома.
Это пример реакции электрофильного присоединения AE
H2C |
|
CH2 + Br2 |
H2C |
|
CH2 |
|
|
||||
|
|
||||
|
|
|
Br Br |
||
1,2-дибромэтан
Механизм.
1. Образование -комплекса (стрелка показывает направление смещения электронной плотности — от основания Льюиса к кислоте Льюиса):
H |
|
|
H |
H |
|
|
H |
|
C |
+ |
Br2 |
C |
|||
|
|
|
|
|
Br2 |
||
|
C |
|
|
|
|||
|
|
C |
|||||
H |
|
|
H |
H |
|
|
H |
2. Образование галогенониевого иона (в данном случае бромониевого):
H |
H |
H |
|
H |
|
|
|
|
|
|
|
||
|
C |
|
C |
|
|
|
|
|
Br Br |
+ |
|
||
|
|
|
|
|||
|
C |
|
|
Br |
+ |
Br |
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
H |
H |
H |
|
H |
|
|
|
|
|
|
|
||
3. Атака бромониевого иона бромид-ионом происходит с тыльной стороны галогенониевого иона:
H |
|
H |
H |
H |
|
|
|
||
|
C |
+ |
|
C Br |
|
|
|
||
Br |
|
Br |
|
|
C |
|
|
|
|
|
|
Br |
C |
|
|
|
|
||
H |
|
H |
H |
H |
|
|
|
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 25 |

Надо обратить внимание, что атомы галогена в итоге присоединяются с двух сторон двойной связи. Т.е. в данном случае наблюдается транс-присоединение.
Например, если проводить реакцию с циклогексеном, то будет получаться транс-1,2- дибромциклогексан:
Br2
Br H
H |
H |
H |
Br |
|
Напишите уравнения реакций электрофильного присоединения галогеноводородов к этилену. Опишите механизм реакции.
H2C |
|
|
CH2 + HBr |
H2C |
|
CH3 |
|
|
|
||||
|
|
|
||||
|
|
|
|
Br |
||
Этилен |
бромоводород |
бромэтан |
||||
Это пример реакции электрофильного присоединения AE
Механизм.
1.Присоединение протона с образованием -комплекса.
2.Превращение -комплекса в карбокатион.
3.Присоединение бромид-иона к карбокатиону.
|
|
|
|
H+ |
|
|
|
|
|
|
|
Br |
||
|
|
|
H+ |
+ |
Br |
|
|
|
||||||
H2C |
|
CH2 |
H2C |
|
CH2 |
H3C |
|
CH2 |
|
|
H3C |
|
CH2 |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|||||||||
Напишите уравнения реакций электрофильного присоединения воды к этилену. Опишите механизм реакции.
|
|
|
H+ |
||
H2C |
|
CH2 + H2O |
H2C |
|
CH3 |
|
|
||||
|
|
|
OH |
||
Это пример реакции электрофильного присоединения AE
Механизм.
1. Присоединение протона с образованием -комплекса.
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 26 |

2. Образование карбокатиона 3. Присоединение воды к карбокатиону с образованием протонированного спирта.
4. Отщепление протона (регенерируется катализатор — протон).
|
|
|
+ |
.. |
H |
H + H |
|
|
|
|
|||||||
|
|
|
|
H |
|
|
.O |
|
|
|
O |
|
|
OH |
|||
|
|
|
H+ |
. |
H |
|
|
|
|
||||||||
|
|
|
+ |
|
|
|
|
|
|
|
|
||||||
|
|
|
H3C |
|
CH2 |
H3C |
|
CH2 |
|||||||||
H2C |
|
CH2 |
H2C |
|
CH2 |
H3C |
|
CH2 |
|
|
|
||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H+ |
|||
Напишите уравнения реакций электрофильного присоединения галогенов, галогеноводородов и воды к бутену-2. Опишите механизмы реакций присоединения.
Как и в случае этилена — см. выше.
Напишите уравнения реакций электрофильного присоединения галогенов, галогеноводородов и воды к пропилену. Опишите механизмы реакций присоединения.
Присоединение брома к пропилену.
CH |
|
HC |
|
CH2 + |
Br2 |
CH |
|
|
CH |
|
|
|
CH2 |
|
|||||||||||||
3 |
|
3 |
|
||||||||||
|
|||||||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
Br Br |
|||||
пропен |
бром |
1,2-дибромэтан |
|||||||||||
Это реакция является примером электрофильного присоединения AE
Механизм.
1. Образование -комплекса
H |
|
|
CH3 |
H |
|
|
CH3 |
|
C |
+ |
Br2 |
C |
|||
|
|
|
|
|
Br2 |
||
|
C |
|
|
|
|||
|
|
C |
|||||
H |
|
|
H |
H |
|
|
H |
2. Образование галогенониевого иона (в данном случае бромониевого):
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 27 |

H |
CH3 |
H |
|
CH3 |
|
|
|
C |
|
|
|
||
|
|
C |
|
|
|
|
|
Br Br |
|
+ |
|
||
|
|
|
|
|||
|
C |
|
|
Br |
+ |
Br |
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
H |
H |
H |
|
H |
|
|
|
|
|
|
|
||
3. Атака бромониевого иона бромид-ионом с тыльной стороны.
H |
|
CH3 |
H |
CH |
3 |
|
C |
|
|
|
|
|
+ |
|
C Br |
||
|
|
|
|||
Br |
|
Br |
|
|
|
C |
|
|
|
|
|
|
|
Br |
C |
|
|
|
|
|
|
||
H |
|
H |
H |
H |
|
|
|
|
|
||
Присоединение бромоводорода к пропилену.
Это реакция электрофильного присоединения AE. Реакция идѐт по правилу Марковникова.
Правило Марковникова. При присоединении HX к кратным связям, водород присоединяется к наиболее гидрогенизированному атому углерода.
CH |
|
HC |
|
CH2 + HBr |
CH |
|
|
CH |
|
CH3 |
|
|
3 |
|
|||||||
3 |
|
|||||||||
|
|
|
||||||||
|
|
|
|
|
|
|
Br |
|||
пропен |
|
бромоводород |
2-бромпропан |
|||||||
NB! 1-бромпропан (продукт образующийся против правила Марковникова) тоже образуется, но в меньших количествах. В присутствии перекисей реакция идѐт против правила Марковникова и по радикальному механизму (эффект Хараша).
Механизм.
1. Присоединение протона с образованием -комплекса.
2. Присоединение протона с образованием карбокатиона
3. Присоединение бромид-иона к карбокатиону.
|
|
|
|
H+ |
+ |
|
Br |
|
|
|
Br |
|||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
H3C |
|
CH |
|
CH3 |
||||||
H3C |
|
CH |
|
CH2 |
H3C |
|
CH |
|
CH3 |
|
|
|
||||
|
|
|
|
|
|
|
||||||||||
|
||||||||||||||||
Присоединение воды к пропилену в присутствии кислотного катализатора.
Реакция является реакцией AE и идѐт по правилу Марковникова.
CH |
|
HC |
|
CH2 |
+ H2O |
H+ |
CH |
|
|
CH |
|
CH3 |
|
|
|
3 |
|
|
|||||||
3 |
|
|
||||||||||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
http://norgchem.professorjournal.ru |
Нижник Я.П. |
|
|
|
|
|
Страница 28 |
|||||

Механизм.
2. Образование карбокатиона 3. Присоединение воды к карбокатиону с образованием протонированного спирта.
4. Отщепление протона (регенерируется катализатор — протон).
|
|
|
|
H+ |
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
H2O |
|||||||||
H3C |
|
CH |
|
CH2 |
|
H3C |
|
CH |
|
CH2 |
|
|
|
H3C |
|
CH |
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
H |
+ |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
H3C |
|
CH |
|
CH3 |
-H+ |
H3C |
|
CH |
|
CH3 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Напишите уравнения реакций электрофильного присоединения галогенов, галогеноводородов и воды к бутадиену-1,3. Опишите механизмы реакций присоединения.
Бутадиен-1,3 является сопряжѐнной системой. В этом случае возможно два вида присоединения – прямое присоединение (1,2) и сопряжѐнное (1,4):
H2C |
|
|
CH |
|
CH |
|
CH2 |
1,2-product |
|
|
|
||||||
|
|
|||||||
|
|
|
||||||
|
|
|
|
|||||
|
|
|
|
|||||
Br |
Br |
|
||||||
H2C CH CH  CH2 Br2
CH2 Br2
H2C |
|
CH |
|
CH |
|
CH2 |
1,4-product |
|
|
||||||
|
|
||||||
|
|
|
|||||
Br |
|
|
|
|
Br |
|
|
Присоединение галогеноводородов и воды идѐт аналогично:
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 29 |

H3C |
|
|
CH |
|
CH |
|
CH2 |
1,2-product |
|
|
|
||||||
|
|
|||||||
|
|
|
||||||
|
|
|
|
|||||
|
|
|
|
|
||||
|
|
Br |
|
|||||
HBr
H2C  CH CH
CH CH  CH2
CH2
H3C |
|
CH |
|
CH |
|
CH2 |
1,4-product |
|
|
||||||
|
|
||||||
|
|
|
|||||
|
|
|
|
|
|
Br |
|
Механизмы 1,2-присоединения аналогичны механизму присоединения в случае алкенов.
Как происходит 1,4-присоединение?
H2C |
|
|
|
CH |
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
||||
H3C |
|
|
|
CH |
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
H3C |
|
|
CH |
|
|
CH |
|
|
CH2 |
Мезомерный |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
карбокатион |
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
H3C |
|
|
|
|
CH |
|
|
CH |
|
|
|
CH2 |
H3C |
|
|
CH |
|
|
CH |
|
|
|
CH2 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|||||
NB! Обоюдоострая стрелка не означает, что один карбокатион переходит в другой. Она означает, что это две предельные структуры, описывающие реальный карбокатион при наложении (суперпозиции) одной на другую.
Объясните правило Марковникова.
Правило Марковникова. При присоединении HX к кратным связям, водород присоединяется к наиболее гидрогенизированному атому углерода.
В начале происходит присоединение протона к алкену c образованием карбокатиона. При этом главным образом образуется наиболее стабильный карбокатион (обладающий наименьшей энергией) — с наибольшим числом алкильных заместителей.
Почему алкильные заместители стабилизируют карбокатион? За счѐт +I
эффекта алкильных групп происходит делокализация положительного заряда и уменьшение энергии, и, соответственно, увеличение стабильности.
http://norgchem.professorjournal.ru |
Нижник Я.П. |
Страница 30 |
