
- •Лабораторный практикум по физической химии
- •Составители: в.А.Хомич, с.А.Эмралиева
- •Введение
- •Электрохимии - лабораторные работы
- •Лабораторная работа №1 Определение интегральной теплоты растворения соли
- •Работа с термометром Бекмана.
- •Порядок выполнения лабораторной работы.
- •Определение термодинамических характеристик процесса гидролиза соли.
- •Порядок выполнения лабораторной работы.
- •Степень и константа гидролиза растворов соли
- •Термодинамические характеристики процесса гидролиза
- •Порядок проведения измерения рН на иономере и-130
- •Лабораторная работа №3 Определение термодинамического равновесия в гомогенной системе
- •Порядок выполнения лабораторной работы.
- •Порядок расчета константы равновесия реакции
- •, Моль/дм3
- •, Моль/ дм3
- •Порядок расчета константы равновесия реакции омыления эфира водой:
- •Результаты титрования
- •Расчет константы равновесия обратимой реакции
- •Лабораторная работа №4 Изучение равновесия в двухкомпонентной системе «жидкость-пар».
- •Порядок выполнения лабораторной работы.
- •Экспериментальные данные для построения кривой зависимости «температура кипения – состав»
- •Порядок измерения показателя преломления на рефрактометре ирф-45462м.
- •Порядок измерения показателя преломления на рефрактометре портативном “Карат-мт”
- •Лабораторная работа №5 Термический анализ
- •Состав, %
- •Порядок выполнения лабораторной работы.
- •Данные для построения кривых охлаждения
- •Результаты термического анализа
- •Лабораторная работа №6 Измерение электропроводности слабого электролита
- •Последовательность выполнения лабораторной работы
- •Характеристики процесса диссоциации слабого электролита
- •Лабораторная работа №8 Изучение скорости инверсии сахара
- •Принцип работы поляриметра см-3.
- •Порядок выполнения лабораторной работы.
- •Результаты измерения скорости инверсии сахара
- •Библиографический список
- •Содержание
Лабораторная работа №5 Термический анализ
Цель работы: построить диаграмму плавкости смеси веществ нафталина и диазобензола; определить состав эвтектической смеси.
Термический анализ изучает зависимость температуры кристаллизации или плавления исследуемой системы от ее состава. Результаты термического анализа оформляются в виде диаграммы плавкости в координатах «температура – состав», которая отражает фазовые превращения в гетерогенных системах. Анализ диаграмм плавкости позволяет определить число и химическую природу фаз, границы их существования, характер взаимодействия компонентов, устойчивость образующихся веществ.
Для построения диаграмм плавкости используют кривые охлаждения, рис. 4а. Кривые охлаждения строятся в координатах «температура – время». Если в системе не происходит никаких фазовых превращений, температура при охлаждении падает равномерно. Появление кристаллов в расплаве и переход одной кристаллической модификации в другую сопровождается выделением тепла, и падение температуры замедляется. Таким образом, всякий излом на кривой охлаждения соответствует появлению новой фазы
Т,ºС а) б) Т,ºС
Время,
мин. ТºА ТºВ С Д Е кристаллы
А и В расплав А (100%) В (100%)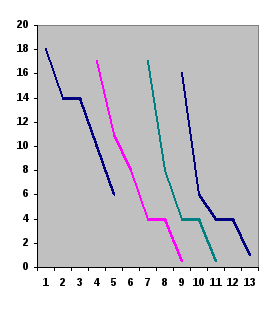
Состав, %



 Схема
построения диаграммы плавкости показана
на рис. 4. Строят кривые охлаждения для
чистых веществ и их смесей. Обычно берут
6…8 смесей различных концентраций.
Значения температур соответствующих
Схема
построения диаграммы плавкости показана
на рис. 4. Строят кривые охлаждения для
чистых веществ и их смесей. Обычно берут
6…8 смесей различных концентраций.
Значения температур соответствующих
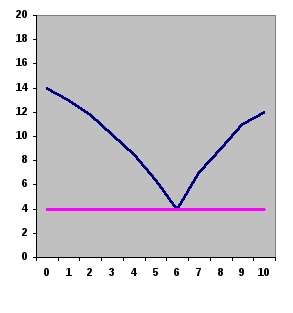
Рис. 4. Схема построения диаграммы плавкости: а – кривые охлаждения; б – диаграмма плавкости; Т0А и Т0В – температура плавления чистых компонентов А и В; ТАЕТВ – линия ликвидуса; СЕД линия солидуса; Е – эвтектическая точка.
появлению новых фаз (горизонтальные плато) переносят с кривых охлаждения на диаграмму плавкости (диаграмму состояния системы) в координатах «температура-состав», рис 4б.
Смесь, которая кристаллизуется без изменения состава называется эвтектикой. Линия солидуса СЕД соответствует температуре кристаллизации эвтектики. В эвтектической точке Е сосуществует три фазы: расплав и кристаллы чистых компонентов А и В. Количество сосуществующих кристаллических фаз А и В в точке Е определяется по правилу рычага:
![]()
Порядок выполнения лабораторной работы.
В пронумерованные пробирки поместить чистые вещества и их смеси различного состава, табл.6. Пробирки закрывают пробками с термометрами таким образом, чтобы ртутный шарик был помещен в вещество. Пробирки опускают в водяную баню и нагревают до полного расплавления в них вещества.
Пробирки вынуть из бани, обтереть досуха и поместить в воздушную рубашку (узкогорлую колбу с фильтровальной бумагой на дне) для их равномерного охлаждения.
Вести наблюдения за охлаждением системы, записывая температуру расплава в пробирке через каждые 30 сек., табл.6. Время отсчитывать по секундомеру. Кристаллизация чистых веществ или эвтектической смеси -
сопровождается продолжительной температурной остановкой. После того, как все вещество или эвтектическая смесь закристаллизуется, происходит дальнейшее понижение температуры. Наблюдение за охлаждением системы продолжать еще 5 минут.
Таблица 6
