
- •Лабораторный практикум по физической химии
- •Составители: в.А.Хомич, с.А.Эмралиева
- •Введение
- •Электрохимии - лабораторные работы
- •Лабораторная работа №1 Определение интегральной теплоты растворения соли
- •Работа с термометром Бекмана.
- •Порядок выполнения лабораторной работы.
- •Определение термодинамических характеристик процесса гидролиза соли.
- •Порядок выполнения лабораторной работы.
- •Степень и константа гидролиза растворов соли
- •Термодинамические характеристики процесса гидролиза
- •Порядок проведения измерения рН на иономере и-130
- •Лабораторная работа №3 Определение термодинамического равновесия в гомогенной системе
- •Порядок выполнения лабораторной работы.
- •Порядок расчета константы равновесия реакции
- •, Моль/дм3
- •, Моль/ дм3
- •Порядок расчета константы равновесия реакции омыления эфира водой:
- •Результаты титрования
- •Расчет константы равновесия обратимой реакции
- •Лабораторная работа №4 Изучение равновесия в двухкомпонентной системе «жидкость-пар».
- •Порядок выполнения лабораторной работы.
- •Экспериментальные данные для построения кривой зависимости «температура кипения – состав»
- •Порядок измерения показателя преломления на рефрактометре ирф-45462м.
- •Порядок измерения показателя преломления на рефрактометре портативном “Карат-мт”
- •Лабораторная работа №5 Термический анализ
- •Состав, %
- •Порядок выполнения лабораторной работы.
- •Данные для построения кривых охлаждения
- •Результаты термического анализа
- •Лабораторная работа №6 Измерение электропроводности слабого электролита
- •Последовательность выполнения лабораторной работы
- •Характеристики процесса диссоциации слабого электролита
- •Лабораторная работа №8 Изучение скорости инверсии сахара
- •Принцип работы поляриметра см-3.
- •Порядок выполнения лабораторной работы.
- •Результаты измерения скорости инверсии сахара
- •Библиографический список
- •Содержание
Лабораторная работа №4 Изучение равновесия в двухкомпонентной системе «жидкость-пар».
Цель работы: изучить равновесие в двухкомпонентной системе «жидкость-пар», построить диаграмму состояния «состав раствора – температура кипения».
Диаграмма равновесия двухкомпонентной системы «жидкость – пар» в координатах «температура – состав» при постоянном давлении должна иметь следующий вид, рис. 2.
Т Т0В Т0А
А (100%) В (100%)
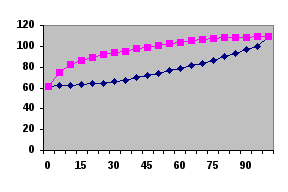

Рис. 2. Диаграмма равновесного состояния двухкомпонентной смеси «жидкость-пар».
Точки Т0А и Т0В – температуры кипения соответствующих чистых компонентов А и В. Верхнее поле на диаграмме отвечает пару, нижнее – жидкости. Нижняя кривая характеризует зависимость температуры кипения раствора от его состава (концентрации). Верхняя кривая показывает состав пара, находящегося в равновесии с жидкостью при температуре его кипения. Между этими кривыми находится область гетерогенного равновесия «жидкость – пар».
Порядок выполнения лабораторной работы.
Приготовить десять растворов смеси двух органических жидкостей толуола C6H5CH3 и хлороформа CHCl3 следующего состава:
1) Толуол 100% - 50см3
2) Толуол 95% - 47,5см3 + 2,5см3 хлороформа.
3) Толуол 90% - 45,0см3 + 5,0см3 хлороформа.
4) Толуол 85% - 42,5см3 + 7,5см3 хлороформа.
5) Толуол 80% - 40,5см3 + 9,5см3 хлороформа.
6) Толуол 70% - 35,0см3 + 15,0см3 хлороформа.
7) Толуол 60% - 30,0см3 + 20,0см3 хлороформа.
8) Толуол 45% - 22,5см3 + 27,5см3 хлороформа.
9) Толуол 30% - 15,0см3 + 35,0см3 хлороформа.
10) Толуол 0% - 50,0см3 хлороформа 100%.
Смеси готовят в сухих конических колбах с притертыми пробками.
Измерить показатели преломления чистых жидкостей и растворов известного состава с помощью рефрактометра.
Построить кривую зависимости показателя преломления от состава раствора. Калибровочную кривую использовать для определения состава раствора неизвестной концентрации по его показателю преломления.
Определить температуру кипения чистых компонентов и их смесей с помощью прибора изображенного на рис.3. для этого в колбу 1 налить 40см3 жидкости и поместить фарфоровые кусочки (кипелки). Кипелки способствуют равномерному кипению жидкости и предотвращают ее перегрев.
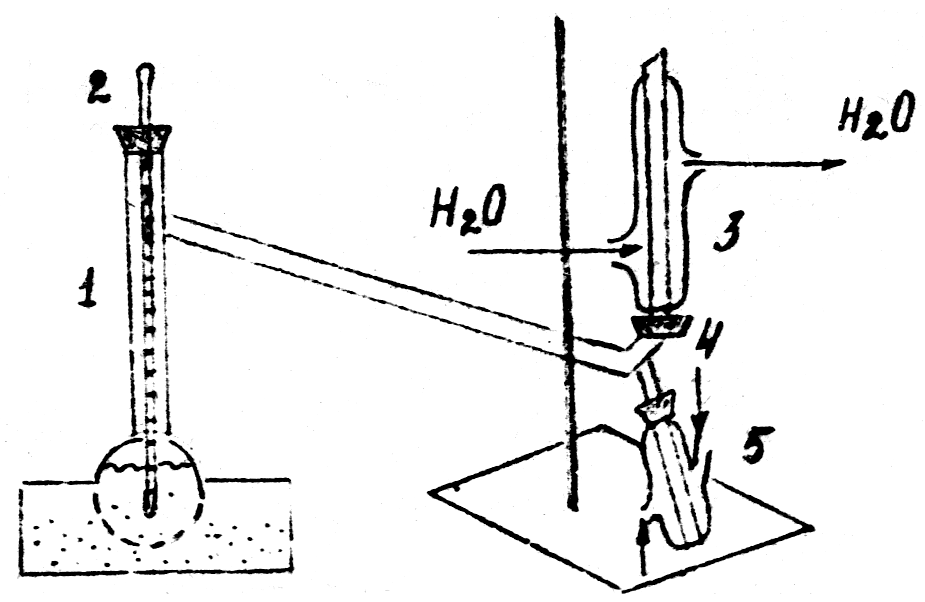
Рис.3. Установка для определения температуры кипения органических жидкостей:
1 – колба с жидкостью, помещенная в водяную баню; 2 – термометр; 3 – водяной холодильник в положении для конденсации пара; 4 – холодильник в положении для отбора конденсата.
Колбу закрыть пробкой с термометром таким образом, чтобы шарик термометра был погружен в жидкость. Колбу соединить с холодильником, пустить в него воду и медленно нагревать колбу.
После того, как температура жидкости перестанет изменяться записать температуру кипения. Затем холодильник повернуть в положение для отбора конденсата, т.е. открытым концом вниз. В заранее приготовленную сухую пробирку отобрать 5…10 капель конденсата; пробирку закрыть пробкой. Холодильник вновь установить в вертикальное положение; продолжить кипячение 2…3 минуты и вновь записать температуру кипения. При этом температура не должна отличаться от температуры до отбора пробы более чем на 1 градус. Нагревание прекратить, сосуд охладить и содержимое его вылить в склянку для слива.
Аналогичные измерения температуры кипения жидкостей провести со всеми 10 смесями. Перед каждым опытом кипелки заливают новым раствором, им же споласкивают колбу.
Измерить показатель преломления конденсата, собранный в пробирке. По измеренным показателям преломления конденсата, пользуясь калибровочной кривой определить состав пара жидкости, температуру кипения которой определяли.
Полученные экспериментальные данные записать в табл.5:
Таблица 5
