
- •А.А. Капустина методика преподавания химии курс лекций
- •Лекция № 1
- •Предмет методики обучения химии и ее задачи
- •Принципы обучения
- •Истоки и основные этапы развития методики обучения химии в России
- •Советский период методики преподавания химии
- •Лекция № 2 Принцип построения типовых школьных программ и их общая характеристика
- •Государственный образовательный стандарт по химии
- •I раздел. Цели и задачи химии:
- •Лекция № 3 Методическая работа учителя
- •План-конспект урока
- •Методы обучения химии
- •Словесные методы
- •Лекция № 4 Методы наглядного обучения. О средствах наглядности
- •Демонстрация химических опытов
- •Практические методы обучения
- •Лекция № 5 Правила техники безопасности при работе в школьном кабинете
- •Общие положения
- •Требования к помещениям кабинета (лаборатории) химии
- •Требования безопасности при размещении и хранении химических реактивов
- •Утилизация реактивов и растворов
- •Решение расчетных химических задач
- •Решение типовых задач в 8 классе
- •Лекция № 6 Решение типовых задач в 8 классе (продолжение)
- •Решение расчетных задач в 9 классе
- •Решение расчетных задач в 10 классе
- •Решение расчетных задач в 11 классе
Решение расчетных задач в 11 классе
В 11 классе новыми являются задачи на химическую кинетику.
Задача 1: Вычислите среднюю скорость реакции
A + B = 2C,
1 моль 1 моль
если концентрация вещества A была 0.22 моль/л, а через 10 секунд стала 0.215 моль/л. Как изменилась за это время концентрация вещества B?
|
Дано: |
|
|
C1 = 0.22 моль/л |
|
|
C2 = 0.215 моль/л |
|
|
t = 10 сек. |
|
|
= ? CB = ? |
|
Решение:
![]()
![]()
CB = CA = 0.005 моль/л.
Задача 2: Во сколько раз увеличится скорость реакции при повышении температуры от 150С до 200С, если = 3?
|
Дано: |
|
|
t1 = 150C |
|
|
t2 = 200C |
|
|
= 3 |
|
|
|
|
Решение:
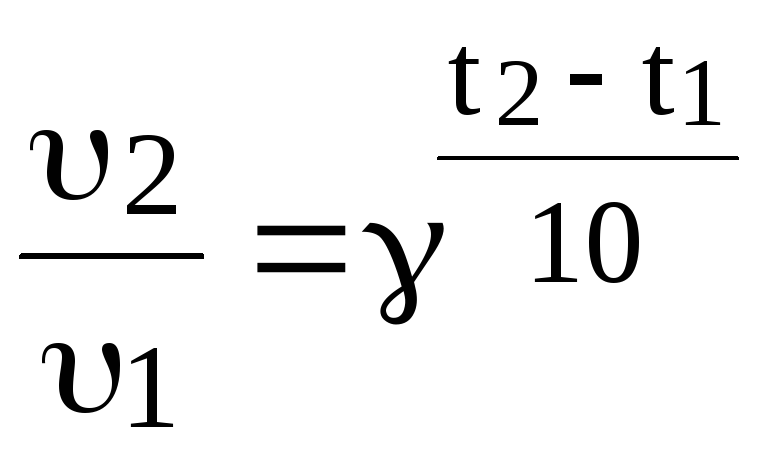
![]() .
.
Ответ: В 243 раза.
Задача 3: В момент равновесия обратимой реакции
2SO2 + O2 2SO3
[SO2] = 0.002 моль/л; [O2] = 0.004 моль/л; [SO3] = 0.003 моль/л. Вычислите исходные концентрации кислорода и оксида серы.
Решение:
Согласно уравнению реакции, в нее вступают 2 моль SO2, 1 моль O2 и получается 2 моль SO3:
2SO2 + O2 2SO3.
2 моль 1 моль 2 моль
Обозначим количество реально вступающих и получающихся веществ через .
Первоначально объясним учащимся:
![]() ,
если принять V = 1 л,
то C = .
,
если принять V = 1 л,
то C = .
Затем составим таблицу по уравнению:
2SO2 + O2 2SO3.
2 моль 1 моль 2 моль
исх. 0.005 0.0055 0.0
0.003 0.0015 0.003
равн. 0.002 0.004 0.003.
Исходные концентрации SO2 и O2 находим, суммируя и равн. Так как по уравнению реакции из 2 моль SO2 получается 2 моль SO3, то:
(SO2) = равн.(SO3) = (SO3).
На образование 2 моль SO3 по уравнению реакции расходуется 1 моль кислорода, следовательно:
(O2) = 1/2 равн.(SO3).
Задача 4: Во сколько раз возрастет скорость реакции взаимодействия азота с водородом N2 + 3H2 2NH3, если увеличить концентрацию водорода в 2 раза?
Решение:
= K·[N2]·[H2]3
Пусть [H2]1 = x, тогда [H2]2 = 2x
1 = K·[N2]·x3 2 = K·[N2]·(2x)3
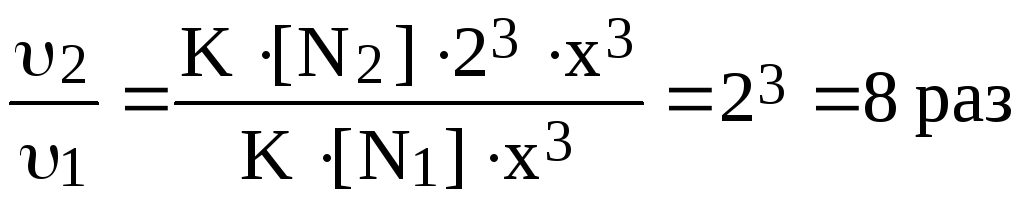 .
.
