
Лекция 21
.docЛекция 21.
СВОБОДНЫЕ РАДИКАЛЫ
I. СТРОЕНИЕ И УСТОЙЧИВОСТЬ
Свободный радикал (СР) – это частица, содержащая один или несколько неспаренных электронов.
Такое определение включает некоторые неорганические молекулы, например, NO, NO2, а также многие индивидуальные атомы, например, Na, Cl.
Радикалы (Р) обладают магнитным моментом и являются парамагнитными частицами. Детектируются обычно методом электронного спинного резонанса (ЭСР), который называют также методом электронного парамагнитного резонанса (ЭПР). В принципе этот метод аналогичен методу ЯМР.
Удается получить спектры Р со временем жизни меньше одной секунды. Если концентрация Р слишком мала, то применяют метод спиновой ловушки, заключающийся в добавлении такого соединения, которое, взаимодействуя с очень реакционноспособными Р, образует более стабильные Р, регистрируемые с помощью ЭПР:

СР могут быть детектированы с помощью обычного спектрометра ЯМР, используя явление химической индукции динамической поляризации ядер (ХИДПЯ).
Порядок устойчивости СР такой же, как и в случае карбокатионов:
третичные > вторичные > первичные.
Как и в случае КК, этот ряд объясняется гиперконьюгацией:

Бензильные и аллильные радикалы, благодаря резонансу, устойчивее простых, но и они существуют только как промежуточные частицы:
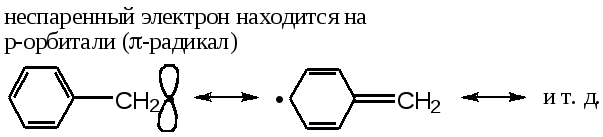
Однако такие Р, как трифенилметильный радикал, сохраняются в растворе при комнатной температуре, правда, в равновесии с димерной формой:

В случае Р трифенилметильного типа главной причиной устойчивости является не резонансная стабилизация, а стерические затруднения димеризации.
Радикал Ph3C• не является плоским, а имеет форму пропеллера (см. лекцию 18, трифенилметильный катион).
Еще более устойчивы полностью хлорированные трифенилметильные радикалы, по-видимому, по стерическим причинам. Они инертны в растворах и в твердом состоянии.
Известны очень устойчивые Р, в которых неспаренный электрон находится на гетероатоме:

Мерой относительной устойчивости СР служит энергия диссоциации (D) связи R−H: чем выше величина D, тем менее устойчив радикал.
|
Радикал |
Ph• |
Me• |
Et• |
CCl3• |
Me2CH• |
Me3C• |
CH2=CH−CH2• |
PhCH2• |
|
D, ккал/моль |
110 |
104 |
98 |
96 |
95 |
92 |
89 |
85 |
Для простых алкильных радикалов возможны два типа структур:

Химические данные и физические эксперименты (ЭПР, УФ-, ИК-спектры) свидетельствуют в пользу плоской или почти плоской структуры, однако разность энергий плоских и пирамидальных радикалов невелика.
СР типа CF3• предпочитают низкую пирамидальную форму, с очень малым барьером инверсии; чем выше электроотрицательность соседнего с радикальным центром атома, тем больше отклонение от планарности.
Резонансно стабилизированные свободные радикалы имеют плоскую форму, хотя, как у же было отмечено выше, радикалы трифенилметильного типа Ar3C•, подобно соответствующим карбокатионам, имеют форму пропеллера.
II. СПОСОБЫ ПОЛУЧЕНИЯ СВОБОДНЫХ РАДИКАЛОВ
1) ИЗ МОЛЕКУЛ В РЕЗУЛЬТАТЕ ГОМОЛИТИЧЕСКОГО РАЗРЫВА СВЯЗИ
В зависимости от источника энергии различают два типа гомолитического разрыва связи.
1. Термическое расщепление (пиролиз)
При достаточно высоких температурах в газовой фазе любая органическая молекула дает СР. При энергии связи 20 ÷ 40 ккал/моль расщепление молекулы можно вызвать и в жидкой фазе:


2. Фотохимическое расщепление (фотолиз)
Энергия света с длиной волны от 600 до 300 нм составляет 48 ÷ 96 ккал/моль, что совпадает с диапазоном энергии ковалентных связей:
![]()
(ii) Декарбонилирование кетонов:

(iii) Декарбонилирование альдегидов:

2) ИЗ ДРУГИХ СВОБОДНЫХ РАДИКАЛОВ
1. При реакции между радикалом и молекулой:
![]()

2. При разложении (расщеплении) радикалов:
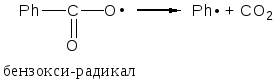
См. также 1)-2-(ii), 1)-2-(iii).
3. При перегруппировке радикалов:

3) ПРИ ОКИСЛЕНИИ ИЛИ ВОССТАНОВЛЕНИИ, В ТОМ ЧИСЛЕ – ЭЛЕКТРОЛИТИЧЕСКОМ:
![]()


![]()
(v) Синтез углеводородов по Кольбе (электролиз):


III. РЕАКЦИИ СВОБОДНЫХ РАДИКАЛОВ
Если радикалы термодинамически стабильны, и стерические факторы не препятствуют их димеризации, то они находятся в равновесии с продуктами димеризации:
![]()
Если радикалы термодинамически нестабильны, то они возникают только как интермедиаты и сразу же вступают в химические реакции.
1) РЕАКЦИИ ОБРЫВА ЦЕПИ
В этих реакциях образуются устойчивые продукты нерадикального типа.
1. Комбинация одинаковых или разных радикалов:
![]()
![]()

Молекула кислорода в основном состоянии (триплетом) напоминает бирадикал (спины электронов параллельны).
2. Диспропорционирование
![]()
2) РЕАКЦИИ РОСТА ЦЕПИ
В этих реакциях образуются другие реакционноспособные радикалы, вступающие в дальнейшую реакцию.
Известно 4 главных типа реакции роста цепи, из которых наиболее распространены первые два.
1. Отрыв радикалом атома или группы от молекулы, обычно – атома водорода:
![]()
Если R'• и R'−H имеются в значительном избытке по сравнению с R•, то возникает цепная реакция.
Пример – реакция галогенирования углеводородов:
Инициирование:
![]()
Рост цепи:

Обрыв цепи:

2. Присоединение радикала к кратной связи:


и т. д. – свободнорадикальная полимеризация этиленовых соединений.
3. Разложение радикалов:


4. Перегруппировки:

1,2-Свободнорадикальные перегруппировки встречаются реже, чем перегруппировки КК. Они не наблюдаются в случае R= Alk, H и характерны лишь для следующих R:

Обычно направлены в сторону наиболее устойчивого радикала.
Пример:

Механизмы перегруппировок СР:



3) ОКИСЛЕНИЕ ДО КАРБОКАТИОНОВ И ВОССТАНОВЛЕНИЕ ДО КАРБАНИОНОВ
Происходит путем прямого переноса электрона.
IV. ИОН-РАДИКАЛЫ
Обычно неспаренный электрон и/или заряд находятся на атомах, отличных от углерода:

Лишь очень редко и заряд, и неспаренный электрон находятся на атомах углерода:

Реакции восстановления щелочными металлами часто проходят через промежуточное образование анион-радикалов. Примером является восстановление ароматических соединений по Берчу (по результату – это 1,4-дигидроприсоединение):


Анион-радикалы образуются как промежуточные частицы при протекании ароматического нуклеофильного замещения по механизму SRN1. Иногда такому же механизму следует алифатическое нуклеофильное замещение.
Примером катион-радикала является катион-радикал красителя (Кр), возникающий при его окислении кислородом воздуха на свету:

![]()

Образование Н2О2 является сопутствующим явлением, а не причиной фотообесцвечивания:

