
- •1 Основные положения молекулярно-кинетической теории газа. Понятие о идеальном и реальном газе.
- •2 Параметры и функции состояния. Уравнение состояния идеального газа.
- •3 Смеси газов. Кажущаяся молекулярная масса. Газовая постоянная смеси газов.
- •4 Первый закон термодинамики.
- •5 Энтальпия газа.
- •6 Теплоемкость газа. Удельные теплоемкости газа. Средние и истинные теплоемкости.
- •7 Теплоемкость газа в изохорном и изобарном процессах. Уравнение Майера.
- •8 Изохорный процесс. Вывод уравнения, график в координатах p-V и t-s. Изменение внутренней энергии, теплоты и работы в процессе.
- •9 Изобарный процесс. Вывод уравнения, график в координатах p-V и t-s. Изменение внутренней энергии, теплоты и работы в процессе.
- •10 Изотермический процесс. Вывод уравнения, график в координатах p-V и t-s. Изменение внутренней энергии, теплоты и работы в процессе.
- •11 Адиабатный процесс. Вывод уравнения, график в координатах p-V и t-s. Изменение внутренней энергии, теплоты и работы в процессе.
- •12 Политропный процесс. Вывод уравнения. Изменение теплоты и работы в процессе,
- •13 Политропный процесс. Обощающий характер процесса
- •14 Тепловая диаграмма в координатах p-V
- •15 Второй закон термодинамики.
- •16 Прямой цикл Карно.
- •17 Энтропия газа.
- •18 Циклы холодильных установок.
- •19 Обратный цикл Карно.
- •20 Реальные газы. Уравнение Ван-дер-Ваальса. Изотерма Ван-дер-Ваальса.
- •21 Диаграмма h-s водяного пара. Определение параметров состояния.
- •22 Диаграмма h-s водяного пара. Расчет изменений внутренней энергии, работы и теплоты в паровых процессах.
- •23 Способы передачи теплоты. Суть каждого.
- •24 Понятие о стационарном и нестационарном теплообмене, тепловом потоке, плотности теплового потока.
- •25 Закон Фурье.
- •26 Теплопроводность через плоскую стенку.
- •27 Теплопроводность через цилиндрическую стенку.
- •28 Теплопроводность через многослойную плоскую стенку.
- •29 Теплопроводность через многослойную цилиндрическую стенку.
- •30 Коэффициент теплопроводности. Методика экспериментального определения.
- •31 Теплоотдача. Факторы влияющие на интесивность теплоотдачи. Уравнение Ньютона.
- •32 Критерии подобия: Nu, Re, Ре, Pr, Gr.
- •34 Коэффициент теплоотдачи. Методика экспериментального определения.
- •35 Лучистый теплообмен. Тепловые лучи, их свойства. Способность тел поглощать, и отражать тепловые лучи.
- •36 Закон Планка
- •37 Закон Стефана-Больцмана.
- •38 Методика экспериментального определения коэффициента излучения.
- •39 Лучистый теплообмен между двумя параллельными поверхностями.
- •40 Ослабление излучения экранами.
- •41 Составной теплообмен. Учет лучистого теплообмена при расчете теплоотдачи.
- •42 Теплопередача между средами разделенными плоской стенкой.
- •43 Теплопередача между средами разделенными цилиндрической стенкой.
1 Основные положения молекулярно-кинетической теории газа. Понятие о идеальном и реальном газе.
Основные положения МКТ:
1. Все вещества состоят из мельчайших частиц: молекул, атомов или ионов.
2. Эти частицы находятся в непрерывном хаотическом движении, скорость которого определяет температуру вещества.
3. Между частицами существуют силы притяжения и отталкивания, характер которых зависит от расстояния между ними.
Идеальный газ - это газ, взаимодействие между молекулами которого пренебрежимо мало.
Основные отличия идеального газа от реального: частицы идеального газа - шарики очень малых размеров, практически материальные точки; между частицами отсутствуют силы межмолекулярного взаимодействия; соударения частиц абсолютно упругие. Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона — Менделеева. Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объем. Состояние реального газа часто на практике описывается обобщенным уравнением Менделеева — Клапейрона.
2 Параметры и функции состояния. Уравнение состояния идеального газа.
Параметры:
Давление обусловлено взаимодействием молекул рабочего тела с поверхностью и численно равно силе, действующей на единицу площади поверхности тела по нормали к последней.
Температурой называется физическая величина, характеризующая степень нагретости тела. С точки зрения молекулярно-кинетических представлений температура есть мера интенсивности теплового движения молекул.
Удельный
объем v — это объем единицы массы
вещества. Если однородное тело массой
М занимает объем v, то по определению v=
V/М. В системе СИ единица удельного объема
1 м3/кг. Между удельным объемом вещества
и его плотность существует очевидное
соотношение:
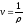
Если все термодинамические параметры постоянны во времени и одинаковы во всех точках системы, то такое состояние системы называется равновесным.
Для равновесной
термодинамической системы существует
функциональная связь между параметрами
состояния, которая называется
уравнением состояния
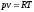
уравнение
Клапейрона — Менделеева
3 Смеси газов. Кажущаяся молекулярная масса. Газовая постоянная смеси газов.
Смесь газов
– механическое соединение не вступающих
друг с другом химическую реакцию газов.
Основным законом, определяющим поведение
газовой смеси, является закон Дальтона:
полное давление смеси идеальных
газов равно сумме парциальных давлений
всех входящих в нее компонентов: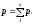 Парциальное давление pi — давление,
которое имел бы газ, если бы он один при
той же температуре занимал весь объем
смеси. Газовую постоянную смеси определяют
как:
Парциальное давление pi — давление,
которое имел бы газ, если бы он один при
той же температуре занимал весь объем
смеси. Газовую постоянную смеси определяют
как: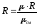 ,
, -
кажущаяся (средняя) молекулярная масса
смеси. При объемном составе
-
кажущаяся (средняя) молекулярная масса
смеси. При объемном составе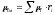 ,
при массовом составе:
,
при массовом составе: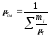 .
.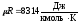 -универсальная
газовая постоянная.
-универсальная
газовая постоянная.
4 Первый закон термодинамики.
Первый закон термодинамики - это закон сохранения энергии, записанный с помощью термодинамических понятий (аналитическая формулировка: вечный двигатель 1 рода невозможен):
Энергия. Под внутренней энергией в термодинамике понимают кинетическую энергию движения молекул, потенциальную энергию их взаимодействия и нулевая (энергея движения частиц внутри молекулы при T=0K). Кинетическая энергия молекул является функцией температуры, значение потенциальной энергии зависит от среднего расстояния между молекулами и, следовательно, от занимаемого газом объема V, т. е. является функцией V. Поэтому внутренняя энергия U есть функция состояния тела.
Теплота. Энергия, предаваемая от одного тела к другому за счет разности температур, называется теплотой. Теплота может передаваться либо при непосредственном контакте между телами (теплопроводностью, конвекцией), либо на расстоянии (излучением), причем во всех случаях этот процесс возможен только при наличии разности температур между телами.
Работа.
Энергия, передаваемая от одного тела к
другому при изменении объема этих тел
или перемещение в пространстве, называется
работой. При конечном изменении объема
работа против сил внешнего давления,
называемая работой расширения, равна
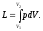 Работа изменения объема эквивалентна
площади под кривой процесса в диаграмме
р, v.
Работа изменения объема эквивалентна
площади под кривой процесса в диаграмме
р, v.
Внутренняя энергия — это свойство самой системы, она характеризует состояние системы. Теплота и работа — это энергетические характеристики процессов механического и теплового взаимодействий системы с окружающей средой. Они характеризуют те количества энергии, которые переданы системе или отданы ею через ее границы в определенном процессе.
Выражение
первого закона термодинамики

