
biokhimia_ekz
.pdfостатка рибозы тРНК (другой группой лигаз аминоацил переносится на 2'-ОН- группу). В аминоацил-тРНК карбоксильная группа аминокислотного остатка этерифицируется остатком рибозы 3'-концевого остатка аденозина, входящего в последовательность ...ССА-3'.
Точность трансляции зависит, прежде всего, от субстратной специфичности аминоацил-тРНК-лигаз. Корректирующий механизм активного центра лигазы обеспечивает немедленное удаление ошибочно присоединенных аминокислотных остатков. В среднем встречается только одна ошибка на 1300 аминокислотных остатков — поразительно высокая точность «работы», если представить, насколько близки структуры некоторых аминокислот 50. Взаимосвязь всех обменов.
Глюкозо6фосфат – активная форма глюкозы, которая идет на синтез гликогена. При распаде гликогена образуется глюкозо1фосфат и из нее глкозо6фосфат. Глюкозо6фосфат участвует в гликолизе, в результате чего образуется ПВК. С глюкозо6фосфата начинается ПФЦ, в результате чего образуется НАДФН (используется в реакциях восстановительного биосинтеза – синтез жирных кислот УиЛ) рубозо5фосфат и фосфорибозилпирофосфат синтез нуклеотидов (БиУ). ПВК – под действием лактатдегидрогеназы превращается в молочную кислоту. ПВК образуется при гликолизе, участвует в глюконеогенезе. ПВК превращается в оксалоацетат, который в реакции аминирования в аспартат (БиУ). Окислительное декарбоксилирование ПВК приводит к образованию АцКоА. АцКоА – образуется при окислительном декарбоксилировании ПВК, при бета-окислении жирных кислот (ЛиУ), из кетогенных а/к. АцКоА запускает ЦТК, идет на синтез жирных кислот, кетоновых тел и холестерина.
51. Роль ключевых метаболитов: глюкозо6фосфат, ПВК, АцКоА.
Глюкозо6фосфат – активная форма глюкозы, которая идет на синтез гликогена. При распаде гликогена образуется глюкозо1фосфат и из нее глкозо6фосфат. Глюкозо6фосфат участвует в гликолизе, в результате чего образуется ПВК. С глюкозо6фосфата начинается ПФЦ, в результате чего образуется рибозо5фосфат фосфорибозилпирофосфат синтез нуклеотидов. ПВК – под действием лактатдегидрогеназы превращается в молочную кислоту. ПВК образуется при гликолизе, участвует в глюконеогенезе. Окислительное декарбоксилирование ПВК приводит к образованию АцКОА. АцКоА – образуется при окислительном декарбоксилировании ПВК, при бета-окислении жирных кислот, из кетогенных а/к. АцКоА запускает ЦТК, идет на синтез жирных кислот, кетоновых тел и холестерина.
52.Липиды, классификация и распространение. Химическая природа, свойства и биологическая роль триглицеридов. Липиды играют важнейшую роль в процессах жизнедеятельности. Будучи одним из основных компонентов биологических мембран, липиды влияют на их проницаемость, участвуют в передаче нервного импульса, создании межклеточных контактов. Жир служит в организме весьма эффективным источником энергии либо при непосредственном использовании, либо потенциально – в форме запасов жировой ткани. В натуральных пищевых жирах содержатся жирорастворимые витамины и «незаменимые» жирные кислоты. Важная функция липидов – создание термоизоляционных покровов у животных и растений, защита органов и тканей от механических воздействий.
A. Простые липиды: сложные эфиры жирных кислот с различными спиртами.
1. Глицериды представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот.
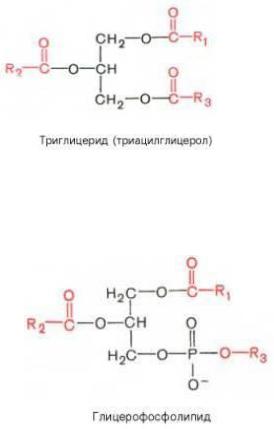
2. Воска: сложные эфиры высших жирных кислот и одноатомных или двухатомных спиртов.
Б. Сложные липиды: сложные эфиры жирных кислот со спиртами, дополнительно содержащие и другие группы.
1. Фосфолипиды: липиды, содержащие, помимо жирных кислот и спирта, остаток фосфорной кислоты. В их состав часто входят азотистые основания и другие компоненты:
а) глицерофосфолипиды (в роли спирта выступает глицерол);
б) сфинголипиды (в роли спирта – сфингозин).
2.Гликолипиды (гликосфинголипиды).
3.Стероиды.
4.Другие сложные липиды: сульфолипиды, аминолипиды. К этому классу можно отнести и липопротеины
B. Предшественники и производные липидов: жирные кислоты, глице-рол, стеролы и прочие спирты, альдегиды жирных кислот, углеводороды, жирорастворимые витамины и гормоны.
53.Классификация глицерофосфолипидов, химическое строение и биологическая роль в организме.
В их состав входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения. R1и R2– радикалы высших жирных кислот, a R3– чаще радикал азотистого соединения.
Классификация:
-Фосфатидилхолины (лецитины) соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин [НО—СН2—СН2—N+(CH3)3]
-Фосфатидилэтаноламины наличие в составе последних азотистого основания этаноламина
(HO—CH2—CH2—N+H3)
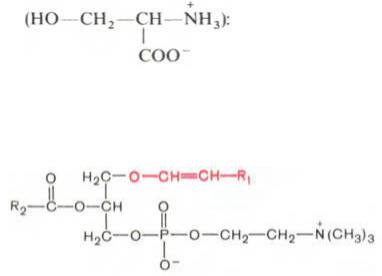
- Фосфатидилсерины. азотистым соединением служит остаток аминокислоты серина
-Фосфатидилинозитолы Радикалом (R3) в является шестиуглеродный циклический спирт инозитол. В животном организме найдены в мозге, печени и легких.
-плазмогены
-кардиолипин-является как бы «двойным» глицерофосфолипидом. Кардио-липин локализован во внутренней мембране митохондрий.
54.Стерины, стериды, их представители и свойства. Биологическая роль.
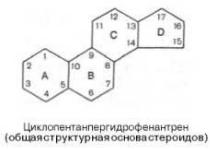 К стероидам относятся, гормоны коркового вещества надпочечников, желчные кислоты, витамины группы D, сердечные гликозиды и другие соединения. В организме человека важное место среди стероидов занимают стерины, т.е. стероидные спирты. Главным представителем стеринов является холестерин. Каждая клетка в организме млекопитающих содержит холестерин. Находясь в составе мембран клеток, неэтерифицированный холестерин вместе с фосфолипидами и белками обеспечивает избирательную проницаемость клеточной мембраны и оказывает регулирующее влияние на состояние мембраны и на активность связанных с ней ферментов. В цитоплазме холестерин находится преимущественно в виде эфиров с жирными кислотами, образующих мелкие капли – так называемые вакуоли. В плазме крови как неэтерифицированный, так и этерифицированный холестерин транспортируется в составе липопротеинов.
К стероидам относятся, гормоны коркового вещества надпочечников, желчные кислоты, витамины группы D, сердечные гликозиды и другие соединения. В организме человека важное место среди стероидов занимают стерины, т.е. стероидные спирты. Главным представителем стеринов является холестерин. Каждая клетка в организме млекопитающих содержит холестерин. Находясь в составе мембран клеток, неэтерифицированный холестерин вместе с фосфолипидами и белками обеспечивает избирательную проницаемость клеточной мембраны и оказывает регулирующее влияние на состояние мембраны и на активность связанных с ней ферментов. В цитоплазме холестерин находится преимущественно в виде эфиров с жирными кислотами, образующих мелкие капли – так называемые вакуоли. В плазме крови как неэтерифицированный, так и этерифицированный холестерин транспортируется в составе липопротеинов.
Холестерин – источник образования в организме млекопитающих желчных кислот, а также стероидных гормонов (половых и кортикоидных). Холестерин, а точнее продукт его окисления – 7-дегидрохолестерин, под действием УФ-лучей в коже превращается в витамин D3.
55.Переваривание и всасывание простых и сложных липидов в желудочнокишечном тракте. Возрастные особенности.
Расщепление липидов происходит в 12—перстной кишке, куда поступают липаза с соком поджелудочной железы и конъюгированные желчные кислоты в составе желчи.
Эмульгирование жира— обязательное условие для переваривания, так как делает гидрофобный субстрат более доступным для действия гидролитических ферментов — липаз. Эмульгирование происходит при участии желчных кислот, которые из—за своей амфифильности, окружают каплю жира и снижают поверхностное натяжение, что приводит к дроблению капли.
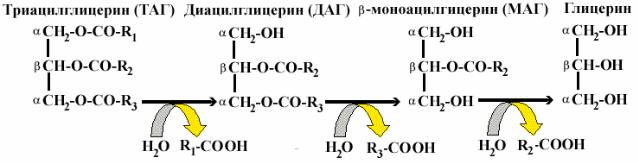
Гидролиз жираосуществляется при участии панкреатической липазы, которая, сорбируясь на поверхности капель жира, расщепляет эфирные связи в триацилглицеринах (ТАГ). Жирные кислоты отщепляются прежде всего из —положения. В результате образуется — диацилглицерин, затем —моноацилглицерин, который является основным продуктом гидролиза:
Всасываниепроисходит также при участии желчных кислот, которые образуют вместе с моноацилглицеринами, холестерином и жирными кислотами смешанные мицеллы — растворимые комплексы, обеспечивающие переход продуктов гидролиза в клетки слизистой кишечника. Желчные кислоты с током крови доставляются в печень, затем снова секретируются желчью в кишечник, то есть повторно используются, циркулируя по кругу: печень — кишечник — печень.
56.Судьба всосавшихся простых и сложных липидов. Жировые депо.
Липотропные вещества и ихроль. Ресинтез триглицеридов происходит в эпителиальных клетках двумя путями. Первый путь – β-моноглицеридный. Суть его состоит в том, что β- моноглицериды и жирные кислоты, проникающие в процессе всасывания в эпителиальные клетки кишечной стенки, задерживаются в гладком эндоплазматическом ретикулуме клеток. Здесь из жирных кислот образуется их активная форма – ацил-КоА и затем происходит ацилирование β- моноглицеридов с образованием сначала диглицеридов, а затем триглицеридов:
β-Моноглицерид + R—СО—S-KoA –> Диглицерид + HS-KoA ;
Диглицерид + R1—СО—S-KoA –> Триглицерид + HS-KoA.
Второй путь ресинтеза триглицеридов протекает в шероховатом эндоплазматическом ретикулуме эпителиальных клеток и включает следующие реакции:
1)образование активной формы жирной кислоты – ацил-КоА при участии ацил-КоА-синтетазы;
2)образование α-глицерофосфата при участии глицеролкиназы;
3)превращение α-глицерофосфата в фосфатидную кислоту при участии глицерофосфатацилтрансферазы;
4)превращение фосфатидной кислоты в диглицерид при участии фос-фатидат-фосфогидролазы;
5)ацилирование диглицерида с образованием триглицерида при участии диглицеридацилтрансферазы.
α-глицерофосфатный путь ресинтеза жиров (триглицеридов) приобретает значение, если в эпителиальные клетки слизистой оболочки тонкой кишки поступили преимущественно жирные кислоты. В случае, если в стенку кишки поступили жирные кислоты вместе с β-моноглицеридами, запускается β-моногли-церидный путь.
Ресинтезированные в эпителиальных клетках кишечника триглицериды и фосфолипиды, а также поступивший в эти клетки из полости кишечника холестерин соединяются с небольшим количеством белка и образуют относительно стабильные комплексные частицы – хиломикроны (ХМ). ХМ диффундируют в лимфатическую систему кишечника, а из нее – в грудной лимфатический проток. Затем из грудного лимфатического протока ХМ попадают в кровяное русло, т.е. с их помощью осуществляется транспорт экзогенных триглицеридов, холестерина и частично фосфолипидов из кишечника через лимфатическую систему в кровь. Известно, что печень и жировая ткань играют наиболее существенную роль в дальнейшей судьбе ХМ. Последние свободно диффундируют из плазмы крови в межклеточные пространства печени (синусоиды). ХМ не способны (из-за своих размеров) проникать в клетки жировой ткани. В связи с этим триглицериды ХМ подвергаются гидролизу на поверхности эндотелия капилляров жировой ткани при участии фермента липопротеидлипазы.
Липотропные вещества - витаминоподобные вещества холин, инозит, биотин и а/к метионин являются липотропными веществами - т. е. участвуют в обмене жиров, и их основная функция состоит в предупреждении ненормального или чрезмерного накопления жира в печени. Они увеличивают производство лецитина, который сохраняет холестерин более растворимым, очищает печень и увеличивает сопротивляемость заболеваниям.
57.Липопротеины. Состав и функции липопротеидов крови. Липиды входят в состав липопротеидов плазмы крови. Классы:
- ХМ — носители пищевых триглицеридов, синтезируются в клетках слизистой кишечника; -Липопротеидыочень низкой плотности (ЛПОНП) — носители эндогенных ТГ, синтезируются в
клетках печени; -Липопротеиды низкой плотности (ЛПНП) —являются конечным продуктом катаболизма ЛПОНП
иглавным переносчиком ХС в клетки организма;
-Липопротеиды высокой плотности (ЛПВП) —транспортируют холестерин из клеточных мембран в печень.
58.Депонирование и мобилизация жиров в жировой ткани. Физиологическое значение.
Транспорт и использование жирных кислот, образующихся при мобилизации жиров. Биосинтез и использованиекетоновых тел. Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии. При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии, то жир депонируется в адипоцитах —
специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жир. В качестве источника энергии могут использоваться только свободные, т.е. неэстерифицированные, жирные кислоты. Поэтому триглицериды сначала гидролизуются при помощи специфических тканевых ферментов – липаз – до глицерина и свободных жирных кислот. Последние из жировых депо могут переходить в плазму крови (мобилизация высших жирных кислот), после чего они используются тканями и органами тела в качестве энергетического материала.
Жирные кислотытранспортируются кровью в виде комплексов с сывороточными альбуминами в разные органы и ткани, где включаются в процесс окисления. Окисление жирных кислот состоит из двух этапов: —окислениеи цитратный цикл .
Оба этапа сопряжены с дыхательной цепью. —окислениепроисходит в митохондриях клетки, а жирная кислота поступает из кровотока в цитозоль, где активируется путем конденсации с коферментом А, образуя тиоэфир. Для того чтобы пройти через митохондриальную мембрану,
жирной кислоте необходим специальный переносчик — карнитин. Поэтому сначала ацильная группа переносится с ацил—СоА на карнитин. Ацил—карнитин пересекает мембрану и отдает свой ацильный фрагмент снова на кофермент А. Ферментом этой обратимой реакции служит ацил— карнитинтрансфераза. Результатом четырех последующих реакций —окисления является отщепление двухуглеродного фрагмента и перенос его на кофермент А с образованием ацетил— СоА, который затем может включаться в цитратный цикл для полного окисления. Укороченная ацильная цепь вторично входит в цикл —окисления. Конечным итогом повторяющихся циклов—окисления будет окисление всей ацильной цепи до ацетил—СоА. Основным путем дальнейшего использования ацетил—СоА, образованного при —окислении в печени,
является синтез кетоновых тел, который происходит следующим образом: двухуглеродные молекулы конденсируются друг с другом с образованием в дальнейших реакциях ацетоацетата и
—гидроксибутирата. Эти две кислоты называются кетоновыми телами. Кетоновые тела диффундируют в кровь и используются внепеченочными тканями в качестве источников энергии. В норме концентрация кетоновых тел в крови 2 мг/дл. Ферменты, катализирующие синтез кетоновых тел, находятся в митохондриях. В определенных метаболических условиях, когда в печени происходит интенсивное окисление жирных кислот, образуется значительное количество кетоновых тел.
59.Желчные кислоты, их строение и свойства. Участие в переваривании и всасывании липидов.
Желчные кислоты — первичные (хенодезоксихолевая и холевая) образуются в клетках печени из холестерина. После выделения в кишечник под влиянием бактерий они преобразуются во вторичные (литохолевая и дезоксихолевая). В кишечник желчные кислоты поступают в составе желчи в виде конъюгатов с глицином и таурином. Ранее описывались функции желчных кислот в процессе переваривания липидов. После переваривания и всасывания желчные кислоты возвращаются через воротную вену в печень, совершая такой цикл до 10 раз в сутки. Этот цикл называется кишечно—печеночная циркуляция желчных кислот. Постоянным компонентом желчи является холестерин. Как и желчные кислоты, он подвергается обратному всасыванию, но некоторое количество желчных кислот и холестерина теряются с калом. Для восполнения потери желчных кислот, выводимых с фекалиями, происходит постоянно синтез желчных кислот из холестерина. Получается, что удаление холестерина в свободном виде или в виде желчных кислот является единственным способом освобождения организма от него.
60. Окисление высших жирных кислот. Последовательность реакций окисления. Связь окисления жирных кислот с цитратным циклом и дыхательной цепью. Энергетический эффект окисления.
Свободная жирная кислота независимо от длины углеводородной цепи является метаболически инертной и не может подвергаться никаким биохимическим превращениям, в том числе окислению, пока не будет активирована. Активация жирной кислоты протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой. В результате реакции образуется ацилКоА, являющийся активной формой жирной кислоты. Переносчиком активированных жирных кислот с длинной цепью через внутреннюю митохондриальную мембрану служит карнитин. После прохождения ацилкарнитина через мембрану митохондрий происходит обратная реакция – расщепление ацилкарнитина
Внутримитохондриальное окисление жирных кислот.Ацил-КоА под действием Ацил-КоА дегидрогеназы превращается в Еноил-КоА→под действ. Еноил-КоА-гидратазы в 3-гидроксиацил- КоА →3-оксиацил-КоА →Ацил-КоА и .ацетил-КоА. Образовавшийся ацетил-КоА подвергается окислению в цикле трикарбоновых кислот, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь β-окисления вплоть до образования бутирил-КоА, который в свою очередь окисляется до 2 молекул ацетил-КоА.
При каждом цикле β-окисления образуются одна молекула ФАДН2 и одна молекула НАДН. Последние в процессе окисления в дыхательной цепи и сопряженного с ним фосфорилирования дают: ФАДН2 – 2 молекулы АТФ и НАДН – 3 молекулы АТФ, т.е. в сумме за один цикл образуется 5 молекул АТФ. При окислении пальмитиновой кислоты образуется 5 х 7 = 35 молекул АТФ. В процессе β-окисления пальмитиновой кислоты образуется 8 молекул ацетил-КоА, каждая из которых, «сгорая» в цтк, дает 12 молекул АТФ, а 8 молекул ацетил-КоА дадут 12 х 8 = 96 молекул АТФ.
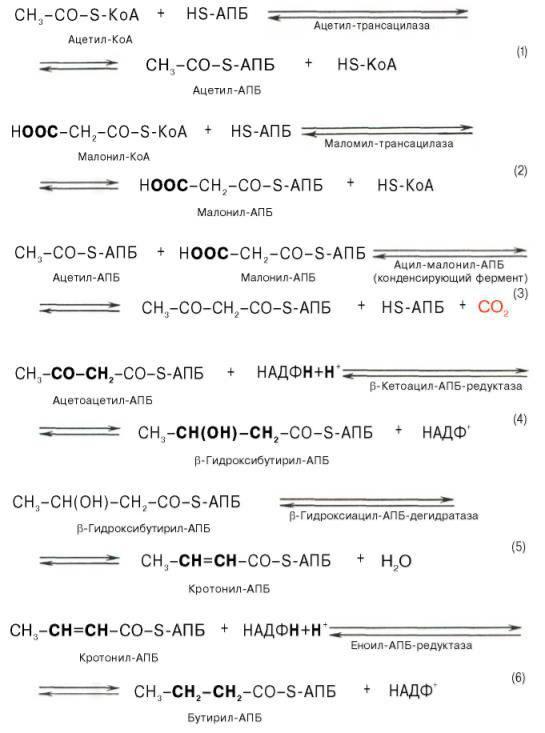
61.Биосинтез жирных кислот, последовательность реакций.Физиологическое значение. Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот.
Далее цикл реакций повторяется.
62.Биосинтез триацилглицеринов. Биосинтез холестерина. Атеросклероз.
Сложные липиды, такие, как нейтральные жиры (триацилглицерины), фосфо- и гликолипиды, синтезируются по основным реакционным путям. Синтез начинается (на схеме внизу) с sn-З-глицерофосфата. Обозначение
«sn» |
относится |
к стереохимической |
номенклатуре, |
так |
как |
симметричный глицерин после |
|||||
присоединения фосфата приобретает хиральность. |
sn-3-Глицерофосфат образуется |
при восстановлении [1] |
|||||||||
промежуточного |
|
продукта гликолиза,дигидроксиацетон-3-фосфата, |
или |
|
в |
||||||
результате фосфорилирования глицерина [2]. |
|
Приэтерификации sn-3-глицерофосфата |
по |
C-1 |
|||||||
длинноцепочечной жирной |
кислотой образуются |
лизофосфатиды |
[3], |
|
при |
||||||
повторной этерификации ненасыщенной жирной |
кислотой по |
С-2 |
|
—фосфатидаты [4], |
ключевые |
||||||
промежуточные продукты в биосинтезе жиров, фосфо- игликолипидов. |
|
|
|
|
|
||||||
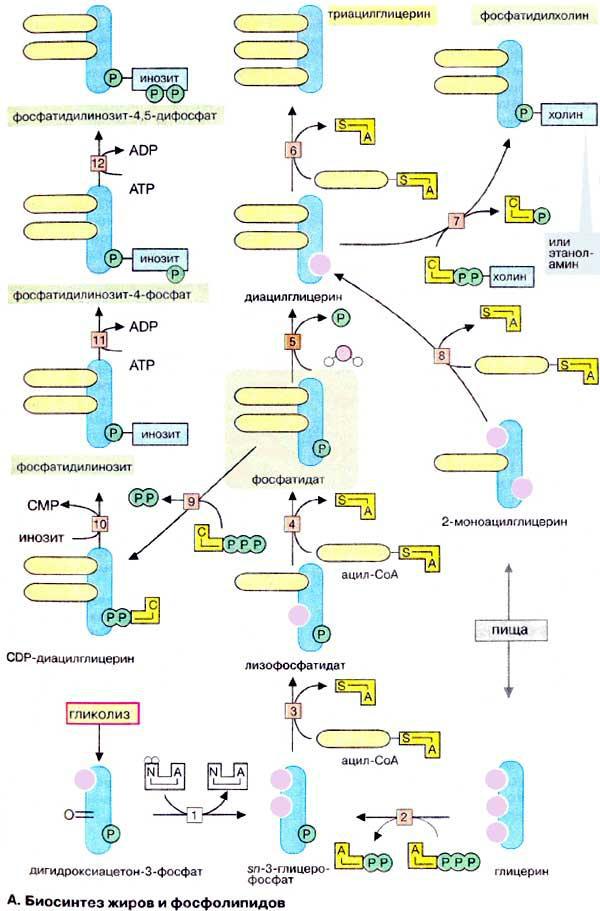
Из фосфатидовых |
кислот после |
гидролитического |
отщепления |
фосфатной |
группы |
[5] |
и |
последующего ацилирования жирной |
кислотой [6] |
образуются триацилглицерины (жиры). |
После |
||||
завершения биосинтеза нейтральные жиры сохраняются в цитоплазме в виде жировых капель. |
|
|
|||||
Из фосфатидовых |
кислот также |
через |
промежуточное |
образование |
диацилглицерина |
синтезируется фосфатидилхолин (лецитин) [7]. Фосфохолиновая группа переносится на диацилглицерин из холинцитидиндифосфата [ЦДФ-холина (CDP-холина)] (см. с. 112), представляющего собой активированную форму холина.
По |
аналогичной реакции диацилглицерина |
|
и |
|
|
ЦДФ-этаноламина |
образуется |
||||||
фосфатидилэтаноламин. Фосфатидилсерин образуется |
из фосфатидилэтаноламина путем |
|
обмена |
||||||||||
аминоспиртовых групп. |
Последующие реакции заключаются |
во |
взаимопревращениифосфолипидов: |
||||||||||
например, фосфатидилсерин декарбоксилируется |
с образованиемфосфатидилэтаноламина; |
последний |
в |
||||||||||
результате метилирования S-аденозилметионином превращается в фосфатидилхолин. |
|
|
|
|
|||||||||
Для биосинтеза нейтральных |
жиров, |
фосфо- |
|
|
и гликолипидов также |
используются |
|||||||
пищевыелипиды. Нейтральные |
жиры расщепляются |
|
|
в |
пищеварительном |
|
тракте |
||||||
панкреатическимилипазами до жирных кислот и |
2-моноацилглицеринов. |
Эти метаболиты всасываются |
|||||||||||
слизистой |
кишечника и |
используются в качестве предшественников в |
синтезе липидов (см. |
с. 266). |
|||||||||
Последовательное ацилирование 2-моноацилглицерина |
с |
образованием |
в |
качестве |
конечных |
||||||||
продуктов нейтральных |
жиров катализируется |
двумя |
|
ацилтрансферазами |
[8, |
|
6] |
в |
|||||
последовательности реакций: 2-моноацилглицерин → диацилглицерин → триацилглицерин (нейтральный жир).
Биосинтез холестерина.
3 основные стадии: I – превращение активного ацетата в мевалоновую кислоту, II – образование сквалена из мевалоновой кислоты, III – циклизация сквалена в холестерин. Рассмотрим стадию превращения активного ацетата в мевалоновую кислоту. Начальным этапом синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции.
Затем при последующей конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА при участии гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтаза) образуется β-гидрокси-β- метилглутарил-КоА. Далее β-гидрокси-β-метилглутарил-КоА под действием регуляторно-го фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза) в результате восстановления одной из карбоксильных групп и отщепления HS-KoA превращается в мевалоновую кислоту.
Атеросклероз — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов. Отложения формируются в виде атероматозных бляшек. Последующее разрастание в них соединительной ткани (склероз), и кальциноз стенки сосуда приводят к деформации и сужению просвета вплоть до облитерации (закупорки).теория липопротеидной инфильтрации — первично накопление липопротеидов в сосудистой стенке.
63.Липопротеины, холестерин, их связь с развитием атеросклероза.
Атеросклероз — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов. Отложения формируются в виде атероматозных бляшек. Последующее разрастание в них соединительной ткани (склероз), и кальциноз стенки сосуда приводят к деформации и сужению просвета вплоть до облитерации (закупорки).теория липопротеидной инфильтрации — первично накопление липопротеидов в сосудистой стенке.
