
- •Основные теоретические сведения
- •Предельные углеводороды
- •1.1. Общие сведения, номенклатура предельных углеводородов
- •1.2. Химические свойства
- •Этиленовые углеводороды
- •Общие сведения, номенклатура этиленовых углеводородов
- •2.2. Химические свойства алкенов
- •Реакции окисления
- •Ацетиленовые углеводороды
- •Общие сведения, номенклатура ацетиленовых углеводородов
- •Химические свойства ацетиленовых углеводородов
- •Реакции присоединения
- •Реакции замещения
- •Реакции полимеризации
- •Реакции конденсации с карбонильными соединениями
- •Экспериментальная часть
- •Контрольные вопросы
- •Список рекомендуемой литературы
Этиленовые углеводороды
Общие сведения, номенклатура этиленовых углеводородов
Алкены – ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Атом углерода в молекуле находится в состоянии sp2-гибридизации атомных орбиталей. Простейший представитель ряда – этилен СH2=CH2. Общая формула гомологического ряда алкенов CnH2n.
Согласно систематической номенклатуре названия этиленовых углеводородов производят из названий соответствующих алканов с заменой суффикса -ан на –ен. Алкены простого строения называют заменяя суффикс -ан на -илен.
Таблица 2
Углеводороды ряда этилена
|
Предельные углеводороды |
Этиленовые углеводороды |
|
Метан СН4 |
- |
|
Этан С2Н6 |
Этен (этилен) С2Н4 |
|
Пропан С3Н8 |
Пропен (пропилен) С3Н6 |
|
Бутан С4Н10 |
Бутен (бутилен) С4Н8 |
|
Пентан С5Н12 |
Пентен (амилен) С5Н10 |
|
Гексан С6Н14 |
Гексен (гексилен) С6Н12 |
|
и.т.д. |
и.т.д. |
Двойная связь в молекуле этилена – это сочетании одной и одной -связи. Приблизительная энергия -связи 350 кДж/моль, -связи 262,4 кДж/моль. Длина связи между атомами углерода составляет 0,134 нм.
2.2. Химические свойства алкенов
Химические свойства олефинов определяются наличием в их молекуле -связи. Будучи более энергодоступной, -связь разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов или групп атомов. Ионное присоединение реагентов к -связи носит электрофильный характер AdЕ (от английского слова addition – присоединение и латинского electrophilic – электрофильный, любящий отрицательное).
Под влиянием
-электронного
облака олефина молекула галогена
поляризуется
![]() ,
при этом образуется наведенный диполь.
,
при этом образуется наведенный диполь.
Положительный конец диполя выступает как электрофильный реагент и захватывает -электроны двойной связи с образованием неустойчивого -комплекса:
![]()



этилен -комплекс


-комплекс карбкатион
На II этапе -связь и связь хлор-хлор гетеролитически разрывается. Хлор за счет -электронов этилена образует обычную -связь с одним из атомов углерода. Этот атом углерода переходит в состояние sp3-гибридизации атомных орбиталей. Второй атом углерода двойной связи, лишившись электронов, заряжается положительно, и вся частица становится карбкатионом (частица с положительным зарядом на углероде). Положительно заряженный атом углерода в карбкатионе находится в состоянии sp2-гибридизации. Карбкатион также называется -комплексом.

карбкатион дихлорэтан
На III этапе процесса карбокатион, взаимодействуя с анионом Cl-, образует с ним -связь за счет пары электронов аниона.
Реакции присоединения могут быть:
1) Гидрирование (присоединение водорода) происходит в присутствии катализаторов Pt , Pd или Ni :
![]()
этилен этан
2) Галогенирование (присоединение Сl2, Br2):
![]()
этилен
![]()
![]()
1,2 дибромэтан
Присоединение Br2 к олефину – это качественная реакция для обнаружения этиленовых углеводородов. При пропускании этилена через раствор Br2 в воде, имеющей желто-коричневую окраску, происходит обесцвечивание раствора вследствие реакции присоединения.
3) Гидрогалогенизирование (присоединение галогеноводорода)
В.В. Марковников, изучая реакции присоединения галогеноводородов к несимметричным алкенам, установил следующую закономерность: водород присоединяется по месту двойной связи к наиболее гидрогенизированному (связанному с большим числом водородных атомов) атому углерода, а галоген – к наименее гидрогенизированному. С позиции электронной теории правило Марковникова можно объяснить так: в результате двухстадийного электрофильного присоединения в качестве промежуточных продуктов могут образоваться два разных по устойчивости карбкатиона:

![]() I
I
II
Из них наиболее
устойчив первый. Поэтому реакции
электрофильного присоединения по
двойной связи идут в направлении
образования наиболее устойчивого
промежуточного карбкатиона I:![]()
![]()
![]()
пропилен 2-хлорпропан
4) Гидратация (присоединение воды)
В присутствии катализаторов (концентрированной H2SO4, ZnCl2) к алкенам присоединяется вода с образованием спиртов. Реакция идет в соответствии с правилом Марковникова.
![]()
![]()
![]() пропилен
пропанол-2
пропилен
пропанол-2
Реакции полимеризации позволяют получить высокомолекулярные соединения – полиэтилен и полипропилен
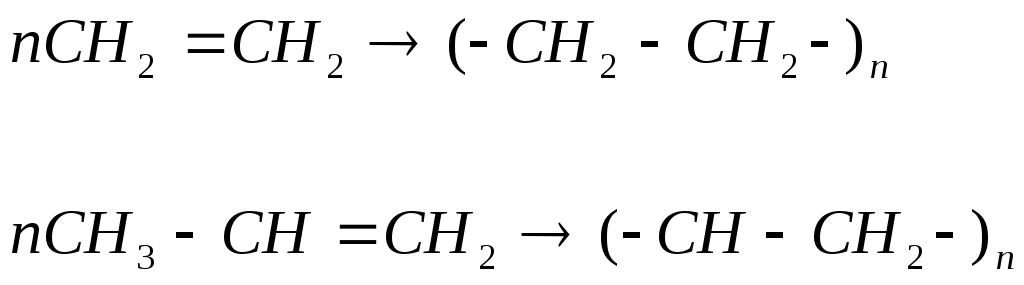
![]()
