
- •Химия гетероциклических соединений
- •49 01 01, 49 01 02, 91 01 01, 48 01 02
- •Содержание
- •Введение
- •Номенклатура гетероциклических соединений
- •Пятичленные гетероциклические соединения с одним гетероатомом
- •Источники и методы получения фурана, тиофена и пиррола
- •Получение из 1,4-дикарбонильных соединений
- •Получение фурана и пиррола из слизевой кислоты
- •Галогенирование
- •Сульфирование
- •Нитрование
- •Ацилирование
- •Восстановление и окисление пятичленных гетероциклических соединений.
- •Реакции гидрирования
- •Реакция окисления
- •Другие реакции пятичленных гетероциклических соединений
- •Фурфурол, особенности его химического поведения
- •Важнейшие производные пиррола
- •Индол и его важнейшие производные
- •Способы получения индола
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Пиразол (1,2-диазол)
- •Имидазол (1,3-диазол)
- •Тиазол (1-тиа-3-азол)
- •Шестичленные гетероциклические соединения
- •Пиридин (азин)
- •Биологически активные соединения пиридинового ряда
- •Понятие о хинолине, изохинолине, акридине
- •Хинолин
- •Изохинолин
- •Акридин
- •Шестичленные гетероциклические соединения с двумя атомами азота
- •Пиримидин, пиримидиновые основания
- •5.2 Пурин, пуриновые основания
- •Понятие о нуклеозидах и нуклеотидах
- •Шестичленные кислородсодержащие гетероциклические соединения неароматического характера и их природные производные
- •Кумарин (-бензопирон)
- •Хромон (-бензопирон)
- •Литература
Биологически активные соединения пиридинового ряда
Многие производные пиридина обладают ярко выраженной биологической активностью. Ядро пиридина содержится в молекуле витамина РР, являющегося амидом никотиновой (-пиридинкарбоновой) кислоты:
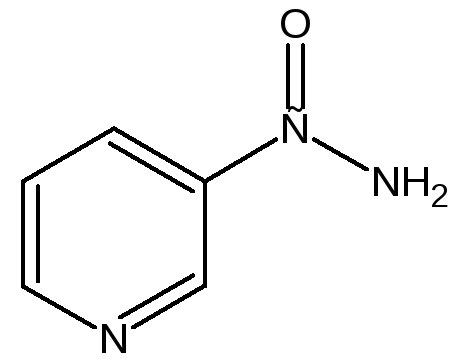
Витамин РР применяется для лечения пеллагры и других заболеваний, а также входит в состав никотинамидадениндинуклеотида (НАД+) и никотинамидадениндинуклеотидфосфата (НАДФ+), являющихся коферментами большого числа ферментов оксидоредуктаз, катализирующих окислительно-восстановительные реакции, лежащие в основе биологического окисления.
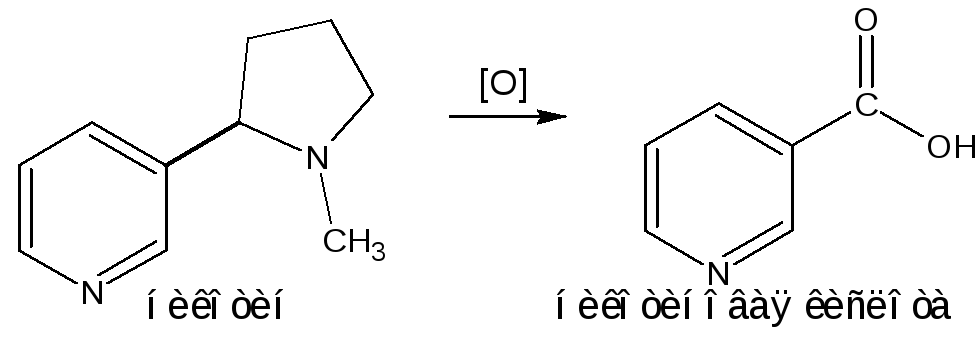
Пиридиновый цикл является также основным структурным элементом молекул многих алкалоидов. Алкалоиды – это группа азотистых соединений, обладающих основными свойствами и встречающихся в основном в растениях. Очень часто алкалоиды обладают сильным физиологическим или фармакологическим действием. Ряд известных алкалоидов содержит ядро пиридина и пиперидина. К ним относятся никотин, анабазин, кониин и др. Никотин в виде солей лимонной и яблочной кислот (является сильным основанием) в большом количестве (до 3%) содержится в листьях и корнях табака. Это один из наиболее ядовитых алкалоидов, 40 мг никотина является смертельной дозой для человека. В небольших дозах он возбуждает центральную и периферическую нервные системы, повышает кровяное давление.
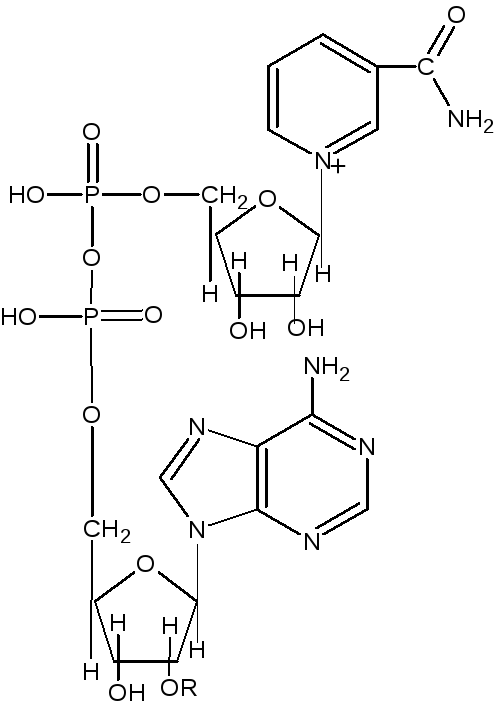
где R=H, PO3H2
НАД+ (R=H)
НАДФ+ (R=РО3Н2)
Рисунок 1 – Структурные формулы никотинамидадениндинуклеотида (НАД+) и никотинамидадениндинуклеотидфосфата (НАДФ+)
Анабазин – изомер никотина, содержится в листьях табака:
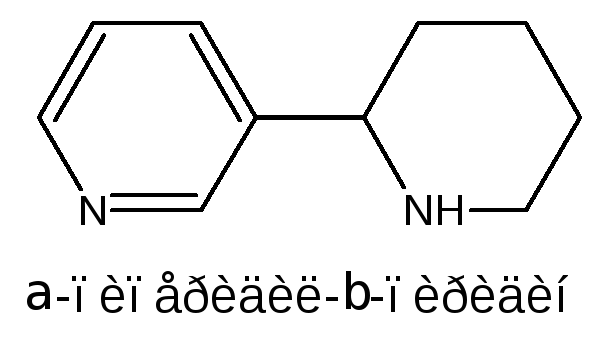
Являясь сильным ядом для насекомых, анабазин вместе с никотином применяется в сельском хозяйстве в качестве инсектицида.
Кониин – сильный яд, содержащийся в соке болиголова, вызывающий паралич двигательных центров, а в больших дозах – паралич дыхательного центра.

Витамин В6 представляет собой смесь трех веществ – пиридоксаля I, пиродоксола II и пиродоксамина III, которые являются производными 3-гидроксипи-ридина и отличаются друг от друга природой замещающей группы в положении 4 пиридинового кольца:
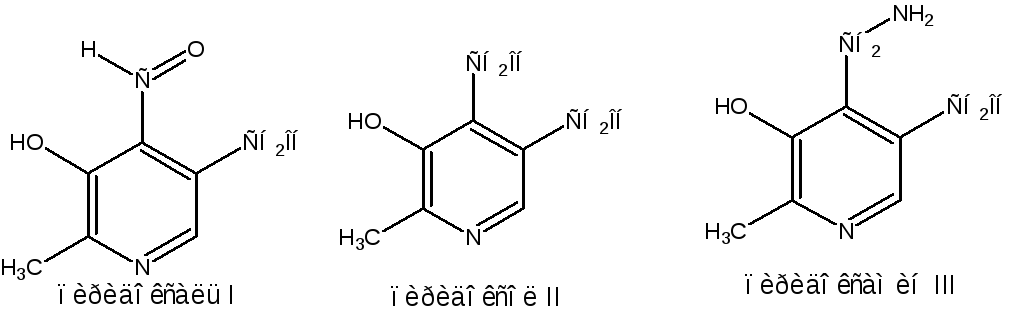
Эти витамины входят в структуру ферментов, регулирующих белковый обмен и катализирующих, в частности, реакции переаминирования и декарбоксилирования аминокислот. Оказалось, что коферментные функции выполняют только фосфорилированные производные пиродоксаля и пиридоксамина.
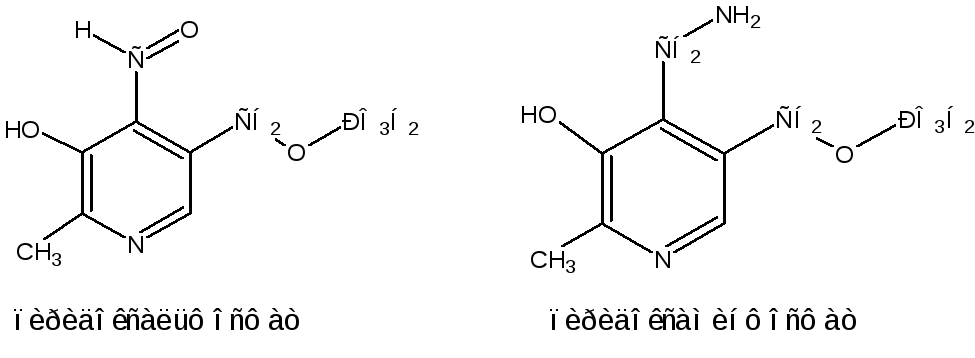
Доказано, что пиридоксальфосфат является простетической группой ферментов аминотрансфераз, катализирующих обратимый перенос аминогруппы от аминокислот на -кетокислоту, и декарбоксилаз аминокислот, осуществляющих необратимое отщепление СО2 от карбоксильной группы аминокислот с образованием биогенных аминов.
Понятие о хинолине, изохинолине, акридине
Хинолин, изохинолин и акридин относятся к бензо- или дибензопроизводным пиридина (акридин). В зависимости от того, как бензольное кольцо сконденсировано с пиридиновым циклом, существует два бензопроизводных пиридина: хинолин и изохинолин:
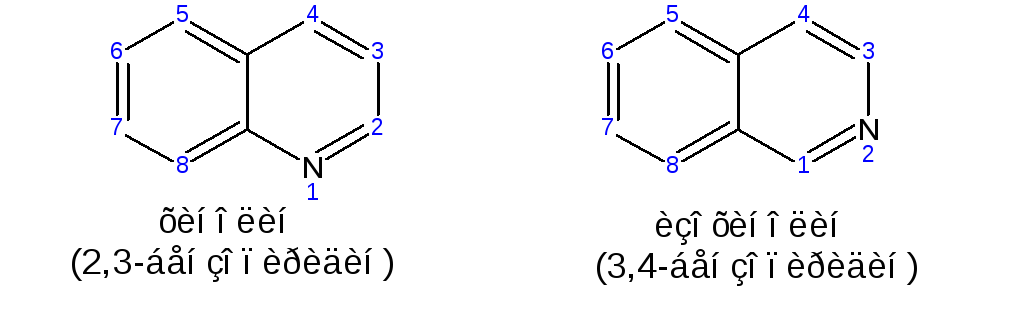
Подобно тому, как пиридин является гетероаналогом бензола, хинолин и изохинолин – гетероаналоги нафталина.
Хинолин
Хинолин и его гомологи содержатся в каменноугольной смоле, а также в некоторых нефтях, откуда их и получают. Кроме этого, разработаны синтетические методы получения этих соединений. Из них наиболее широко используется синтез Скраупа, который заключается в нагревании анилина с глицерином и концентрированной серной кислотой в присутствии нитробензола в качестве окислителя. В результате дегидратации серной кислотой глицерин превращается в акролеин, который конденсируется с анилином в дигидрохинолин, окисляющийся в хинолин нитробензолом:
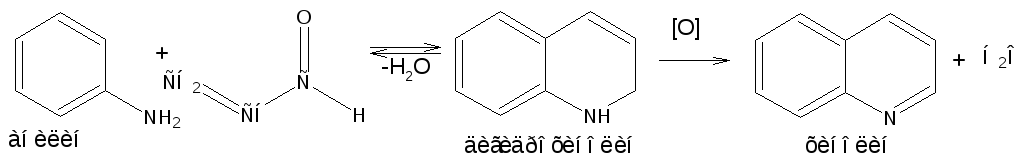
Хинолин подобен пиридину как по физическим свойствам, так и по химическим превращениям. Основные свойства у хинолина менее выражены, что является результатом влияния бензольного кольца, в сторону которого и смещена электронная плотность. Но как и пиридин, хинолин образует соли хинолиния с кислотами: соляной, серной, азотной; легко оксиляется в N-окись:
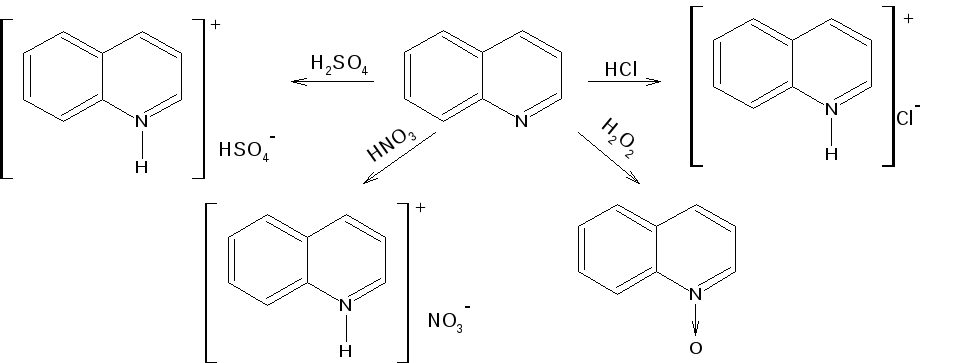
Являясь ароматической системой, содержащей децет -электронов, хинолин вступает в реакции электрофильного и нуклеофильного замещения.
Электрофильные реагенты атакуют бензольную половину молекулы хинолина в положения 5 и 8, причем реакции протекают легче, чем для пиридина:
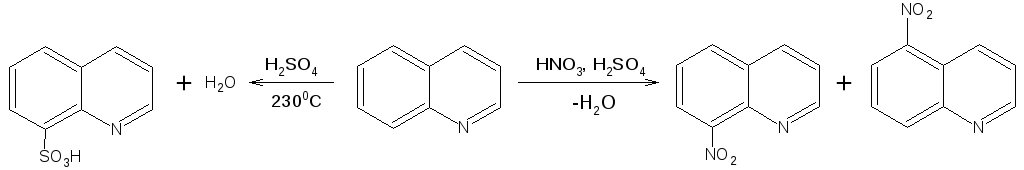
Реакции нуклеофильного замещения протекают по пиридиновому кольцу в положения 2 и 4, причем для 2- и 4-оксихинолинов возможна окси-оксо-таутомерия (оксо-форма более устойчива):

При оксилении хинолина образуется 2,3-пиридиндикарбоновая (хинолиновая) кислота, т.е. окисляется бензольное кольцо. Восстановлению, наоборот, поддается пиридиновый цикл:
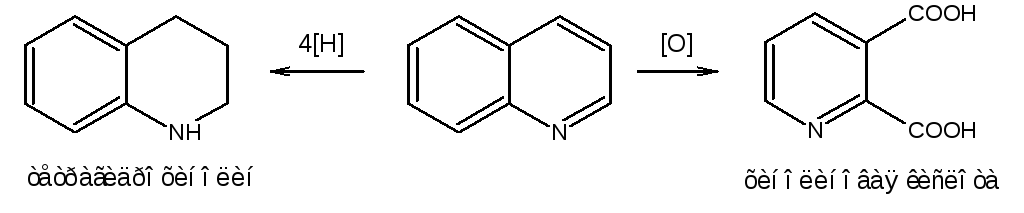
Ряд замещенных хинолина используется в синтезе лекарственных препаратов и красителей. 8-оксихинолин (оксин) широко применяется в качестве реагента в аналитической химии. В природе хинолиновое и изохинолиновое ядра встречаются в молекулах алкалоидов (хинин, папаверин), наркотиков (морфин, кодеин, героин и т.д.).
