
5.6 Атом водорода
.pdf
Содержание лекции:
•Модель атома Томсона.
•Опыты Резерфорда по рассеянию альфачастиц.
•Ядерная модель атома.
•Эмпирические закономерности в атомных спектрах.
•Формула Бальмера
•Атом Бора
•Опыты Франка и Герца
Развитие представлений об атоме
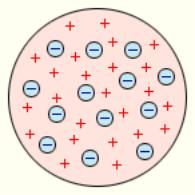
Модель атома Томсона «пудинг с изюмом» 1903 г.
• Атом – электрически нейтральная система шарообразной формы радиусом примерно равным 10–10 м
• Положительный заряд атома равномерно распределен по всему объему шара
• Отрицательно заряженные электроны находятся внутри шара. При отклонении электрона от положения равновесия возникают силы, стремящиеся возвратить его в исходное положение, что порождает колебания электронов и обуславливает излучение атомов.

Джозеф Джон Томсон
(1856-1940)
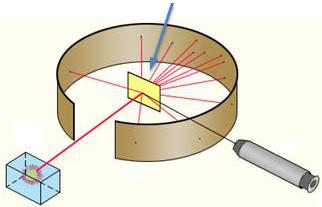
Опыты Резерфорда (1911 г.)
золотая фольга
экран
источник -частиц микроскоп
Масса α-частиц в 7300 раз больше массы электрона, а положительный заряд равен +2e
Резерфорд использовал α-частицы с кинетической энергией около 5 МэВ (скорость таких частиц велика – порядка 107 м/с)
Результаты
Большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения
Однако небольшая часть частиц отклоняется на значительные углы. Очень редкие α-частицы (приблизительно одна на двадцать тысяч) испытывали отклонение на углы больше 150°

Эрнест Резерфорд
(1871-1937)

Планетарная модель атома Резерфорда
•Отклонение -частиц на большие углы возможно, если есть локализованный положительный заряд.
•В центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10–14 … 10–15 м
•Ядро содержит весь положительный заряд и не менее 99,95 % его массы
• Плотность ядерного в-ва: ρ ≈ 1015 г/см3
• Заряд ядра равен суммарному заряду всех электронов, входящих в состав атома
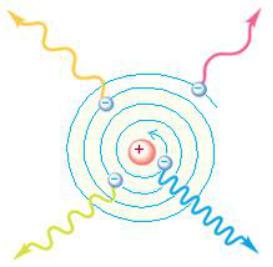
•В центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома.
•Вокруг ядра, подобно планетам, вращаются под действием кулоновских сил со стороны ядра электроны
•Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро
Недостатки модели Резерфорда:
•По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию.
•За время порядка 10–8 с все электроны в атоме Резерфорда должны растратить свою энергию и упасть на ядро.
•Спектры атомов должны быть сплошными, а не линейчатыми (как в экспериментах)

Линейчатые спектры
•Простейшим из атомов является водород
•Ядро атома водорода – протон,
заряд = +е; масса = 1836 те
• Линейчатый спектр – дискретные спектральные линии в излучении атома водорода
• Обобщённая формула Бальмера:
|
1 |
|
1 |
|
|
|
||
R |
|
|
|
|
|
; |
m 1, 2, 3,...; |
n m 1, m 2,... |
|
2 |
n |
2 |
|||||
m |
|
|
|
|
|
|
||
R = 3,29 1015 1/с – постоянная Ридберга

Иоганн Якоб Бальмер |
Йоханнес Роберт Ридберг |
(1825-1898) |
(1854-1919) |
