
- •1. Строение атома
- •2. Химическая связь
- •3. Химическая термодинамика
- •Кинетика и равновесие химических реакций
- •Концентрация растворов
- •Электролитическая диссоциация
- •6 Гальванический элемент
- •Электролиз
- •Коррозия металлов
- •Энтальпии образования веществ, стандартные энтропии и температурные коэффициенты в уравнении теплоемкости
- •Электроотрицательность элементов по Полингу
- •Константы диссоциации кислот и оснований в водных растворах
- •Стандартные электродные потенциалы металлов (ряд напряжений)
Электролитическая диссоциация
Задание 1. Напишите уравнения диссоциации электролитов, указанных в табл. 6. Для слабых электролитов приведите выражение для константы диссоциации.
Таблица 6.
|
Номер варианта |
Электролиты |
|
1 |
H2SO4, H2SO3, CrOH(NO3)2, Ba(OH)2, KHCO3 |
|
2 |
H2CO3, FeOHCl2, NaHSO3,NaHSO4, Ca(OH)2 |
|
3 |
Na3PO4, SnOHNO3, Ba(NO3)2, RbHS, Sr(OH)2 |
|
4 |
H2S, Fe(OH)3, Na2HPO4, ZnOHCl, K2SO4 |
|
5 |
H3BO3, Pb(NO3)2, KH2PO4, Ni(OH)2, MgOHCl |
|
6 |
CaHPO4, Ba(OH)2, (CuOH)2SO4, HF, H2SO4 |
|
7 |
Pb(OH)2, LiHS, InOH(NO3)2, Ba(NO3), H2SO3 |
|
8 |
Pb(NO3)2, Ba(OH)2, NaHCO3, NaHSO4,, AlOHCl2 |
|
9 |
Fe(OH)SO4, Cu(NO3)2, H2SO4, CaHPO4, Mg(OH)2 |
|
10 |
Zn(OH)2, Ba(OH)2, NiOHCl, LiHCO3, Co(NO3)2 |
|
11 |
BiOH(NO3)2, Ba(H2PO4)2, AlCl3, Cu(OH)2, Ca(OH)2 |
|
12 |
Ni(OH)2, Sr(OH)2, H2SO3, KHSO4, InOH(NO3)2 |
|
13 |
GaOHCl2, LiHS, Cu(NO3)2, H2CO3, Ba(OH)2 |
|
14 |
H2S, H2SO4, CrOHCl2, Mn(OH)2, Li2(HPO4) |
|
15 |
Cd(OH)2, FeOHSO4, KHSO3, H3PO4, Ba(NO3)2 |
|
16 |
Zn(NO3)2, Zn(OH)2, LiHSO3, CoOHCl, HCN |
|
17 |
NH4OH, Co(HSO4)2,, (ZnOH)2SO4, Cu(NO3)2, H3BO3 |
|
18 |
CaHPO4, BaCl2, AlOHBr2, Ni(OH)2, H2SO4 |
|
19 |
Al(OH)3, Sr(OH)2, H3PO4, Ba(HSO4)2, CrOH(NO3)2 |
|
20 |
CsNO3, LiHS, FeOHSO4, HAlO2, H2CO3 |
|
21 |
(NH4)2SO4, KHCO3, KHSO4, Cr(OH)3, TiOHCl2 |
|
22 |
Mg(OH)2, LiH2PO4, FeOHSO4,CH3COOH, Na2SO4 |
|
23 |
BiOH(NO3)2, Co(OH)2, H2SO3, KClO4, KHSO3 |
|
24 |
H2SO3, Ba(HCO3)2, AlOHClL2, Sr(OH)2, Cr2(SO4)2 |
|
25 |
Ca(NO3)2, Cr(OH)2NO3, NaH2BO3, H2SeO4, Fe(OH)3 |
|
26 |
Zn(OH)2, (CoOH)2SO4, Ba(HSO3)2, H2S, CH3COONa |
|
27 |
Al2(SO4)3, Ba(H2PO4)2, HCN, FeOHSO4, Ca(OH)2 |
|
28 |
Co(HSO4)2, (NH4)2CO3, Mg(OH)2, CuOHCl, KHS |
|
29 |
InOH(NO2)2, KH2PO4, AlCl3, H3BO3, Cu(OH)2 |
|
30 |
(NH4)2HPO4, FeOHCl2, Sr(OH)2,Be(OH)2, H2SO3 |
Пример 1. Напишите уравнения диссоциации гидроксида кальция и гидроксида никеля.
Решение. Ca(OH)2 является сильным электролитом (основание щелочно-земельного металла), поэтому диссоциирует необратимо в одну стадию:
Ca(OH)2 Ca2+ +2OH-.
Ni(OH)2 – малорастворимое в воде основание, является слабым электролитом.
Ni(OH)2 диссоциирует ступенчато в две стадии. Процесс диссоциации слабых электролитов протекает обратимо, следовательно, можно записать выражение константы диссоциации:
I Ni(OH)2 NiOH+ +OH-

II. NiOH+ Ni2+ +OH-
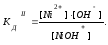
Пример 2. Напишите уравнения диссоциации серной и сероводородной кислот.
Решение. Серная кислота – сильный электролит, диссоциирует в одну стадию:
H2SO4 2H++SO42-.
H2S – слабый электролит, диссоциирует в две стадии:
I. H2SH++HS-

II. HS-H++S2-
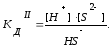
Пример 3. Напишите уравнения диссоциации сульфата алюминия, гидроксонитрата магния и гидрофосфата натрия.
Решение. Сульфат алюминия Al2(SO4)3 относится к средним солям, является сильным электролитом:
Al2(SO4)3 2Al3++3SO42-.
При диссоциации основных и кислых солей первая стадия диссоциации соответствует диссоциации сильного электролита, а остаток основания или кислоты диссоциирует как слабый электролит:
Гидроксонитрат магния MgOHNO3 – основная соль, диссоциирует по схеме:
I. MgOHNO3 MgOH++OH- сильный электролит.
II. MgOH+Mg2++ OH- слабый электролит.
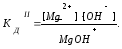
Гидрофосфат натрия Na2HPO4 – кислая соль, диссоциирует по схеме:
I. Na2HPO4 2Na++HPO42- сильный электролит.
II. HPO42- H++ PO43- слабый электролит.
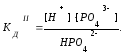
Задание 2. Определите pH раствора заданной концентрации С (табл. 7). При расчете pH раствора слабого электролита учитывайте первую стадию диссоциации. Значения констант диссоциации слабых электролитов приведены в справочных таблицах.
Таблица 7.
|
Номер вар. |
Раствор |
С, моль/л |
Номер вар. |
Раствор |
С, моль/л |
|
1 |
Ca(OH)2 |
0,01 |
16 |
H3AsO3 |
0,08 |
|
2 |
H2SeO4 |
0,1 |
17 |
HIO |
0,025 |
|
3 |
H2SO3 |
0,02 |
18 |
Ba(OH)2 |
0,01 |
|
4 |
H3BO3 |
0,055 |
19 |
H2CO3 |
0,02 |
|
5 |
KOH |
0,05 |
20 |
LiOH |
0,01 |
|
6 |
H3PO4 |
0,03 |
21 |
H3AsO4 |
0,07 |
|
7 |
HNO3 |
0,1 |
22 |
Sr(OH)2 |
0,005 |
|
8 |
Ba(OH)2 |
0,03 |
23 |
HI |
0,025 |
|
9 |
HNO2 |
0,2 |
24 |
HMnO4 |
0,003 |
|
10 |
HCN |
0,035 |
25 |
H2S |
0,005 |
|
11 |
HMnO4 |
0,45 |
26 |
H3PO3 |
0,02 |
|
12 |
NH4OH |
0,002 |
27 |
HClO2 |
0,004 |
|
13 |
H2SeO3 |
0,07 |
28 |
Ra(OH)2 |
0,001 |
|
14 |
CsOH |
0,005 |
29 |
CH3COOH |
0,01 |
|
15 |
HClO |
0,03 |
30 |
NH4OH |
0,025 |
