
DVS_TRP
.pdfТаблица 2.13
Формулы для определения средних мольных теплоемкостей газов при постоянном объеме, кДж/(кмоль град)
Газ |
|
Для температур газа, °С |
|
|
|
|
|
|
|
|
|
|
от 0 до 1500 |
|
|
от 1501 до 2800 |
|
|
|
|
|
||
|
|
|
|||
Воздух |
µcv = 26,600 + 0,002638 t |
µcv = 22,387 + 0,001449 t |
|||
|
|
|
|
|
|
Кислород О2 |
µc |
= 20,930 + 0,004641 t − 0,00000084 t2 |
µcv O |
2 |
= 23,723 + 0,001550 t |
|
v O2 |
|
|
|
|
Азот N2 |
µcv N2 |
= 20,398 + 0,002500 t |
µcv N2 |
= 21,951 + 0,001457 t |
|
Водород H2 |
µc |
= 20,684 + 0,000206 t + 0,000000588 t 2 |
µcv H |
2 |
= 19,678 + 0,001758 t |
|
v H2 |
|
|
|
|
Оксид углерода CO |
µcv CO = 20,597 + 0,002670 t |
µcv CO = 22,490 + 0,001430 t |
|||
|
|
|
|
|
|
Углекислый газ CO2 |
µc |
= 27,941 + 0,019 t − 0,000005487 t 2 |
µcv CO |
= 39,123 + 0,003349 t |
|
|
v CO2 |
|
|
2 |
|
Водяной пар H2O |
µcv H2O = 24,953 + 0,005359 t |
µcv H2O = 26,670 + 0,004438 t |
|||
|
|
|
|
|
|
41
или
ξz (Hu − ∆ Hu) |
+ |
[(µcv )tc |
+ γr (µcv" )tc ]tc |
= µ раб. см(µcv" ) t z t z . (2) |
M1(1 + γr ) |
|
|
||
|
|
1 + γr |
||
б) В дизелях предполагается, что сгорание происходит вначале при постоянном объеме, а затем при постоянном давлении с совершением работы и коэффициентом избытка воздуха всегда больше единицы (α > 1)
|
|
|
ξz Hu |
|
|
|
|
+ |
uc + γr uc'' |
+ R λT |
= µ |
|
(u |
'' + R T |
|
) , |
|||||||||
|
|
M1(1 + γr ) |
|
раб. см |
z |
||||||||||||||||||||
|
|
|
|
|
1 + γr |
|
|
µ |
c |
|
|
z |
µ |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
или |
|
|
|
|
|
|
[(µcv )tc + γr (µcv" ) tc ]tc |
|
|
|
|
|
|
||||||||||||
|
|
ξz Hu |
|
|
+ |
+ R λT = |
|
|
|
||||||||||||||||
|
M1(1 + γr ) |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
1 + |
γr |
|
|
|
µ |
c |
|
|
|
(3) |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
= µ |
раб. см |
[(µc" ) t z t |
z |
+ R |
(t |
z |
+ 273)]. |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
v |
|
µ |
|
|
|
|
|
|
|
|
|
|
|||||
в) Для газообразного топлива принимается условие, что сгорание происходит при постоянном объеме, коэффициент избытка воздуха может быть как больше, так и меньше единицы и с учетом приведения теплоты к килоджоуль/моль:
|
|
|
22,4 ξz (Hu − ∆ Hu) |
|
uc + γr uc'' |
'' |
|
|||||
|
|
|
|
|
|
|
|
+ |
|
= µ раб. см u z |
, |
|
|
|
|
M1(1 + γr ) |
|
|
1 + γr |
||||||
|
|
|
|
|
|
|
|
|
||||
или |
(Hu − ∆ Hu) |
|
[(µcv )tc |
+ γr (µcv" ) tc ]tc |
= µ раб. см (µcv" )t z t z . (4) |
|||||||
|
22,4 ξz |
+ |
||||||||||
|
M1 |
|
|
|
||||||||
|
(1 + γr ) |
1 + γr |
|
|
|
|||||||
В уравнениях (2) - (4):
22,4 м3/кмоль – объем киломоля любого газа; ξz – коэффициент использования теплоты, вводимый в уравнение для учета потерь теплоты, выделившейся при сгорании топлива в систему охлаждения и вследствие утечек рабочего тела через поршневые кольца, и по другим направлениям; принимается по опытным данным (табл. 2.14).
uc = (µcv )tc tc – внутренняя энергия горючей смеси (воздуха) в конце сжатия, кДж/моль;
42

u" = u пр сг = (µc" )tc t – внутренняя энергия остаточных газов в
c c . v c
конце сжатия, кДж/моль;
λ = pz / pc – степень повышения давления при сгорании; принимается по опытным данным (табл. 2.14). При расчете цикла дизеля чаще задаются значением давления pz, максимально допустимого для надежной работы двигателя;
u"z = (µcv" )t z t z – внутренняя энергия продуктов сгорания при темпера-
туре tz (условная точка окончания сгорания при расчете разомкнутого термодинамического цикла).
В уравнениях (2) и (4) неизвестными являются две величины: теплоемкость продуктов сгорания (µcv" ) t z и их температура tz. Решение этих
уравнений может выполняться методом последовательных приближений, графически или аналитически с использованием формул для определения теплоемкостей (см. табл. 2.13).
При использовании метода последовательных приближений и подстановки всех известных величин уравнение баланса энергии преобразуется к виду:
–уравнение 2
t z i |
= C |
µ раб.см(µcv" ) t z |
, |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
ξ |
z |
(Hu − ∆ Hu) |
|
(µcv ) tc + γr (µcv" ) tc |
tc |
|
|
||
где |
C = |
|
|
|
|
+ |
|
|
; |
(5) |
||
|
|
M1(1 + γr ) |
|
|
1 + γr |
|
||||||
–уравнение 3
|
|
|
" |
t |
z |
|
|
|
t z i = C |
|
(µcv ) |
|
|
, |
|||
µ раб.см |
|
|
+ R |
|||||
|
|
|
|
|
|
|
|
|
|
ξz Hu |
|
|
(µcv )tc |
+ γr (µcv" )tc tc |
|
|
|
где C = |
|
+ |
|
|
+ R λT ; |
(6) |
||
M1(1 + γr ) |
|
|
||||||
|
|
|
1 + γr |
µ |
c |
|
||
|
|
|
|
|
|
|||
–уравнение 4
t z i = C |
µ раб.см(µcv" ) t z |
, |
|
|
|
|
|
|
|
|
|
43

где C = |
22,4 ξz (Hu − ∆ Hu) |
+ |
[(µcv ) tc + γr (µcv" ) tc ]tc |
; |
(7) |
||
M1(1 + γr ) |
|
1 + γr |
|||||
|
|
|
|
||||
где i – номер приближения. |
|
|
|
|
|||
Для нулевого приближения |
задается температура |
для |
дизелей: |
||||
tz0 > 1600 ºC, а для бензиновых и газовых двигателей tz0 > 2500 ºC. Определяется теплоемкость продуктов сгорания при tz0 и вычисляется в первом приближении температура tz1 .
Процесс приближений продолжается до выполнения условия
(t zi − t z(i −1) ) t zi < 2 10−3 .
Tz = t zi + 273 .
При аналитическом решении уравнений (2) и (4) также вычисляется значение С, а в формулы (5) - (7) для вычисления теплоемкости продуктов сгорания вместо значений теплоемкостей компонентов подставляются соответствующие формулы (см. табл. 2.13). После преобразования первое уравнение приводится к виду
At z2 + Bt z + C = 0 ,
где А и В – коэффициенты, определяемые после подстановки формул для теплоемкостей.
Тогда
t z = |
− B + |
B2 + 4 A C |
|
; |
|
|
|
2 A |
Tz = t z + 273 .
Расчетное значение давления газов в конце сгорания
pzр = µ раб. см pc (Tz 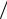 Tc ).
Tc ).
Вбензиновых двигателях действительное давление меньше, поэтому принимают pz = 0,85 pzp , а степень повышения давления при сгорании
вычисляют по формуле λ = pzр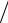 pc .
pc .
В дизелях значениями pz или λ задаются перед расчетом Tz. Неизвестное значение вычисляется по уравнению λ = pz 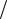 pc .
pc .
44

Степень предварительного расширения ρ = Vz' 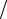 Vc , характеризующая продолжительность сгорания при p = const, определяется по формуле
Vc , характеризующая продолжительность сгорания при p = const, определяется по формуле
ρ = µ раб.см Tz 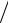 (λTc ).
(λTc ).
Средние значения параметров, характеризующих процесс сгорания, приведены в табл. 2.14. Для дизелей меньшие значения относятся к двигателям без наддува.
|
|
|
|
|
|
|
Показатели процесса сгорания |
|
Таблица 2.14 |
|||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||
Тип двигателя |
|
ξz |
|
λ |
pz, МПа |
Tz, К |
||||||
Дизель с неразде- |
|
|
|
|
|
|
|
|||||
ленной камерой |
|
0,65…0,82 |
|
1,6…2,1 |
7,0…12,0 |
|
1750…2300 |
|||||
сгорания |
|
|
|
|
|
|
|
|
|
|
||
Дизель с разделен- |
|
|
|
|
|
|
|
|||||
ной камерой |
|
|
|
0,60…0,75 |
|
1,2…1,8 |
5,5…7,5 |
|
1700…2000 |
|||
сгорания |
|
|
|
|
|
|
|
|
|
|
||
Бензиновый |
|
|
|
0,8…0,9 |
|
3,8…4,2 |
3,0…6,5 |
2500…2900 |
||||
Газовый |
|
|
|
|
0,80…0,85 |
|
3,5…4,0 |
2,5…5,5 |
2200…2500 |
|||
14. Расчет параметров процесса сгорания |
|
|
||||||||||
Б) |
|
Количество продуктов сгорания |
|
|
|
|||||||
Так |
как α = 0,96 < 1, то |
сгорание является неполным и продукты |
||||||||||
сгорания будут включать следующие компоненты: |
|
|
||||||||||
M 2 = M CO 2 + M CO + M H 2 O + M H 2 + M N 2 . |
|
|
||||||||||
Количество оксида углерода |
|
|
|
|||||||||
M |
CO |
= |
2 |
1 − α |
0,208 L , |
|
|
|
|
|
||
|
|
|
|
|
|
|||||||
|
|
1 + K |
0 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
где коэффициент К = 0,45…0,50. В данном расчете принимается К = 0,5.
M CO = 21 − 0,96 0,208 0,517 = 0,00574 кмоль. 1 + 0,5
Количество диоксида углерода
M CO |
|
= |
C |
− M CO = |
0,855 |
− 0,0057 = 0,06551 кмоль. |
2 |
|
|
||||
|
12 |
12 |
|
|||
45
Количество водорода
M |
H 2 |
= 2K |
1 − α |
0,208 L = 2 0,5 |
1 − 0,96 |
0,208 0,517 = 0,00287 кмоль. |
|||||||
|
|
||||||||||||
|
|
|
1 + K |
|
0 |
|
1 + 0,5 |
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
Количество водяного пара |
|
|
|||||||||||
M H |
|
O = |
H |
− M H |
|
= |
0,145 |
− 0,0029 = 0,06963 кмоль. |
|||||
2 |
|
2 |
|
||||||||||
|
|
2 |
|
|
|
2 |
|
|
|
||||
Количество азота |
|
|
|
|
|
||||||||
M N 2 |
= 0,792 α L0 = 0,792 0,96 0,517 = 0,39309 кмоль. |
||||||||||||
Общее количество продуктов сгорания
M 2 = 0,00574 + 0,06551 + 0,00287 + 0,06963 + 0,39309 = 0,53684 кмоль.
Объемные доли компонентов в продуктах сгорания
rCO = M CO 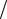 M 2 = 0,00574 / 0,53684 = 0,01069 ;
M 2 = 0,00574 / 0,53684 = 0,01069 ;
аналогично
rCO 2 = 0,06551/ 0,53684 = 0,12203 ; rH 2 = 0,00287 / 0,53684 = 0,00535 ; rH 2 O = 0,06963 / 0,53684 = 0,12970 ; rN 2 = 0,39309 / 0,53684 = 0,73223 .
Проверка ∑ ri = 0,01069 + 0,12203 + 0,00535 + 0,12970 + 0,73223 = 1.
Коэффициенты молекулярного изменения:
–горючей смеси
µ 0 = M 2 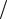 M1 = 0,53684 / 0,505 = 1,063 ;
M1 = 0,53684 / 0,505 = 1,063 ;
–рабочей смеси
µ раб.см |
= |
µ0 + γr |
|
= |
1,063 + 0,054 |
= 1,060 . |
|
|
|
|
|||||||
1 + γr |
|
|
1 + |
0,054 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Температуру продуктов сгорания Тz в конце сгорания |
определяем по |
||||||||||||||||
уравнению |
|
|
|
|
|
(µcv )tc |
+ γr (µcv" ) tc tc |
|
|
|
|
||||||
|
ξ |
z |
(Hu |
− ∆ Hu) |
|
= µ раб.cм(µcv" ) |
t |
|
|||||||||
|
|
|
|
|
|
+ |
|
|
|
|
|
|
z t z . |
||||
|
|
M1(1 + γr ) |
|
|
|
|
1 + γr |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Коэффициент использования теплоты с учетом применения распределенного впрыска топлива принимаем ξz = 0,86 (см. табл. 2.14).
Низшая теплота сгорания бензина среднего состава
Hu = 44000 кДж/кг (см. табл. 2.12).
46
Количество теплоты, потерянной вследствие химической неполноты сгорания бензина при α = 0,96
∆ Hu = 114000 (1 − α) L0 = 114000 (1 − 0,96) 0,517 = 2358 кДж/кг.
Температура в конце сжатия tc = Tc − 273 = 742 − 273 = 469 |
°C. |
||||
Мольную теплоемкость воздуха при постоянном объеме в конце сжа- |
|||||
тия определяем методом интерполирования (прил. 4 ): |
|
||||
(µcv )469 = (µcv )400 + |
(µcv )500 − (µcv )400 |
(469 − 400) = |
|
||
|
|
|
|||
|
|
|
500 − 400 |
|
|
= 21,475 + |
21,781 − 21,475 |
69 = 21,686 кДж/(кмоль °C). |
|
||
|
|
||||
100 |
|
|
|
|
|
Мольная теплоемкость остаточных газов при tc = 469 °C |
опреде- |
||||
ляется последовательным интерполированием по температуре и коэффициенту избытка воздуха (прил. 5).
При α = 0,95 |
|
|
|
(µcv" )500 − (µcv" )400 |
|
|
|
|
|||||||||||||
(µcv" )469 = (µcv" )400 + |
|
(469 − 400) = |
|||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
500 − 400 |
|
|
|
|
|||
= 23,586 + |
24,014 − 23,586 |
69 = 23,881 кДж/(кмоль °C). |
|||||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
100 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
При α = 1,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
(µcv" )469 = 23,712 + |
24,150 − 23,712 |
69 = 24,014 кмоль. |
|||||||||||||||||||
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
Аналогично интерполированием определяется теплоемкость при |
|||||||||||||||||||||
α = 0,96 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(µcv" )469 = 23,881 + |
24,014 − 23,881 |
(0,96 − 0,95) = 23,908 кмоль. |
||||||||||||||||||
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,0 − 0,95 |
|
|
|
|
|||
Значение постоянных известных величин в уравнении баланса энергии |
|||||||||||||||||||||
|
|
|
ξ |
z |
(Hu − ∆ Hu) |
|
|
(µcv ) tc + γr (µcv" ) tc |
tc |
|
|
||||||||||
C = |
|
|
|
|
|
+ |
|
|
|
|
|
|
|
= |
|
||||||
|
|
M1(1 + γr ) |
|
|
|
|
|
|
1 + γr |
|
|
|
|||||||||
= |
0,86 (44000 − 2358) |
+ |
(21,686 + 0,054 23,908) 469 |
= 77506 . |
|||||||||||||||||
|
0,505 (1 + 0,054) |
|
|
|
1 + 0,054 |
|
|
||||||||||||||
Для определения tz значения теплоемкостей продуктов сгорания представляем в виде формул (см. табл. 2.13):
47

i = n
2µcv" CO 2 t z +
i=1
+rH 2 (µcv" H 2 ) t z + rH 2 O (µcv" H 2 O ) t z + rN 2 (µcv" N 2 ) t z = 0,01069 (22,490 +
+0,00143 t z ) + 0,12203(39,123 + 0,003349 t z ) + 0,00535 (19,678 +
+0,001758t z ) + 0,1297 (26,670 + 0,004438 t z ) + 0,73223 (21,951+
+0,001457 t z ) = 24,6522 + 0,002076 t z( ) )()( )(∑
тогда
C = µ раб.см(µcv" ) t z t z ;
77506 = 1,06(24,6522 + 0,002076 t z ) t z ; 0,0022 t z2 + 26,1313 t z − 77506 = 0 ,
откуда
t z = |
− 26,1313 + |
26,13132 + 4 0,0022 77506 |
= 2458 oC ; |
|
2 0,0022 |
||
|
|
|
Tz = t z + 273 = 2458 + 273 = 2731 K .
Расчетное давление в конце сгорания (максимальное давление газа в цикле):
p |
zр |
= µ |
раб.см |
p |
|
Tz |
= 1,06 1,6750 |
2731 |
= 6,5349 МПа. |
c T |
|
||||||||
|
|
|
742 |
|
|||||
|
|
|
|
|
|
c |
|
|
|
Действительное максимальное давление в конце сгорания pz = 0,85 pzp = 0,85 6,5349 = 5,5547 МПа.
Степень повышения давления при сгорании
λ = pzp 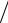 pc = 6,5349
pc = 6,5349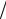 1,6750 = 3,90 .
1,6750 = 3,90 .
Полученные значения сравнить с табл. 2.14.
Д) Количество продуктов сгорания при α = 1,5
M 2 = M CO 2 + M H 2O + M O 2 + M N 2 .
Количество диоксида углерода
M CO 2 = C 12 = 0,87 12 = 0,0725 кмоль.
Количество водяного пара
M H 2 O = H 2 = 0,126 2 = 0,063 кмоль.
Количество оставшегося кислорода
48
M O 2 = 0,208 (α−1) L0 = 0,208 (1,5 −1) 0,499 = 0,0519 кмоль.
Количество азота
M N 2 = 0,792 α L0 = 0,792 1,5 0,499 = 0,5928 кмоль.
Общее количество продуктов сгорания
M 2 = 0,0725 + 0,063 + 0,0519 + 0,5928 = 0,7802 кмоль.
Объемные доли компонентов в продуктах сгорания rCO 2 = M CO 2 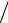 M 2 = 0,0725 / 0,7802 = 0,0929 ;
M 2 = 0,0725 / 0,7802 = 0,0929 ;
аналогично
rO 2 = 0,0519 / 0,7802 = 0,0665 ; rH 2 O = 0,063 / 0,7802 = 0,0808 ; rN 2 = 0,5928 / 0,7802 = 0,7598 .
Проверка ∑ ri = 0,0929 + 0,0808 + 0,0665 + 0,7598 = 1.
Коэффициенты молекулярного изменения:
–горючей смеси
µ 0 = M 2 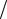 M1 = 0,7802 / 0,7485 = 1,042 ;
M1 = 0,7802 / 0,7485 = 1,042 ;
–рабочей смеси
µ |
раб.см |
= |
µ 0 + γr |
|
= |
1,042 + 0,031 |
= 1,041. |
|
|||||
|
1 + γr |
|
|
||||||||||
|
|
|
|
|
1 + 0,031 |
|
|
|
|||||
Температуру продуктов сгорания Тz в конце сгорания определяем по |
|||||||||||||
уравнению баланса энергии: |
|
|
|||||||||||
|
ξ |
z |
Hu |
|
|
(µcv )tc |
+ γr (µcv" ) tc tc |
|
|
||||
|
|
|
+ |
|
|
|
+ 8,315 λT |
= |
|||||
|
M1(1 + γr ) |
|
|
|
|
||||||||
|
|
|
|
|
1 + γr |
c |
|
||||||
= µ раб.см (µcv" ) t z t z + 8,315 Tz . |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Коэффициент использования теплоты ξz для дизеля с неразделенной камерой сгорания и объемно-пленочным смесеобразованием принимаем
ξz = 0,80 (см. табл. 2.14).
Низшая теплота сгорания дизельного топлива Нu = 42500 кДж/кг
(см. табл. 2.12).
Максимальное давление сгорания в дизелях находится в пределах рz = 7,5…12 МПа. Большие значения имеют место в дизелях с наддувом. Для рассчитываемого дизеля принимаем рz = 8 МПа.
49

Степень повышения давления при сгорании
λ = pz 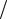 pc = 8,0 / 4,2611 = 1,877 .
pc = 8,0 / 4,2611 = 1,877 .
Температура воздуха в конце сжатия
tc = Tc − 273 = 937 − 273 = 664 oC .
Мольную теплоемкость воздуха при постоянном объеме и tс = 664 ºC определяем методом интерполяции по таблице прил. 4.
(µcv )664 = (µcv )600 + (µcv )700 − (µcv )600 64 =
700 − 600
= 22,091 + 22,409 − 22,091 64 = 22,295 кДж/(кмоль °C). 100
Мольная теплоемкость остаточных газов при tc = 664 °C и α = 1,5 (прил. 6 )
(µcv )664 = 23,819 + |
24,218 − 23,819 |
64 = 24,074 кДж/(кмоль °C). |
|
||||||
|
|
||||||||
|
|
|
|
|
700 − 600 |
|
|
|
|
Преобразуем уравнение баланса энергии, подставив в него известные |
|||||||||
величины |
|
(22,295 + 0,031 24,074) 664 |
|
|
|||||
|
0,80 42500 |
|
+ 8,315 1,877 937 |
|
|||||
|
|
+ |
|
|
= |
||||
0,7485 (1 + 0,031) |
1 + 0,031 |
||||||||
= 1,041 (µcv" ) t z t z |
+ 8,315 (t z + 273) ; |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
71159 = 8,656 t z +1,041 (µcv" ) t z |
t z . |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Это уравнение решаем методом последовательных приближений. В нулевом приближении принимаем t z0 = 1800 oC .
Первое приближение (α=1,5):
(µcv" )1800 = 27,497 кДж/(кмольºC) (прил. 6)
71159 = 8,656 t z1 + 1,041 27,497 t z1 .
t z1 = 71159 / 37,280 = 1909 oC .
Второе приближение:
(µcv )1909 = (µcv )1900 + (µcv )2000 − (µcv )1900 (1909 −1900) =
2000 −1900
50
