
- •Глава 4. Непредельные углеводороды
- •4.1. ОБщность строения и химических свойств
- •4.1.1. Реакции электрофильного присоединения
- •4.1.2. Реакции радикального присоединения
- •4.1.3. Реакции радикального замещения
- •4.1.4. Другие реакции
- •4.2. Этиленовые углеводороды
- •4.2.1. Номенклатура, изомерия
- •4.2.2. Физические свойства
- •4.2.3. Химические свойства
- •4.2.4. Способы получения
- •4.2.5. Физиологическое действие и Важнейшие представители
- •4.3. Диеновые (и полиеновые) углеводороды
- •4.3.1. Классификация, номенклатура
- •4.3.4. Особенности химического поведения диенов с изолированными двойными связями
- •4.3.5. Способы получения
- •4.3.6. Важнейшие представители
- •4.4. Ацетиленовые углеводороды
- •4.4.1. Номенклатура, изомерия
- •4.4.2. Особенности строения и свойств
- •4.4.3. Способы получения
- •4.4.4. Физиологическое действие и Важнейшие представители
- •Вопросы и упражнения
4.4.2. Особенности строения и свойств
О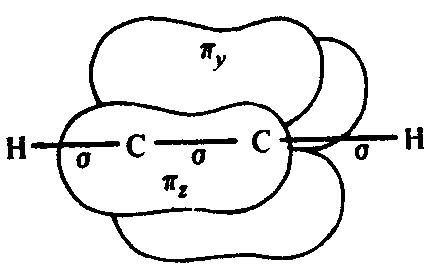 собенности
строения, отличающие ацетиленовые
углеводороды от соединений, например,
с двойными связями, связаны прежде всего
с наличием линейного фрагмента тройной
связи, её меньшей длиной и большей
поляризуемостью, чем двойная связь,
более электроотрицательными атомами
углерода вsp-гибридном
состоянии. Это объясняет более высокие
температуры кипения и плотности по
сравнению с соответствующими этиленовыми
углеводородами, а также является причиной
некоторых химических свойств, характерных
только для углеводородов с тройной
связью (например, проявление ими кислотных
свойств, способность вступать в реакции
AdN
и SE).
собенности
строения, отличающие ацетиленовые
углеводороды от соединений, например,
с двойными связями, связаны прежде всего
с наличием линейного фрагмента тройной
связи, её меньшей длиной и большей
поляризуемостью, чем двойная связь,
более электроотрицательными атомами
углерода вsp-гибридном
состоянии. Это объясняет более высокие
температуры кипения и плотности по
сравнению с соответствующими этиленовыми
углеводородами, а также является причиной
некоторых химических свойств, характерных
только для углеводородов с тройной
связью (например, проявление ими кислотных
свойств, способность вступать в реакции
AdN
и SE).
Этин (ацетилен), пропин и бутины являются бесцветными газами; углеводороды, имеющие от 5 до 15 атомов углерода, — жидкости; высшие — твёрдые вещества. Ацетилен имеет характерный резкий запах, хорошо растворяется в ацетоне.
Как и для всех непредельных углеводородов, для алкинов характерны реакции электрофильного и радикального присоединения (AdE и AdR) и радикального замещения (SR).
Реакции электрофильного присоединения
Алкины присоединяют бром, причём реакция проходит в две раздельные стадии:
R-CC-R
![]() R-CBr=CBr-R
R-CBr=CBr-R
![]() R-CBr2-CBr2-R
,
R-CBr2-CBr2-R
,
и вторая стадия, как правило, осуществляется быстрее первой, так как она представляет собой присоединение по двойной связи.
Возможно также присоединение галогеноводородов (1 или 2 молей):
R-CC-R
![]() R-CH=CBr-R
R-CH=CBr-R
![]() R-CH2-CBr2-R
R-CH2-CBr2-R
Алкины хуже протонируются, поэтому гидратацию тройных связей обычно проводят с применением в качестве катализаторов солей двухвалентной ртути (обычно сульфатов) — реакция М.Г. Кучерова*:
R-CCН
+ H2О
![]() R-CО-CH3
R-CО-CH3
Механизм реакции включает участие катиона Hg2+ на первой стадии:
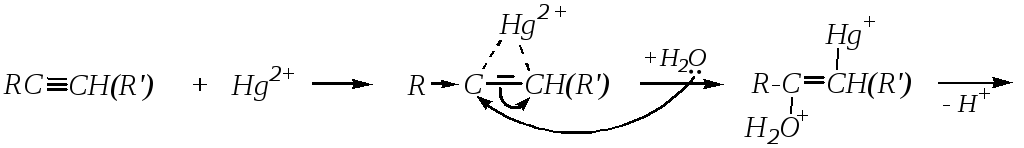

Продуктами гидратации алкинов являются кетоны (только в случае ацетилена образуется ацетальдегид). Поэтому данной реакцией можно удобно получать соответствующие карбонильные соединения.
Реакции радикального замещения
Ацетиленовые углеводороды легче должны вступать в реакции радикального замещения, чем этиленовые, вследствие более полной мезомерной стабилизации промежуточного радикала:
R-CH2-CCH + Cl R-ĊH-CCH + HCl
Кислотные свойства: металлические производные алкинов
В молекулах терминальных алкинов связь С–Н, образованная sp-гибридизованным атомом углерода, значительно полярнее, чем С–Н-связи в других углеводородах. Поэтому кислотные свойства ацетилена и его гомологов существенно сильнее выражены, чем, например, этиленовых углеводородов, и характеризуются значениями рКа 22 против рКа 40 для этиленовых. Кислотность алкинов выше и по сравнению с аммиаком, однако ниже, чем у воды и спиртов. Кислотные свойства можно проиллюстрировать реакциями со щелочными металлами, их амидами, реактивами Гриньяра:
R-СC-Н
+ Na
R-СC-Na
+
![]() H2
H2
R-СC-Н + KNH2 R-СC-K + NH3
R-СC-Н + C2Н5MgBr R-СC-MgBr + C2Н6
Образующиеся в последней реакции алкинид-галогениды магния называют реактивами Иоцича*.
В молекуле самого ацетилена могут одновременно замещаться оба атома водорода. Так, при взаимодействии с гидроксидом диамминсеребра (реактивом Толленса*) образуется ацетиленид серебра, выделяющийся в виде нерастворимого осадка:
Н-СC-Н + 2 [Ag(NH3)2]OH Ag-СC-Ag + 4 NH3 + 2 H2O
Металлические производные ацетиленовых углеводородов — солеобразные продукты. Они проявляют сильные основные свойства и при действии даже слабых кислот, например, спирта или воды, превращаются в алкины:
R-СC¯ Na+ + C2Н5OH R-СC-H + C2Н5ONa
В то же время они являются эффективными нуклеофилами и могут в этом качестве принимать участие в большинстве реакций SN и AdN. Примером таких реакций является взаимодействие нуклеофилов с галогеналканами, которое широко используется для получения алкинов из ацетилена:
R-СC¯ Na+ + C2Н5Br R-СC-C2Н5 + NaBr
(Со спиртами аналогичная реакция не может пойти, так как с ней конкурирует кислотно-основное взаимодействие, протекающее со значительно большей скоростью — см. предыдущую реакцию). Реакции нуклеофильного присоединения ацетиленидов к альдегидам и кетонам рассмотрены в главе 6.1.4.1, посвящённой свойствам этих классов соединений.
Нуклеофильное присоединение
В отличие от этиленовых углеводородов к алкинам могут присоединяться реагенты по нуклеофильному механизму. Схему реакции можно представить следующим образом:
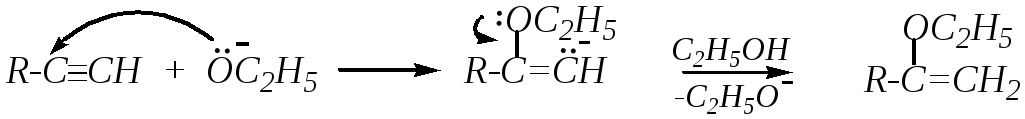
Механизм нуклеофильного присоединения включает две стадии:
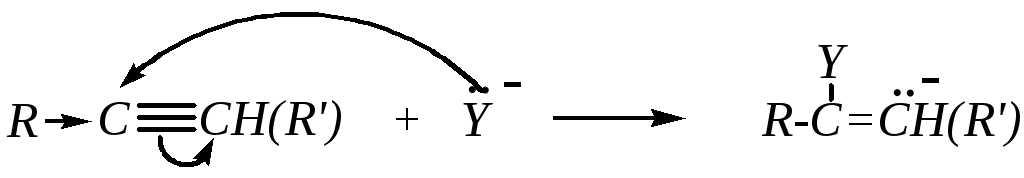
![]()
На первой стадии нуклеофил отдает свою пару электронов для образования связи с атомом углерода. -Электроны при этом смещаются к соседнему атому углерода, образуется карбанион, который далее, на второй стадии, взаимодействует с положительно заряженной частицей Х+ или с нейтральной молекулой HY, от которой может быть оторван катион Н+ (как в приведённом примере).
Бóльшая активность алкинов по отношению к нуклеофилам в сравнении с алкенами обусловлена теми же причинами, какими объясняется их меньшая реакционная способность в реакциях электрофильного присоединения (гл. 4.1.1): 1) большей локализацией -электронной плотности тройной связи, что увеличивает доступность атомов углерода для нуклеофильной атаки, 2) присоединение нуклеофила сопровождается возникновением р--сопряжённого фрагмента в карбанионе.
Тем не менее, нуклеофильная атака по ацетиленовому фрагменту протекает в жёстких условиях, и для алкинов более характерно электрофильное присоединение, а не нуклеофильное.
Электрофильное замещение
Реакции электрофильного замещения не являются наиболее характерными для ацетиленовых углеводородов, однако терминальные алкины с некоторыми реагентами могут взаимодействовать по электрофильному механизму с замещением атома водорода при тройной связи:
R-CC-Н
![]() R-CC-Br
R-CC-Br
Электрофильной частицей является поляризованная молекула брома Br+... :Br-, которая атакует алкилацетиленид-анион R-CC¯.
Подробно механизм электрофильного замещения рассмотрен в главах 9.5.1.1, 9.5.2.1, 10.1.2 на примере ароматических соединений.
Циклотримеризация (ароматизация)
Ацетилен и его гомологи в результате этой реакции превращаются в ароматические углеводороды:

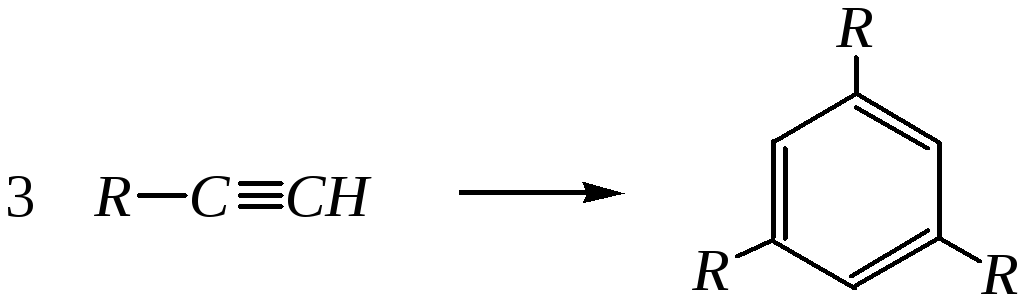
Поэтому циклотримеризация может служить способом получения этих соединений.
Однако ацетилен в эту реакцию вступает труднее, чем алкины. Для него реакция протекает в присутствии металлорганических катализаторов (соединений хрома, никеля, кобальта). Циклотримеризация алкинов осуществляется при нагревании в присутствии концентрированной H2SO4 , но легче — в присутствии соединений хрома, никеля, кобальта. Роль катализаторов заключается в активации тройной связи и пространственной ориентации алкинов в реакциях циклизации.
Взаимодействие с солями платины
Алкины, подобно алкенам, образуют различные -комплексы с металлами. При их образовании линейные молекулы алкина сильно искажаются из-за растяжения углерод-углеродной связи и приобретения цис-подобной конфигурации. Например, взаимодействие ацетилена с комплексной солью платины можно представить в виде схемы:

Таким образом, терминальные алкины можно идентифицировать химически, получая в аммиачном растворе ацетилениды меди (I) или серебра. Алкины, в отличие от алкенов, не реагируют с тетранитрометаном.
