
3 курс / Фармакология / ИК_спектроскопия_в_фармацевтическом_анализе_Мельникова_Н_Б_,_Зимнякова
.pdf
Государственное образовательное учреждение высшего профессионального образования
НИЖЕГОРОДСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
Российского федерального агентства здравоохранения и социального развития
Фармацевтический факультет
__________________________
Кафедра фармацевтической химии и фармакогнозии
Учебно–методическое пособие для студентов 5 курса фармацевтического факультета
Нижний Новгород
2006

УДК 615.1
ИК–спектроскопия в фармацевтическом анализе: Учебно-методическое пособие для студентов 5 курса фармацевтического факультета. – Нижний Новгород: Изд-во Нижегородской государственной медицинской академии, 2006.
Учебно–методическое пособие составлено для студентов 5 курса фармацевтического факультета в соответствии с программой по фармацевтической химии (Москва, 2002 г.). В пособии рассмотрены общие теоретические положения инфракрасной (ИК) спектроскопии и методы установления подлинности, доброкачественности лекарственных средств.
Рекомендовано к изданию Центральным методическим советом Нижегородской государственной медицинской академии. Протокол № 3 от 28 ноября 2005 года.
Составители: Н.Б. Мельникова, О.Е. Зимнякова, В.М. Пожидаев,
Т.В. Саликова, М.С. Гусихина.
Рецензент: профессор кафедры «Биотехнологии, физической и аналитической химии» Нижегородского государственного технического университета, д.х.н. Арбатский А.П.
© Н.Б. Мельникова, О.Е. Зимнякова, В.М. Пожидаев, Т.В. Саликова,
М.С. Гусихина, 2006.
2
СОДЕРЖАНИЕ
Введение . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4
Теоретические положения метода . . . . . . . . . . . . . . . . . . . . . . . 6
Лабораторная работа . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
Перечень приобретаемых навыков и умений . . . . . . . . . . . . . .25
Литература . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .26
Приложение 1 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27
Приложение 2 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 60
3

ВВЕДЕНИЕ
Явление взаимодействия веществ с ИК -излучением было от-
крыто У.Эбни и И.Фестингом в 1861 г. В настоящие время ИК -
спектрофотометрия стала одним из основных методов исследова-
ния веществ различной химической природы, в том число и ле-
карственных соединений.
Впервые метод стал фармакопейным с 1968 г (ГФ X), где он рекомендовался для контроля качества трех лекарственных ве-
ществ: фторотана, оксациллина и метициллина натриевых солей,
а в разделе "Общие методы физико-химического, химического и биологического исследования" фармакопеи помещен материал,
касающийся некоторых практических вопросов ИК-
спектрофотометрии. Со времени выхода 10-го издания фармако-
пеи число препаратов, при исследовании которых рекомендуется метод, значительно выросло, что можно проследить на примере дополнений к фармакопее, издаваемых ежегодно, и отдельно вы-
пускаемых фармакопейных статьях. Наряду с ультрафиолетовой ИК -спектрофотометрия включена во все современные фармако-
пеи. Так, Международная фармакопея (Женева, 1990 г) рекомен-
дует этот метод практически в анализе половины описанных в ней лекарственных веществ. Получать ИК-спектры можно не только для субстанций, но и в ряде случаев для готовых препара-
тов. Для этого необходимо, чтобы вспомогательные вещества,
входящие в состав препарата (например, таблеток), не подавляли спектр действующего вещества. Это условие обычно выполняет-
ся, если процентное содержание вспомогательных веществ не
4
слишком велико - обычно менее 60—70%. ИК-
спектрофотометрия является обязательным методом контроля веществ - стандартных образцов, кроме того, она в настоящее время включается в ФС на многие лекарственные вещества.
Метод используется в фармакопейном анализе для доказа-
тельства отличия лекарственных веществ близкого химического строения (одного ряда). Например, в ФС на эстоцин-препарат из группы эфиров арилалифатических кислот требуется, чтобы в ИК-спектре, снятом в вазелиновом масле, отсутствовала характе-
ристическая полоса поглощения свободной гидроксильной груп-
пы в области 3300-3500 см-1 (отличие от амизила и метацина).
Примеси проявляются в появлении "лишних" полос, измене-
ние формы, интенсивности и резкости отдельных полос.
Направления практического применения
ИК-спектрофотометрии в фармацевтическом анализе
ИК-спектрофотометрия используется:
при установлении структуры новых БАВ получаемых путем химического синтеза или выделяемых из природных объектов
(животное или растительное сырье, продукты жизнедеятельности микроорганизмов); изучении строения метаболитов;
при испытании на подлинность лекарственных веществ;
определении доброкачественности лекарственных соединений;
количественном анализе;
контроле технологического процесса в промышленном про-
изводстве фармпрепаратов (полнота протекания).
5

ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ МЕТОДА
ИК-спектрофотометрия - метод исследования веществ, ос-
нованный на поглощении ИКизлучения, в результате чего про-
исходит усиление колебательных и вращательных движений мо-
лекул. Большее проявление имеют колебательные движения, по-
этому ИКспектры, называются колебательными (или молеку-
лярными).
Атомы в молекулах никогда не находятся в состоянии покоя,
а колеблются относительно каких-то средних положений, отчего расположение их относительно друг друга периодически изменя-
ется. ИК-излучение усиливает эти колебания, при этом часть энергии излучения теряется. Фиксируется ослабление прошедшего ИК-излучения. (J)=J0-Jпотери как функция длины волны (так же, как в электронных спектрах).
Энергия, необходимая для возбуждения колебаний атомов в молекуле, соответствует энергии квантов света с длиной волны 1-
15 мкм или волновым числом 400-4000 см-1, т.е. электромагнит-
ному излучению средней инфракрасной области. Области примы-
кающие к ней называются ближней инфракрасной от 12500-4000
см-1 и дальней инфракрасной от 625-50 см-1. Слова ближний и дальний характеризуют близость к области видимого света.
Колебательные уровни молекул квантованы, энергия перехо-
дов между ними и, следовательно, частоты колебаний могут иметь только строго определенные значения. Поглощая квант света, молекула может переходить на более высокий колебатель-
6
ный уровень, обычно из основного колебательного состояния в возбужденное.
Поглощение инфракрасного излучения вызывают колебания связанные с изменением либо длин связи, либо углов между свя-
зями. Это означает, что в зависимости от частоты поглощенного излучения начинает периодически растягиваться определенная связь или искажаться определенный угол между связями.
Таким образом, основными типами колебаний являются так называемые валентные и деформационные колебания.
Колебания, заключающиеся в изменении длины связи между связанными атомами и не сопровождающиеся отклонением от межъядерной оси, называются валентными, т.о. валентными ко-
лебаниями называются колебания ядер атомов вдоль линии связи,
они обозначаются буквой ν (ν С=С, ν С=О).
Валентные колебания располагаются в области больших час-
тот 4000-1400 см-1, деформационные - в области низких < 1400
см-1. В зависимости от природы колебания подразделяются на скелетные (800-1500 см-1) и колебания групп (>1500 см-1).
Наряду с указанными основными в спектре наблюдаются обертоны, полосы резонансного взаимодействия, составные поло-
сы, возникающие в результате взаимодействия полос поглощения отдельных атомов.
Колебательными спектрами обладают не все молекулы, а
только те, у которых при колебании происходит изменение ее ди-
польного момента. Например, HCI, H2O, но не Cl2, N2, O2, и т.д.
7

Приближенной механической моделью валентных колебаний может служить система из двух шаров, связанных пружиной (ша-
ры изображают атомы, а пружина - химическую связь). При рас-
тяжении или сжатии пружины шары начнут колебаться вокруг положения равновесия, т.е. будет осуществляться гармоническое колебание, описываемое уравнением
|
1 |
|
F |
|
|
|
|
, где |
|
2 |
|
|
||
|
|
|
||
|
|
mr |
||
ν- частота колебания;
F - силовая постоянная; характеризующая прочность связи,
или силу, возвращающую шары в положение равновесия;
mr - приведенная масса атомов, вычисляемая по формулам:
m m
mr m1 m2 , где
1 2
m1 и m2 – массы атомов.
валентные колебания могут быть симметричными (νs ), если обе связи одновременно удлиняются или укорачиваются и пары
атомов одновременно приближаются и отделяются;
m1 
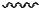 m2 m1
m2 m1 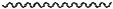
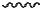 m2
m2
и антисимметричными, если одна из связей укорачивается, а
другая - удлиняется (νаs ), этом случае приближение и отдаление разных пар атомов происходит не одновременно
8
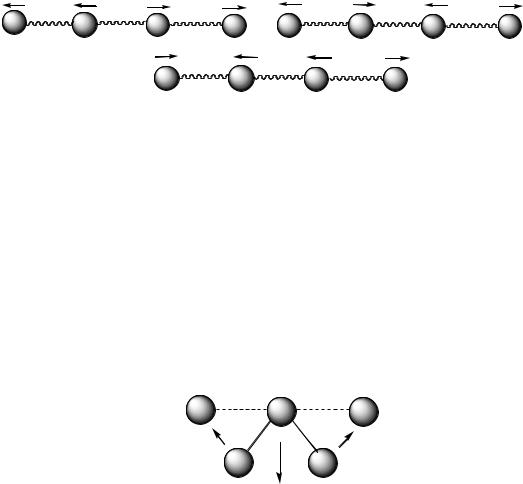
Частота антисимметричного колебания всегда выше, чем симметричного.
Следующим типом колебаний являются деформационные,
которые связаны с изменением валентного угла, образованного связями у общего атома, т.е. колебания, при которых атомы сме-
щаются с межъядерной оси, они обозначаются буквой δ.
Для возбуждения деформационных колебаний требуется меньшая энергия, чем в случае валентных колебаний и, следова-
тельно, они имеют меньшую частоту. С увеличением числа ато-
мов в молекуле число возможных колебаний быстро растет. В ре-
альной молекуле колебания атомов тесно связаны друг с другом и взаимодействуют между собой.
Спектры молекул представляют собой сложный набор раз-
личных колебаний, каждое из которых проявляется в узком ин-
тервале частот. Общее число линий (полос поглощения) в спек-
тре, связанных с колебаниями атомов, определяется для нелиней-
ной молекулы формулой 3N - 6 основных колебаний и 3N - 5 для линейной молекулы, где N- число атомов в молекуле. Фактически
9

число полос в спектре не всегда равно этому числу. Оно может уменьшаться вследствие того, что часть полос не проявляется в ИК-спектре, что связано со степенью симметрии молекулы.
Уменьшение числа полос происходит из-за того, что для доста-
точно симметричных молекул различные колебания могут иметь одинаковые частоты и в результате этого в спектре проявляется вместо 2-3 лишь одна полоса.
Интенсивность поглощения в ИК-спектрофотометрии обычно выражают как поглощение (Д) или чаще как пропускание (Т) све-
тового потока в процентах
T ,% J 100
J 0
Полосы также оцениваются ориентировочно как сильные (с),
средние (ср) и слабые (сл).
При изучении взаимодействия с ИКизлучением веществ различного химического строения (модельные соединения) было установлено, что многие атомные группы такие как -ОН, - NH2, -NO, >СО, а также определенные связи, такие как С-Н, С-С, С=С,
С=О, характеризуются определенными частотами, мало отли-
чающимися в различных соединениях. Такие частоты получили название характеристических или групповых частот. Они обозна-
чаются греческой буквой ν и для основных классов органических соединений приведены в табл.1-5.(приложение 2)
Частота валентных колебаний определяется массой атомов и прочностью (энергией) связи. Чем больше масса, тем меньше час-
тота, например
10
