
2 курс / Нормальная физиология / Гемостаз_Физиологические_механизмы,_принципы_диагностики_основных
.pdf
время (протромбиновый индекс) Тромбиновое время Концентрация фибриногена
Тест растворимости фибринового сгустка в мочевине (активность фактора
XIII)
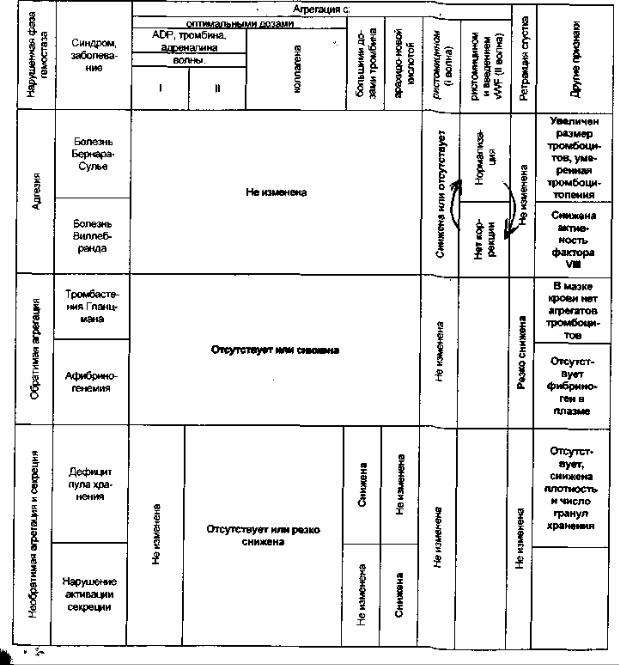
Алгоритм диагностики нарушений тромбоцитарного звена гемостаза
Геморрагические проявления при врожденной или приобретенной недостаточности тромбоцитарного звена гемостаза обусловлены тем, что имеются нарушения на той или иной ступени последовательно развивающихся гемостатических реакций: адгезии, агрегации, секреции кровяных пластинок и ретракции гемостатической пробки. С целью установления недостаточности функциональной активности тромбоцитов и определения ее характера исследование состояния тромбоцитарного гемостаза проводится в три этапа (табл.9). На I этапе, который доступен для применения в широкой медицинской практике, устанавливают факт нарушения в этом звене гемостаза. На II этапе, который проводят в биохимических лабораториях клиник и стационаров, определяют фазу тромбоцитарных реакций, где проявляется недостаточность. И, наконец, на III этапе в высокоспециализированных лабораториях могут быть установлены структурно-биохимические дефекты, лежащие в основе выявленных функциональных нарушений.
Таблица 9
Этапы обследования больных с нарушениями тромбоцитарного звена гемостаза (без значительного изменения числа тромбоцитов)
I. |
Установление |
факта |
1. |
Определение |
типа кровоточивости - |
нарушения |
в |
капиллярный, «смешанный» |
|||
тромбоцитарном |
звене |
2. |
Число тромбоцитов - чаще не изменено или |
||
гемостаза |
|
умеренно снижено |
|
||
|
|
|
3. |
Длительность |
кровотечения - обычно |
|
|
|
увеличена |
|
|
|
|
|
4. |
Адгезивно-афегационный (ретенционный) |
|
|
|
|
тест -результаты снижены |
||
II. |
Установление |
типа |
Оценка функциональных свойств тромбоцитов |
||
нарушения: |
|
|
|
|
|
II. Определение структурно-биохимического дефекта
Вид исследования |
Заболевание/синдром, |
при |
|||
|
|
котором |
данное |
исследование |
|
|
|
необходимо или желательно: |
|
||
Оценка |
распределения |
Болезнь |
Бернара-Сулье, |
||
тромбоцитов по размеру, объему, |
дефицит пула хранения |
|
|||
плотности |
|
|
|
|
|
Исследование |
морфологии |
Тромбастения, |
дефицит |
пула |
|
тромбоцитов, |
определение |
хранения, болезнь Бернара-Сулье |
|||
содержания и плотности гранул |
|
|
|
|
|
хранения |
|
|
|
|
|
Оценка |
изменений |
Тромбастения, |
нарушение |
||
ультраструктурных |
элементов |
активации секреции |
|
|
|
тромбоцитов после их активации |
|
|
|
|
|
Оценка |
|
|
|
процесса |
Болезнь |
Бернара-Сулье, |
|||
распластывания |
тромбоцитов |
на |
тромбасте-ния |
|
|
||||
поверхности стекла |
|
|
|
|
|
|
|||
Оценка |
|
|
|
адгезии, |
Болезнь |
Бернара-Сулье, |
|||
распластывания |
и |
|
агрегации |
болезнь Виллебранда, Тромбастения, |
|||||
тромбоцитов |
на |
субэндотелии |
тромбоцитопатия высвобождения |
||||||
препаратов артерий человека, аорты |
|
|
|
||||||
кролика |
|
|
|
|
|
|
|
|
|
Определение |
содержимого |
Дефицит |
пула |
хранения, |
|||||
гранул |
хранения |
после активации |
нарушение активации секреции |
||||||
тромбоцитов или их разрушения, а |
|
|
|
||||||
также |
высвобождения |
его |
в |
|
|
|
|||
супернатант |
|
|
|
|
|
|
|
|
|
Исследование пула хранения и |
Дефицит |
пула |
хранения, |
||||||
метаболического |
пула |
адениновых |
нарушение активации секреции |
||||||
нуклеотидов |
|
|
|
|
|
|
|
|
|
Определение гликопротеинов |
Болезнь |
Бернара-Сулье, |
|||||||
мембраны тромбоцитов |
|
|
|
тромбасте-ния |
|
|
|||
Определение |
|
уровня, |
Болезнь Виллебранда |
||||||
мультимерного |
состава |
и |
|
|
|
||||
функциональной активности фактора |
|
|
|
||||||
Виллебран-да |
|
в |
плазме |
и |
|
|
|
||
тромбоцитах |
|
|
|
|
|
|
|
|
|
Исследование ферментативной |
Тромбастения, |
нарушение |
|||||||
активности |
тромбоцитов, |
прежде |
активации секреции |
|
|||||
всего |
тромбаксан-генерирующей |
|
|
|
|||||
системы, сАМР и энергетического |
|
|
|
||||||
метаболизма |
|
|
|
|
|
|
|
|
|
Определение |
|
конечных |
Нарушение |
|
активации |
||||
продуктов (или реакции) активации |
секреции |
|
|
||||||
тромбоксан-генерирующей |
системы |
|
|
|
|||||
после |
действия |
различных |
|
|
|
||||
активаторов и аналогов агонистов |
|
|
|
|
|||||
Определение |
мобилизации |
Нарушение |
|
активации |
|||||
внутриклеточного Са2* |
|
|
|
секреции |
|
|
|||
I этап осуществляется на основании анализа анамнестических сведений и данных осмотра больного, позволяющих установить капиллярный или "смешанный" тип кровоточивости, а также посредством применения ориентировочных, скрининговых, тестов первичного гемостаза. К ним относятся определение первичной длительности кровотечения, числа тромбоцитов и их адгезивно-агрегационной активности в ретенцион-ном тесте. Совокупность результатов исследования скрининговых тестов позволяет дифференцировать количественные нарушения, обусловленные
выраженным изменением числа тромбоцитов, и качественные, связанные с недостаточностью функциональной активности кровяных пластинок. На этом этапе могут быть получены следующие варианты результатов исследования.
Если у больного число тромбоцитов снижено, то, очевидно, основная причина нарушений тромбоцитарного аппарата связана с количественными изменениями, и дальнейшее гематологическое обследование должно быть направлено, прежде всего, на выявление причины этих отклонений. Необходимо установить, связана ли тромбоцитопения с нарушением процесса кроветворения, с повышенным разрушением или потреблением кровяных пластинок. Но и при очевидной количественной патологии определение функциональной активности тромбоцитов может быть целесообразным, так как существует ряд тромбоцитопатий, для которых характерна та или иная степень снижения содержания тромбоцитов. С другой стороны, при тромбоцитопении сопутствующие изменения функциональной способности кровяных пластинок могут усугублять недостаточность гемостаза, обусловленную количественным дефектом. Так, у некоторых больных с умеренной ^степенью тромбоцитопении (число тромбоцитов более 100хЮ9/л) исследование функции тромбоцитов может объяснить причину развития геморрагии и увеличение первичной длительности кровотечения. Реже повышение функциональной активности кровяных пластинок способствует определенной компенсации гемостатических нарушений.
При значительном увеличении числа тромбоцитов необходимо также провести целенаправленное клиническое обследование больного для установления причины этого явления. Злокачественные новообразования, хронические воспалительные процессы, железодефицитная анемия могут явиться причиной реактивного тромбоцитоза. Хронические миелопролиферативные процессы (хронический миелолейкоз, миелофиброз, эссенциальная полицитемия) могут осложняться тромбоцитемией. Эссенциальная тромбоцитемия также является проявлением гемобластоза. В неясных случаях исследование функциональной активности тромбоцитов в комплексе с другими клиническими методами может помочь проведению дифференциального диагноза - при тромбоцитозе почти не бывает нарушения функции кровяных пластинок, в то время как при тробоци-темии оно закономерно.
Проявления кровоточивости по капиллярному типу, увеличенная первичная длительность кровотечения при нормальном числе тромбоцитов в периферической крови указывают на наличие у обследуемого больного функциональных изменений в сосудисто-тромбоцитарном звене гемостаза и на необходимость выполнения всех анализирующих тестов второго этапа.
Следует отметить, что встречаются и другие более редкие варианты результатов первоначального исследования сосудисто-тромбоцитарного звена гемостаза. Так, у больного с геморрагическими проявлениями капиллярного типа могут быть получены нормальные значения длительности кровотечения и числа тромбоцитов. Нужно ли проводить исследования
дальше? Результаты скрининговых тестов как будто бы указывают на то, что нарушений в сосудисто-тромбоцитарном звене гемостаза нет. Тем не менее, формальная логика не применима в данном случае, так как общие тесты, оценивающие определенную сумму реакций, являются мало чувствительными. В связи с этим при незначительных степенях нарушения первичного гемостаза вследствие компенсаторных влияний отклонения в общих тестах могут отсутствовать. Следует помнить также, что наличие геморрагии капиллярного типа - это объективный факт, диктующий необходимость соответствующего обследования. Вопрос о том, нужно ли его продолжать после получения отрицательных данных первых отборочных тестов, должен решаться различно в зависимости от тяжести геморрагии и от наличия данных, указывающих на системное нарушение гемостаза. Необходимо отметить, что легкое возникновение мелких синяков на коже у некоторых детей и женщин может наблюдаться без изменений в системе гемостаза. Поэтому, если геморрагические проявления небольшие, локальные, появились недавно, и в клинической картине заболевания нет указаний на возможность врожденного заболевания, то в таком случае отрицательные данные общих, отборочных, тестов позволяют временно прекратить дальнейшее исследование. Но при этом нужно предупредить больного о необходимости повторного лабораторного контроля при возобновлении кровоточивости или перед возможной хирургической операцией. Если геморрагические проявления значительные или распространенные, если имеются анамнестические данные о системном нарушении гемостаза, если больному предстоит операция, то лабораторное исследование в этой ситуации должно быть продолжено.
После установления факта нарушения в тромбоцитарном звене гемостаза следует приступить ко II этапу обследования с целью определения характера тромбоцитопатии. Исследования на этом этапе проводятся так, чтобы с помощью относительно простых, но клинически значимых тестов оценить функцию тромбоцитов во всех фазах первичного гемостаза, выявить основной определяющий дефект или характерное сочетание изменений. Анализ результатов минимального набора методов позволяет дифференцировать основные формы нарушений тромбо-цитарного гемостаза, обусловленные как собственно тромбоцитарным дефектом, так и недостаточностью плазменных кофакторов первичного гемостаза.
Нарушение в фазе адгезии устанавливают на основании отсутствия или резкого снижения первой волны агрегации с ристомицином (ристоцетином). Если этот дефект корригируется добавлением фактора Виллебранда, содержащегося в бестромбоцитной плазме здоровых лиц, то можно считать, что недостаточность тромбоцитарного гемостаза, которая проявилась в геморрагиях и удлинении первичного времени кровотечения, обусловлена нарушением синтеза плазменного кофактора адгезии - фактора Виллебранда, что наблюдается, прежде всего, при болезни Виллебранда. Если подобной коррекции нет, то это свидетельствует, что нарушение взаимодействия тромбоцитов и фактора Виллебранда в присутствии
ристомицина связано с собственно тромбоцитарным дефектом - с отсутствием на мембране этих клеток гликопротеинового рецептора для фактора Виллебранда (GPIb), т.е. в данном случае следует думать о болезни Бернара-Сулье. Первое предположение о болезни Виллебранда подтверждается сочетанием выявленного дефекта в фазе адгезии со снижением коагуляционной активности фактора VIII, поскольку фактор Виллебранда является носителем молекулы фактора VIII и защищает последний от разрушения и элиминации в циркулирующей крови. Во втором случае болезнь Бернара-Сулье подтверждается, прежде всего, обнаружением
вмазке крови гигантских тромбоцитов. Обычно у этих больных имеется и умеренная тромбоцитопения.
Онарушении в фазе первичной агрегации при фотометрической оценке этого процесса свидетельствует резкое снижение или даже отсутствие и первой, и второй волн агрегации с оптимальными дозами ADP и других агрегирующих агентов, а также единственной волны агрегации с умеренными дозами коллагена. Такой тип изменений характерен для врожденной тромбастении Гланцмана, при которой в мембране тромбоцитов нет необходимых для развития агрегации гликопротеинов IIb-IIIa (GPIIb-IIa). Следует обратить внимание на то, что при отсутствии рецептора для фибриногена (GPIIb-IIIa) нарушена также и вторичная агрегация, поскольку и для нее необходимо образование фибриногеновых соединений между этими гликопротеиновыми рецепторами тромбоцитов.
Нарушение механизма агрегации может быть связано также с отсутствием плазменного компонента, необходимого для формирующихся при агрегации межтромбоцитарных связей, то есть самого фибриногена, а не мест фиксации на плазматической мембране фибриногеновых молекул. Это приводит к сходной с тромбастенией картине агрегационных изменений, которые, однако, легко отличить на основании коагуляционных исследований, устанавливающих афибриногенемию. Для обеих форм патологии, связанных как с собственно тромбоцитарным дефектом - тромбастенией, так и отсутствием плазменного кофактора агрегации - афибриногенемией, характерна выраженная недостаточность ретракции, так как нарушено формирование непрерывных тромбоцитарно-фибриновых структур, в которых сокращение актомиозина кровяных пластинок приводит к сокращению всей системы в целом только в случае сохранности всех ее компонентов (т.е.СРПЬ - IIia или фибриногена, соответственно). Понятно, что при афибриногенемии все отклонения тром-боцитарных тестов корригируются in vitro добавлением фибриногена.
Выявление третьей основной группы патологии тромбоцитарного гемостаза, в основе которой лежит недостаточность секреторного процесса,
вклинических условиях проводится обычно на основании характерного отсутствия (или резкого снижения) второй волны агрегации с оптимальными дозами всех агрегирующих агентов и единственной волны агрегации с коллагеном. При графической регистрации агрегации именно эти феномены являются результатом секреции из тромбоцитов эндогенных агрегирующих
агентов. В отличие от предыдущей группы нарушений агрегации, при рассматриваемых тромбоцитопатиях высвобождения первая волна агрегации не изменена. Дифференцировать две основные подгруппы тромбоцитопатий высвобождения, обусловленных дефицитом гранул хранения или нарушениями в механизмах активации секреторного процесса, в известной степени можно на основании оценки агрегации с арахидоновой кислотой и большими дозами тромбина. Агрегация с арахидоновой кислотой не изменена при дефиците/дефекте гранул хранения и отсутствует при многих вариантах второй подгруппы тромбоцитопатий высвобождения. Противоположные результаты получают при использовании больших доз тромбина. Здесь агрегация отсутствует при дефиците пула хранения и может развиваться при функциональной тромбоцитопатий высвобождения, обусловленной в основном недостаточностью ферментов простагландинтромбоксанового пути активации, поскольку большие дозы тромбина стимулируют пластинки по фосфои-нозитидному пути. Более точное определение вариантных форм этой большой группы тромбоцитопатий требует использования сложных биохимических и морфологических методов
(табл.9, III).
Почти при всех вышеописанных формах тромбоцитопатий вторично нарушается и коагуляционная активность тромбоцитов. Это объясняется тем, что мембранная перестройка, приводящая к развитию коагуляцион-ной активности тромбоцитов, индуцируется как в период адгезивноагрегационных реакций, так и в период секреции. Изолированное врожденное нарушение содержания и доступности тромбоцитарного фактора 3 описано у единичных больных. Как правило, эта коагуляционная недостаточность связана с изменениями в других фазах тромбоцитарных превращений.
Алгоритм диагностики нарушений плазменно-коагуляционного звена гемостаза
У больного с коагуляционным типом кровоточивости должен быть установлен характер плазменного дефекта, что обычно проводится с помощью методов, определяющих активность каждого фактора свертывания крови. Такой способ диагностики является оптимальным, но он может быть осуществлен в настоящее время только в специализированных лабораториях по исследованию гемостаза, поскольку требует использование дорогостоящих плазм с изолированным дефицитом различных факторов свертывания крови. Однако диагноз коагулопатии может быть поставлен и в обычной лаборатории, исследующей процессы свертывания крови, на основании последовательного анализа широко распространенных коагуляционных методов. Но при этом необходимо принять во внимание, что анализ результатов проведенных исследований и установление диагноза не возможны без четкого представления о взаимодействии факторов в сложном процессе свертывания крови.
Напомним, что первая стадия свертывания крови - образование протромбиназы, может осуществляться пек внутреннему или по внешнему пути, которые различаются только по характеру реакций, непосредственно предшествующих активации фактора X.
Первая группа реакций, известная как внутренний путь, включает в себя взаимодействие факторов XII, XI, IX, VIII, V, X и фосфолипидов кровяных пластинок, которое завершается образованием протромбиназы. Внутренний путь свертывания крови характеризуют следующие тесты: время свертывания венозной крови, время рекальцификации плазмы, каолиновое время свертывания и активированное парциальное (частичное) тромбопластиновое время (АПТВ). Особо следует подчеркнуть, что определение времени свертывания капиллярной крови не может быть использовано для характеристики внутреннего пути, поскольку техника этого исследования не исключает попадания в исследуемые образцы крови тканевого тромбопластина.
Вторая группа реакций - это взаимодействие факторов VII, X, V и тканевого тромбопластина, обозначается как внешний путь, так как для активации фактора X и соответственно для образования протромбиназы по этому пути помимо плазменных факторов (VII, X, V), необходим внешний для крови компонент тканевый тромбопластин. Наиболее распространенным методом, оценивающим внешнюю систему свертывания крови, является тест одноступенчатого протромбинового времени (протромбиновый индекс).
Третья группа реакций характеризуется тем, что образующаяся в ре- ;зультате активации факторов внутренней и внешней системы протром- ;биназа (комплекс факторов Ха, Va и фосфолипидов) превращает про- ?тромбин (фактор II) в тромбин (На), и далее под действием тромбина | происходит переход фибриногена в плотный и видимый фибриновый сгусток. К методам изучения процесса превращения фибриногена в фибрин относятся определение тромбинового времени, концентрации фибриногена и растворимости фибринового сгустка в мочевине. Последний тест позволяет судить об активности фактора XIII. Подобная систематизация методов имеет большое практическое значение, поскольку сопоставление результатов исследования в перечисленных тестах с учетом особенностей течения коагуляционных реакций в каждой тест системе позволяет диагностировать основные формы коагулопатий.
Анализ данных лабораторного исследования в указанном объеме рекомендуется проводить следующим образом. Сначала оцениваются результаты тестов первой группы, характеризующих внутренний путь свертывания крови. Удлинение времени свертывания венозной крови, времени рекальцификации плазмы, каолинового времени свертывания и АПТВ, то есть нарушение первой группы тестов, прежде всего, является доказательством изменения факторов, принимающих участие во внутреннем пути активации свертывания крови, а именно: XII, XI, IX, VIII, X или V. Следует помнить, что на показателях этих тестов могут отразиться и снижение содержания фибриногена, и повышение антикоагулянтной
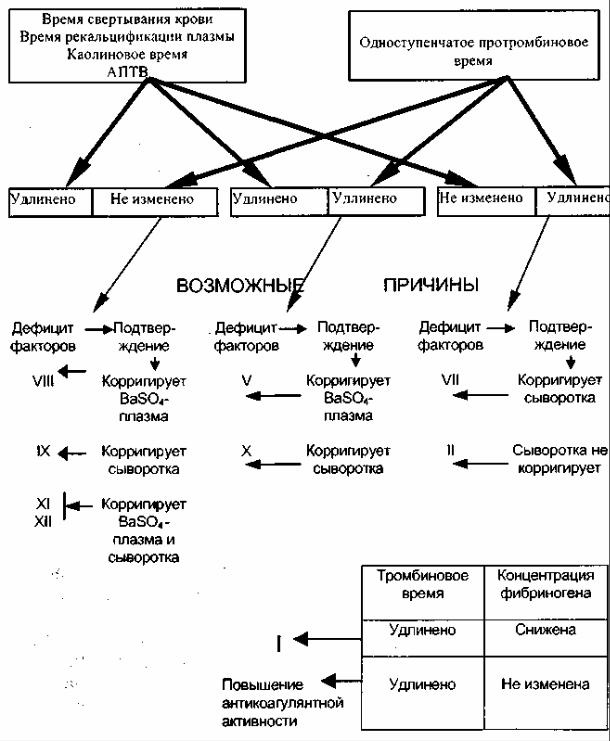
активности крови. Однако для того, чтобы нарушились значения тестов данной группы, степень изменений последних двух показателей должна быть существенной, что на практике встречается крайне редко. Кроме того, указанные изменения показателей фибриногена и антикоагулянтной активности крови всегда сопровождаются удлинением тромбинового времени и не наблюдаются при дефиците любого из факторов внутренней системы активации фактора Ха.
Рис.15. Алгоритм диагностики врожденных коагулопатий
Среди факторов внутреннего пути необходимо выделить две подгруппы. Одна из них - это факторы XII, XI, IX, VIII, участие которых ограничивается исключительно внутренним путем; вторая включает факторы X и V, которые являются общими и для внутреннего, и внешнего пути активации свертывания крови. Из этого следует, что для коагулопатий вследствие дефицита факторов XII, XI, IX, VIII характерным лабораторным признаком будет изолированное нарушение показателей тестов первой группы, оценивающих только внутренний путь свертывания крови. Поскольку ни один из перечисленных факторов (XII, XI, IX, VIII) не принимает участия в активации свертывания крови по внешнему пути, при недостаточности любого из них одноступенчатое протромбиновое время (вторая группа методов) всегда будет в пределах нормы, равно как и показатели тромбинового времени и концентрации фибриногена. Но показатели активности фактора XIII (фибринстабилизирующего фактора), оцениваемой по растворимости фибринового сгустка в мочевине, при этих состояниях могут быть снижены. В основном это наблюдается при гемофилии (дефиците факторов VIII, IX) и объясняется тем, что время, затрачиваемое на получение фибринового сгустка в указанном тесте (20 мин), недостаточно для полного превращения фибриногена в фибрин. В этих случаях повышенная растворимость фибринового сгустка в мочевине обусловлена не снижением активности фактора XIII, а неполноценностью сгустка фибрина вследствие коагулопатий.
Иную лабораторную характеристику имеют коагулопатий из-за дефицита второй подгруппы факторов внутренней активации - X и V. Эти факторы необходимы для осуществления как внутреннего, так и внешнего пути активации свертывания крови. Поэтому при коагулопатиях, обусловленных нарушением их синтеза, наряду с патологическими показателями тестов, характеризующих внутренний путь свертывания крови, у больных выявляется и удлинение протромбинового времени (снижение протромбинового индекса), свидетельствующее о нарушении внешнего пути активации свертывания крови.
Для осуществления второй группы реакций, а именно активации свертывания крови по внешнему пути, наряду с факторами X и V, требуется также присутствие фактора VII и тканевого тромбопластина. Фактор VII, в отличие от факторов X и V, не принимает участия во внутреннем пути активации коагуляции. В связи с этим у больных гипоконверти-немией (дефицит фактора VII) показатели тестов, используемых для характеристики процесса внутренней активации свертывания крови, находятся в пределах нормы, в то время как показатель, оценивающий внешний путь коагуляции (протромбиновый индекс), всегда нарушен.
Изолированное удлинение протромбинового времени (снижение протромбинового индекса) характерно не только для коагулопатии вследствие нарушения синтеза фактора VII, но и для редкой формы врожденного геморрагического диатеза, обусловленной недостаточностью протромбина (фактора II). Если принять во внимание факт, что протромбин
