
Судьба α-кетокислот
Образовавшиеся в процессе дезаминирования и переамини- рования α-кетокислоты могут использоваться в тканях организма с
различными целями. Они могут подвергаться:
1)Восстановительному аминированию и переаминированию с образованием соответствующей аминокислоты.
2)Декарбоксилированию с превращением в жирные кислоты, при β-окислении которых образуется ацетил - КоА, сгорающий в
цикле трикарбоновых кислот с образованием энергии.
3)Превращению в углеводы, включаясь в процесс глюконеогенеза через пируват, α-кетоглутарат, щавелевоуксусную кислоту, сукцинил - КоА, при этом пируват является центральным
связующим звеном. В пируват превращаются аланин, серин, глицин, треонин, цистеин, в ЩУК - аспартат, аспарагин, в α-кетоглутарат - глутамин, в сукцинил- КоА - валин, изолейцин, метионин, треонин.
Эти аминокислоты называют гликогенными или гликопластическими. Глюконеогенез с участием аминокислот особенно активно происходит при голодании, при преимущественно белковом питании. Полагают, что примерно 50% аминокислот в организме могут служить источником для образования глюкозы.
4)Превращениям с образованием ацетоуксусной кислоты и ацетил-КоА (фенилаланин, тирозин, лейцин, лизин), из которых
образуются жирные кислоты и кетоновые тела. Поэтому их называют кетогенными или кетопластическими.
В то же время такие аминокислоты как тирозин, фенилаланин, триптофан и изолейцин являются одновременно и гликогенными и кетогенными, так как часть их молекул при катаболизме превращается
впируват, а другая часть включается в ацетил-КоА.
Лекция 24
ОБЕЗВРЕЖИВАНИЕ АММИАКА В ОРГАНИЗМЕ
Обезвреживание аммиака в организме
Аминокислоты, не использованные для построения тканевых белков или биологически активных веществ, подвергаются распаду с образованием конечных продуктов – СО2, Н2О и NН3.
Образование NН3 происходит во всех тканях в результате:
1.Окислительного дезаминирования аминокислот.
2.Окислительного дезаминирования глутаминовой кислоты.
242
3.Дезаминирования аминов аминооксидазами.
4.Дезаминирования пуриновых и пиримидиновых нуклеотидов.
5.Дезаминирования аминокислот ферментами бактерий в ки-
шечнике с последующим всасыванием этого NН3 в портальную вену.
В сутки в организме подвергаются распаду до 70 г аминокислот,
врезультате чего образуется большое количество NН3. Аммиак для
клеток является ядом, и его накопление в тканях представляло бы серьезную угрозу для организма. При попадании больших количеств аммиака в кровь (цирроз печени) развивается интоксикация, проявляющаяся, прежде всего, поражением центральной нервной системы (затруднение речи, тремор, потеря сознания, эпилептические припадки, кома). Несмотря на непрерывное образование его в тканях и по-
ступление в кровь, количество NН3 в крови очень мало и составляет
0,05 ммоль/л.
Это свидетельствует о существовании механизмов обезвре-
живания аммиака, которые могут нарушаться.
Различают механизмы местного и общего обезвреживания аммиака. Местное обезвреживание сводится к временному связыванию аммиака с образованием его транспортных форм, в составе которых он доставляется к органам, где происходит общее обезвреживание. Последнее заключается в образовании инертных, ненужных организму соединений, которые выводятся с мочой.
Местное обезвреживание аммиака
Осуществляется в тканях (мозг, мышцы, сетчатка и др.), где происходит непосредственное образование NН3, по нескольким меха-
низмам.
1. Главным путем обезвреживания аммиака является его связы-
вание с глутаминовой (у животных) и аспарагиновой (больше у растений) кислотами, т.е. их амидирование. Протекает в мышечной ткани, мозгу, печени, почках с затратой АТФ. Катализируется глутаминсинтетазой, локализованной в ЭПС.
Образуется глутамин, который легко проходит через мембраны (у растений – аспарагин).
Образовавшиеся глутамин и аспарагин являются главными транспортными формами аммиака, в виде которых он доставляется в печень и почки, где происходит общее обезвреживание.
Глутамин и аспарагин являются и главными резервными формами аммиака. Азот амидной группы глутамина и аспарагина используется при синтезе важных органических соединений: пуриновых, пиримидиновых нуклеотидов, триптофана, гистидина, глюкозаминфосфата, карбамоилфосфата. Глютаминсинтетаза - это регуляторный фермент,
243

ингибирующийся каждым из этих конечных продуктов метаболизма (типичный пример регуляции по типу обратной связи). Полагают, что в молекуле фермента имеются участки связывания для каждого из этих ингибиторов.
COOH |
O |
||||||||||
|
|
|
|
|
|
|
|
||||
C |
|
|
NH2 |
||||||||
|
|
|
+ NН3 + АТФ |
|
|||||||
|
|
|
|||||||||
|
|
|
|
|
|
||||||
|
CH2 |
|
|
|
|
|
|
|
|
||
|
|
|
CH2 |
||||||||
|
|
||||||||||
|
CH2 |
|
|
|
CH2 + АДФ + Н3РО4 |
||||||
|
CH |
|
NH2 |
|
|
CH |
|
|
NH2 |
||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
|
COOH |
|
|
COOH |
|||||||
|
ГЛУ |
ГЛН |
|||||||||
2.Обезвреживание аммиака в тканях происходит также путем амидирования остатков глутаминовой и аспарагиновой кислот в белках.
3.Восстановительное аминирование (ретрансаминирование) -
кетоглутарата. В мышечной ткани этот процесс приводит к образованию еще одной транспортной формы аммиака. При интенсивной мы-
шечной работе выделяющийся аммиак связывается с -
кетоглутаровой кислотой под действием глутаматдегидрогеназы. Образуется глутамат:
NН3 + -кг |
НАДФ!Н + Н+ НАДФ |
ГЛУ |
|
глутаматдегидрогеназа |
|
Глутаминовая кислота вступает в переаминирование с пируватом, образующимся при интенсивной мышечной работе в результате распада гликогена или глюкозы. Образующийся аланин является транспортной формой аммиака, доставляемой кровью в печень, где он вступает в переаминирование с -кетоглутаратом, в результате чего
получаются пируват и глутамат. Глутаминовая кислота через аспартат (переаминирование со щавелевоуксусной кислотой) включает свою NН2-группу в мочевину. Пируват используется в глюконеогенезе для
синтеза глюкозы, которая поставляется печенью мышцам. Этот механизм имеет важной значение для выведения аммиака из мышечной ткани и получил название глюкозо-аланинового цикла.
244

|
NH3 |
|
+ |
-кг |
мышечная |
НАДФН+Н+ |
ГЛУÃДГ |
||
ткань |
|
|
ГЛУ |
|
|
|
|
|
|
Глюкоза |
ПВК |
+ |
АлАТ |
|
|
|
|
|
-кг |
печень |
|
|
АЛА |
|
|
|
|
+ -кг |
|
|
|
|
|
|
Глюкоза |
ПВК |
АлАТ |
||
ГЛУ |
|
|||
|
ЩУК |
+ |
АсАТ |
|
|
|
АСП |
-кг |
|
|
|
|
||
синтез мочевины
Общее обезвреживание аммиака
Происходит в печени и почках, где образуются безвредные для организма инертные соединения, которые выводятся с мочой. В печени синтезируется мочевина, в почках – аммонийные соли. У животных и человека азот выводится, в основном, в виде мочевины (около 85- 90%). На соли аммония приходится около 3-6% всего азота, выводи-
мого с мочой.
Синтез мочевины
Синтез мочевины представляет собой циклический процесс, открытый Г.Кребсом в 1932 году. В печень с кровотоком поступают транспортные формы аммиака глутамин и аланин, и, кроме того, по воротной вене аммиак, всосавшийся в кишечнике. Глутамин под действием глутаминазы распадается на глутаминовую кислоту и аммиак. В митохондриях гепатоцитов из аммиака, СО2 с затратой АТФ под действием карбамоилфосфатсинтетазы (1) синтезируется карбамоил-
фосфат.
(1)O
NH3+CO2+2АТФ+Н2О H2N C O ~ PO3H2+2АДФ+Н3РО4
карбамоилфосфат
245

Карбамоилфосфат взаимодействует с орнитином при участии орнитинкарбамоилтрансферазы (2) с образованием цитруллина, кето-
форма которого подвергается таутомерной перегруппировке, переходя в енольную.
|
|
|
O |
|
|
NH |
|
|
|
NH2 |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
(2) |
|
C |
|
|
|
O |
|
|
|
|||||||||
H2N |
|
C |
|
|
|
|
O ~ PO3H2 + |
CH2 |
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
NH |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH2)3 |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
|
|
|
NH2 |
|
HC |
|
|
|
|
|
|
NH2 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
COOH |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
орнитин |
цитруллин |
|||||||||||||||||||
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
NH |
COOH |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
C |
|
|
OH |
H2N |
|
|
COOH |
ТФ |
C |
HN |
|
CH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
NH |
|
CH |
|
|
NH |
CH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH (4) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
(CH2)3 |
|
|
|
|
|
|
|
(CH2)3 |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
COO |
|
|
|
|
|
||||||||||||||||||||
|
|
HC |
|
|
|
NH2 |
|
|
|
|
АМФ |
HC |
|
|
NH2 |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АСП |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
COOH |
|
|
+Н4Р2О7 |
COOH |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
+Н2О аргининсукцинат
2Н3РО4
Цитруллин вступает в конденсацию с аспарагиновой кислотой под действием аргининсукцинатсинтетазы (3) с затратой АТФ. Образуется аргининянтарная кислота, которая аргининсукцинатлиазой (4)
расщепляется на аргинин и фумаровую кислоту.
Аргинин расщепляется аргиназой (5) на орнитин и мочевину,
которая простой диффузией (по градиенту концентрации) выходит из клеток в кровь и выделяется с мочой. В сутки в норме выделяется от 20 до 40г мочевины.
Фумаровая кислота является промежуточным продуктом цикла трикарбоновых кислот и фумаратгидратазой превращается в малат, который окисляется малатдегидрогеназой в щавелевоуксусную кислоту. Оксалацетат вступает в реакцию переаминирования с глутаминовой кислотой и превращается в аспарагиновую, которая вновь используется в синтезе мочевины. Образовавшийся из глутамата α-
кетоглутарат вступает в реакцию переаминирования с любыми аминокислотами печени.
246

|
NH2 |
|
|
|
|
|||
C |
|
NH |
COOH |
|||||
|
||||||||
|
||||||||
|
|
|
|
+ |
|
|
|
|
NH |
||||||||
|
CH |
|||||||
|
|
|
|
|
|
|
|
|
(CH2)3 |
CH |
|||||||
HC NH2 COOH COOH фумарат аргинин
+ Н2О (5)
NH2
NH2 (CH2)3 + C O
HC NH2
NH2
COOH
Таким образом, процесс синтеза мочевины – циклический и требует орнитина и затраты АТФ. Атомы азота мочевины имеют разное происхождение: один атом поступает в составе глутамина, образовавшегося в тканях, и принадлежит азотсодержащим соединениям периферических тканей. Второй атом включается аспарагиновой кислотой, образующейся при переаминировании щавелевоуксусной и глутаминовой кислот. Глутаминовая кислота забирает аминогруппы аминокислот печени (в том числе, поступившего аланина).
Синтез аммонийных солей
Глутамин, доставляемый кровотоком в почки, расщепляется глутаминазой, активируемой протонами и самим глутамином, на глутаминовую кислоту и аммиак. Аммиак взаимодействует с протонами, образуя ион аммония, который соединяется с анионами различных кислот: фосфорной, серной, угольной, соляной, щавелевой, мочевой.
NН3 + Н+ → NН4+
Образуются соли аммония – фосфаты, сульфаты, карбонаты, хлориды, оксалаты, ураты, которые выводятся с мочой. Всего в сутки у здорового человека выделяется 1-1,2 г таких солей.
Процесс имеет важное значение, т.к. является не только механизмом общего обезвреживания аммиака, но участвует в поддержании кислотно-щелочного равновесия в организме, а также сберегает от вы-
ведения с мочой катионы натрия и калия.
247

Лекция 25
ПРЕВРАЩЕНИЯ АМИНОКИСЛОТ ПО КАРБОКСИЛЬНОЙ ГРУППЕ Ã ДЕКАРБОКСИЛИРОВАНИЕ
В тканях животных процесс декарбоксилирования аминокислот протекает под действием декарбоксилаз с образованием аминов.
R CH COOH R CH 2NH 2 + CO 2
NH 2
Декарбоксилазы аминокислот Ã сложные ферменты, кофер-
ментом которых является пиридоксальфосфат. Обнаружены процессы декарбоксилирования гистидина, триптофана, 5-
гидрокситриптофана, тирозина, глутаминовой, аспарагиновой, цистеиновой кислот с образованием соответствующего амина: гистамина, триптамина, серотонина, тирамина, γ-аминомасляной кислоты, β-
аланина, таурина. Их называют биогенными аминами, так как в малых дозах это биологически активные вещества с мощным фармакологическим действием, в больших дозах – фармакологические яды. Декарбоксилазы ароматических аминокислот, гистидина, глютаминовой кислоты и других не отличаются строгой специфичностью. Ферменты мало активны, и процесс протекает с малой скоростью.
При декарбоксилировании тирозина образуется тирамин, проявляющий сосудосуживающее действие.
|
|
OH |
|
|
OH |
|||
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO2 |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|||
|
CH2 |
|
CH2 |
|
NH2 |
||||
|
|
|
|
||||||
Н2N - CН - COOH |
|||||||||
|
|
|
|
|
|
|
|||
тирозин тирамин
Декарбоксилирование триптофана сопровождается образованием триптамина, также обладающего сосудосуживающим действием.
248

H2N CH COOH |
|
|
CH2 |
|
CH2 CH2 NH2 |
NH |
CO2 |
NH |
|
||
триптофан |
|
триптамин |
При декарбоксилировании производного триптофана – 5- гидрокситриптофана образуется 5- гидрокситриптамин или серотонин.
|
H2N CH COOH |
|
|
|
HO |
|
CH2 |
HO |
CH2 CH2 NH2 |
|
NH |
CO2 |
|
NH |
|
|
|
||
5-гидрокситриптофан серотонин
Серотонин преимущественно образуется в нервной ткани и кишечнике. Обладает сильным сосудосуживающим действием, является нервным медиатором, поддерживает нормальную психическую деятельность, участвует в центральной регуляции артериального давления, температуры тела, дыхания, в почечной фильтрации, способствует развитию аллергической реакции, токсикоза беременности.
Декарбоксилирование гистидина приводит к образованию гиста-
мина.
N |
|
H2N |
|
|
|
|
|
CH |
|
COOH |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH |
|
CH |
|
NH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
CO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
гистидин |
|
|
|
|
|
|
|
|
|
|
гистамин |
|
|
|
|
|
|
|
||||||
Декарбоксилирование гистидина гистидиндекарбоксилазой происходит главным образом в тучных клетках, которые имеются в соединительной ткани (практически во всех органах). Гистамин накапливается и хранится в этих клетках в соединении с белками в специальных секреторных гранулах и может освобождаться и выделяться в кровь при разнообразных механических воздействиях (травма, ожог, электрическое раздражение), действии эндогенных веществ.
Физиологическое действие гистамина на сосуды отличается от действия других биогенных аминов: он расширяет сосуды и поэтому
249

снижает кровяное давление. В большом количестве гистамин образуется в месте травмы, в очаге воспалительного процесса, вызывает расширение сосудов, повышает проницаемость капилляров, способствует выходу лейкоцитов, развитию воспалительной реакции. Является медиатором нервных процессов, медиатором боли. Укусы насекомых (комары, клопы, осы и др.) вызывают зуд, боль, отечность, что связано с выделением гистамина. Гистамин стимулирует секрецию желудочного сока и слюны (поэтому его используют в клинике при исследовании секреторной функции желудка - гистаминовый завтрак). Если слизи-
стая желудка на введение гистамина не усиливает секрецию сока, то это свидетельствует о повреждении секреторных клеток - атрофиче-
ском гастрите. Гистамин сокращает гладкие мышцы легких, что проявляется приступом удушья. Гистамин способствует сенсибилизации организма и развитию аллергических реакций.
Обезвреживание гистамина происходит путем его метилирования с образованием 1-метилгистамина, который выводится с мочой.
При α-декарбоксилировании глутаминовой кислоты образуется γ-аминомасляная кислота.
|
|
|
|
COOH |
|
|
|
COOH |
|
|||||
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CO2 |
|
CH2 |
|
||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H N |
|
|
CH |
|
COOH |
|
CH2 |
|
NH |
|||||
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глутаминовая |
|
γ- аминомасляная кислота |
||||||||||||
|
кислота |
|
|
|
|
|
(ГАМК) |
|||||||
ГАМК в большом количестве содержится в сером веществе мозга, в то время как в белом веществе мозга и периферической нервной системе ее почти нет. Является тормозным фактором в нервных клетках. В опытах с изолированной петлей кишечника показано, что ГАМК вызывает прекращение перистальтики даже в присутствии ацетилхолина, стимулирующего перистальтику. Используется в клинике при лечении заболеваний центральной нервной системы, связанных с резким возбуждением коры головного мозга (эпилепсия).
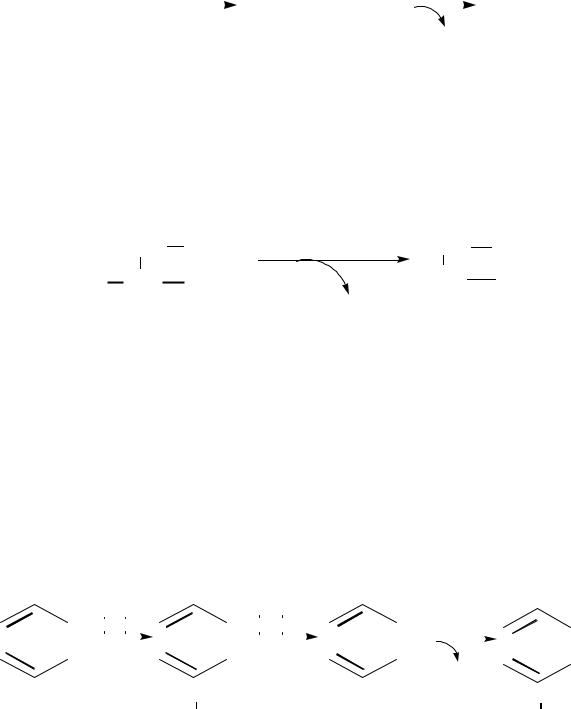
Цистеин окисляется в цистеиновую кислоту, которая в тканях животных декарбоксилируется с большой скоростью с образованием таурина.
250
|
|
CH |
|
SH |
|
+ O2 |
|
|
CH SO H |
|
|
CH SO H |
||||||||||
|
|
|
|
|
|
|
||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
CH |
|
|
COOH |
H2N |
|
CH |
|
COOH |
CO |
CH2 |
|
NH2 |
||||||||
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
||
цистеин |
цистеин-диокси- |
|
|
цистеиновая |
|
|
таурин |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
геназа |
|
|
кислота |
|
|
|
|
|
|
||||
Таурин используется в реакциях конъюгации с желчными кислотами для увеличения их гидрофильности. Непосредственное декарбоксилирование цистеина, протекающее в организме с небольшой скоростью, сопровождается образованием цистеамина.
CH2 |
SH |
CH2 |
SH |
H N CH |
COOH |
CH2 |
NH |
2 |
|
CO2 |
2 |
|
|
|
|
цистеин |
|
цистеамин |
|
Цистеамин оказывает защитное действие при лучевой болезни, однако его действие является непродолжительным, поэтому были синтезированы его производные, аналоги, которые нашли применение в терапии лучевых поражений.
В животных тканях с большой скоростью протекает декарбоксилирование 3,4-диоксифенилаланина - производного фенилаланина. При этом образуется ДОФ-амин, оказывающий мощное сосудосуживающее действие. ДОФ-амин является промежуточным продуктом в
синтезе катехоламинов норадреналина и адреналина.
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
|
OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH2 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H2N - CHCOOH H2N - CН - COOH |
H2N - CН-COOH |
|
|
CH2NH2 |
|||||||||||||||||||||||||||||
фенилаланин |
тирозин |
|
3,4-диоксифенилаланин |
ДОФ-амин |
|||||||||||||||||||||||||||||
Под действием декарбоксилаз из диаминокарбоновых кислот образуются диамины: из орнитина – путресцин, лизина – кадаверин.
251
