
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ 89
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •1.2.1 Радикало-функциональная номенклатура
- •1.2.2 Систематическая (заместительная) номенклатура
- •1.3 Вопросы и упражнения для самопроверки:
- •2. ИЗОМЕРИЯ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ
- •2.1 Структурная изомерия
- •2.2 Стереоизомерия
- •2.2.1.1 Геометрическая изомерия или цис-транс-изомерия один из видов стереоизомерии, возникающий при разном расположении одинаковых заместителей по одну или по разные стороны плоскости π связи или неароматического цикла (Рис.2.1).
- •2.2.1.2 Хиральность.
- •2.2.1.3 Оптическая изомерия. Энантиомеры и диастереомеры
- •2.2.1.4 Относительная и абсолютная конфигурации
- •2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
- •2.3 Вопросы и упражнения для самопроверки
- •3.1. Образование ковалентных связей
- •3.2.3 Ароматичность
- •3.3 Взаимное влияние атомов в молекуле
- •3.3.1 Индуктивный эффект
- •3.3.2 Мезомерный эффект
- •3.4. Вопросы и упражнения для самопроверки
- •4. КИСЛОТНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •4.1 Теория Бренстеда-Лоури, протолитическая
- •4.2. Вопросы и упражнения для самопроверки
- •5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- •5.1 Механизмы органических реакций
- •5.2.1 Гидратация алкенов. Роль кислотного катализатора
- •5.2.2 Реакции присоединения к асимметричным алкенам (правило Марковникова)
- •5.2.3 Реакция присоединения к α, β-ненасыщенным карбонильным соединениям
- •5.3.1 Галогенирование бензола
- •5.3.2 Ориентирующее действие заместителей в бензольном ядре. Ориентанты первого и второго рода
- •5.4 Нуклеофильное замещение у насыщенного атома углерода
- •5.5 Механизм и стереохимия реакций элиминирования (Е)
- •5.6 Окисление и восстановление органических соединений
- •5.6.1 Окисление гидроксильных и оксо-групп
- •5.6.2 Окисление непредельных и ароматических соединений
- •5.6.3 Реакции восстановления
- •5.6.4 Обратимые окислительно-восстановительныесистемы
- •5.7. Вопросы и упражнения для самопроверки
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- •6.1 Способы получения альдегидов и кетонов
- •6.2 Химические свойства альдегидов и кетонов (карбонильных соединений)
- •6.2.1 Реакция альдегидов с нуклеофилами
- •6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
- •6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
- •6.2.2 Реакции конденсации
- •6.2.2.1 Кето-енольная таутомерия альдегидов и кетонов. Альдольное присоединение
- •6.2.2.2 Кротоновая конденсация или альдольно - кротоновая конденсация
- •6.3 Окисление и восстановление альдегидов и кетонов
- •6.4 Вопросы и упражнения для самопроверки
- •7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- •7.1. Основные пути получения карбоновых кислот:
- •7.2. Малоновый синтез карбоновых кислот
- •7.3. Классификация карбоновых кислот
- •7.4 Химические свойства карбоновых кислот
- •7.4.2. Восстановление карбоновых кислот
- •7.4.3. Декарбоксилирование карбоновых кислот
- •7.5. Дикарбоновые кислоты
- •7.6. Угольная кислота и ее производные
- •7.7. Вопросы и упражнения для самопроверки
- •8. ПОЛИ- И ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ
- •8.1. Аминоспирты
- •8.2 Классификация одноосновных гидроксикислот
- •8.2.1 Получение гидроксикислот
- •8.2.2 Специфические реакции гидроксикислот
- •8.3. Многоосновные гидроксикислоты
- •8.4. Оксокислоты
- •8.5 Вопросы и упражнения для самопроверки
- •9. АМИНОКИСЛОТЫ
- •9.1. Изомерия аминокислот
- •9.2. Классификации аминокислот
- •9.2.1. Классификации аминокислот по биологической ценности
- •9.2.2. Классификации аминокислот на основе химического строения аминокислот
- •9.2.2.3. Современная классификация α-аминокислот
- •9.4. Кислотно-основные свойства аминокислот
- •9.5. Способы получения аминокислот
- •9.6. Химические свойства
- •9.7. Специфические реакции α, β, γ, δ-аминокислот
- •9.8. Качественные реакции на аминокислоты, пептиды, белки.
- •9.9. Методы количественного определения аминокислот
- •9.10. Редко встречающиеся аминокислоты
- •9.11.2 Вторичная структура полипептидной цепи
- •9.11.3 Третичная структура белков
- •9.12. Вопросы и упражнения для самопроверки
- •Классификация углеводов
- •10.1. Моносахариды, классификация
- •10.2. Циклическое строение моносахаридов
- •10.3. Химические свойства моносахаридов
- •10.3.1. Реакции полуацетального гидроксила
- •10.3.3. Окисление и восстановление моносахаридов
- •10.3.4. Изомеризация в щелочной среде
- •10.4. Качественные реакции моносахаридов. Отличительные реакции пентоз и гексоз
- •10.5. Производные моносахаридов
- •10.6. Олигосахариды
- •10.6.1. Химические свойства олигосахаридов
- •10.7. Полисахариды
- •10.7.1. Гомополисахариды
- •10.7.2. Гетерополисахариды
- •10.8. Гликопротеины
- •10.9. Вопросы и упражнения для самопроверки
- •11. БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •11.1. Пятичленные ароматические гетероциклы
- •11.2. Шестичленный ароматический гетероцикл
- •11. 3. Нуклеиновые кислоты (НК)
- •11.3.1 Нуклеозиды
- •11.3.2. Нуклеотиды
- •11.3.3. Нуклеозидциклофосфаты
- •11.3.4. Рибо- и дезокси-рибонуклеиновые кислоты
- •11.4. Вопросы и упражнения для самопроверки
- •12. ЛИПИДЫ
- •12.1. Высшие жирные кислоты
- •12.2. Классификация омыляемых липидов
- •12.2.1. Простые липиды
- •12.2.1.1.Химические свойства простых липидов
- •12.2.2 Сложные липиды
- •12.2.2.2. Гликолипиды
- •12.3. Неомыляемые липиды
- •12.3.1 Терпены (изопреноиды)
- •12.3.3. Стероиды
- •12.4. Вопросы и упражнения для самопроверки
- •13. Методы, используемые для изучения соединений в органической химии
- •Литература
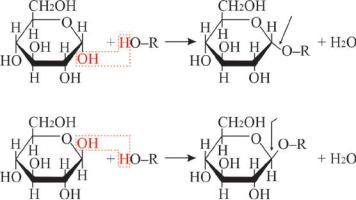
При этом α-D- глюкопираноза различается от β-D- глюкопиранозы величиной удельного вращения: уα-аномера (+112o), у β-аномера (+19o). У свежеприготовленного раствора каждого аномера при стоянии наблюдается постепенное изменение удельного вращения до достижения постоянной величины + 52,5o, что обусловлено преобладанием в растворе β-аномера D-глюкопиранозы, у которого все ОН группы, включая полуацетальную, занимают экваториальное положение.
10.3. Химические свойства моносахаридов
Моносахариды очень реакционноспособные соединения, что обусловлено наличием в них трех видов функциональныхгрупп: карбонила, спиртовых гидроксильных групп и полуацетального гидроксила.
10.3.1. Реакции полуацетального гидроксила
Циклические моносахариды со спиртами в присутствии Н+ в «безводных» условиях образуют полные ацетали, которые называются О-гликозидами (Рис. 10.5):
α-гликозидная
связь
спирт
α-глюкоза α-гликозид
β -гликозидная
связь
спирт
β-глюкоза β-гликозид
Рис. 10.5 Реакции полуацетального гидроксила со спиртами
173
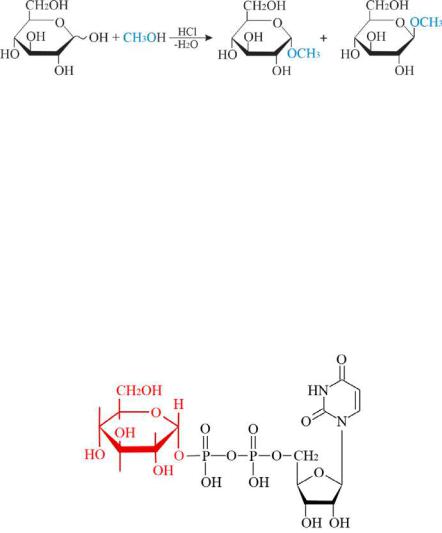
При этом в молекуле моносахарида на остаток спирта (алкоксигруппу,OR)замещаетсятолькополуацетальныйгидроксил.Вназвании гликозида суффикс -оза в названии моносахарида заменяется на - озид, а связь междуатомом С-1 и группой OR называется гликозидной.
D-глюкопираноза |
метил- α- D- |
метил- β- D- |
|
глюкопиранозид |
глюкопиранозид |
Полуацетальный гидроксил обуславливает важнейшие свойства моносахаридов.Врастительномиживотноморганизмахмоносахариды редко встречаются в свободном виде, в основном встречаются в форме ацеталей.
Многие О-гликозиды сравнительно легко гидролизуются в кислой среде (реакция, обратная реакции получению гликозидов). Скорость гидролиза зависит от строения моносахаридного остатка и природы агликона.
В организме образование гликозидов происходит при помощи фосфатов или нуклеотиддифосфатсахарoв, например, при участии уридиндифосфоглюкозы:
174
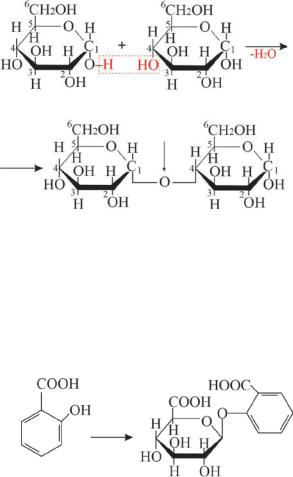
Вэтих соединениях остаток фосфорной кислоты или дифосфат нуклеозида являются хорошими уходящими группами.
Ворганизмемоносахаридыобразуютгликозидызасчётспиртовых групп самих же моносахаридов и образуются олигосахариды и полисахариды (Рис.10.6).
α- D-глюкопираноза α- D-глюкопираноза
Рис. 10.6 Схема образования дисахарида мальтозы (О-глюкозида)
Кроме того, в организме происходит образование гликозидов D-глюкуроновой кислоты с некоторыми токсичными соединениями
(фенолом, салициловой кислотой и др.). Эти гликозиды (О-глюк-
урониды) выводятся из организма с мочой и таким образом осуществляется детоксикация:
салициловая кислота глюкуронид салициловой кислоты
175
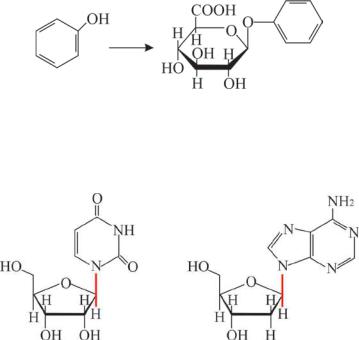
фенол |
фенольный глюкуронид |
Большое значение имеют N-гликозиды, представители которых являются компонентами нуклеиновых кислот, РНК и ДНК:
уридин |
дезоксиаденозин |
Важнейшим свойством гликозидов является способность гидролизоваться в кислойсреде и достаточная устойчивость к разбавленным щелочам.
10.3.2. Реакции спиртовых ОН-групп Образование сложных и простых эфиров.
Сложные эфиры образуются при взаимодействии моносахаридов с ацилирующими агентами, например, ангидридами карбоновых кислот по механизму нуклеофильного замещения. (Рис.10.7).
176
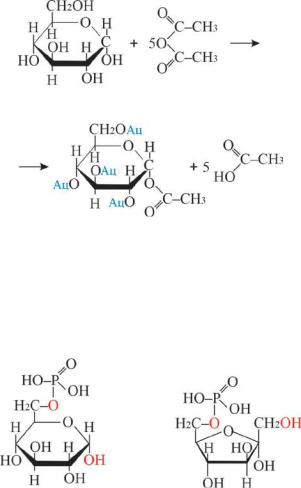
α-D-глюкопираноза |
ангидрид уксусной |
|
кислоты |
уксусная
кислота
1,2,3,4,6-пентаацетил-
α-D-глюкопираноза
Рис. 10.7 Схема образования сложных эфиров
В биологических превращениях моносахаридов важную роль играют фосфаты (сложные эфиры фосфорной кислоты). Это глюкозо-1 -фосфат, глюкозо-6-фосфат, фруктозо-6-фосфат:
глюкозо-6-фосфат фруктозо-6-фосфат
Сложные эфиры в кислой и основной среде подвергаются гидролизу до соответствующей кислоты или соли и моносахарида.
Простые эфиры образуются при взаимодействии гидроксильных групп моносахаридов с алкилгалогенидами. Одновременно в реакцию вступает и гликозидная ОН-группа, образуя гликозид. Гидролиз гликозидоввкислойсредеприводиткобразованиюпростыхэфиров(Рис.10.8)
177
