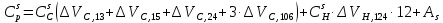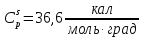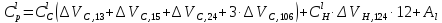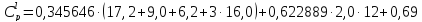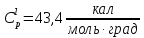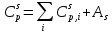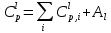- •Введение
- •Патентно-литературный обзор
- •Метод групповых инкрементов по Аскадскому а.А
- •Расчет геометрических характеристик молекулярной цепи поли-1-(триметилсилил)пропина-1
- •Температура стеклования
- •Температура плавления
- •Температура деструкции
- •Показатель преломления
- •Коэффициент оптической чувствительности по напряжению
- •Диэлектрическая проницаемость
- •Плотность энергии когезии и параметр растворимости Гильдебранда
- •Критерий растворимости
- •Теплоемкость
- •Расчет физико-химических свойств поли-1-(триметилсилил)-3-хлорпропина-1
- •Расчет Ван-дер-Ваальсовых объемов
- •Температура стеклования
- •Температура стеклования
- •Приложения
Критерий растворимости
Проблема предсказания растворимости полимеров является актуальной в течение многих лет. Один из способов предварительной оценки растворимости полимера является согласование величин параметров растворимости Гильдебранда для полимера δп и растворителя δр. При этом считается, что если соблюдается условие δп ≈ δр, то можно ожидать растворения полимера в данном растворителе. Опыт показывает, однако, что с помощью такого сопоставления можно лишь уверенно «отбросить» те растворители, в которых растворение данного полимера происходить не будет. Это системы, для которых δп>>δр или δп>>δр. С помощью такой оценки удается значительно сузить круг подлежащих проверке растворителей, в которых полимер может растворяться. Оценки и опыт показывает, что, например, из 160 растворителей можно таким способом сразу же для каждого полимера исключить из рассмотрения 120-130 органических жидкостей, как явно не пригодных для растворения. В оставшихся растворителях, подчиняющихся условию δп≈δр, примерно в половине из них полимер будет растворим. Условие предсказания растворимости полимера учитывает не только химическое строение, но и конкретную надмолекулярную структуру полимера:
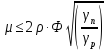 ,
где
,
где
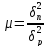 ;
;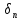 и
и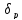 - параметры Гильдебранда соответственно
для полимера и растворителя;
- параметры Гильдебранда соответственно
для полимера и растворителя;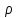 – константа;
– константа;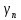 и
и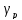 – поверхностное натяжение полимера и
растворителя соответственно.
– поверхностное натяжение полимера и
растворителя соответственно.
По таблице 7.3. [10] выписываем пять растворителей, у которых δр ≈ 8,32 (кал/см3)1/2:
Изопропилбензол δр =8,4 (кал/см3)1/2
1,1,1-Трихлорэтан δр =8,3 (кал/см3)1/2
Винилхлорид δр =8,2 (кал/см3)1/2
Винилиденхлорид δр =8,4 (кал/см3)1/2
Изопропилацетат δр =8,5 (кал/см3)1/2
Теплоемкость
Под теплоемкостью подразумевают количество тепла, которое нужно затратить на нагревание тела на 1°С. Различают молярную теплоемкость, если речь идет о моле вещества, и удельную теплоемкость, если речь идет об 1 г вещества. Теплоемкость при постоянном давлении Ср равняется скорости изменения энтальпии с ростом температуры, а теплоемкость при постоянном объеме Cv -скорости изменения внутренней энергии с ростом температуры.
В довольно широком интервале температур теплоемкость увеличивается линейно с ростом температуры, причем температурный коэффициент роста теплоемкости для твердых полимеров имеет среднюю величину 3∙10-3. При фазовом или физическом переходе полимера теплоемкость меняется скачком.
Например, при переходе из стеклообразного состояния в высокоэластическое наблюдается достаточно резкий скачок теплоемкости в сторону ее увеличения. После прохождения физического перехода теплоемкость вновь начинает слабо увеличиваться с ростом температуры.
Теплоемкость полимеров зависит от их химического строения.
Наиболее низкой теплоемкостью среди углеводородных полимеров обладает полиэтилен и полиоксиметилен.
При замещении атомов водорода на полярные группы теплоемкость возрастает. При переходе от алифатических полимеров к ароматическим наблюдается существенное возрастание теплоемкости.
Молярная теплоемкость полимерного тела пропорциональна Ван-дер-Ваальсовому объему атомов, входящих в повторяющееся звено полимера [9, 10]. Иными словами:
|
|
(31) |
И
|
|
(32) |
где
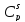 и
и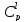 – молярные теплоемкости полимера,
находящегося в стеклообразном и
высокоэластическом состоянии,
соответственно;
– молярные теплоемкости полимера,
находящегося в стеклообразном и
высокоэластическом состоянии,
соответственно;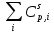 и
и -
инкременты для каждого атома, имеющие
смысл приведенной к единице
Ван-дер-Ваальсового объема теплоемкости,
действующие, соответственно, в
стеклообразном и высокоэластическом
состояниях.
-
инкременты для каждого атома, имеющие
смысл приведенной к единице
Ван-дер-Ваальсового объема теплоемкости,
действующие, соответственно, в
стеклообразном и высокоэластическом
состояниях.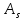 и
и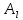 – параметры, равные
– параметры, равные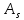 = 0,77 кал/(моль∙град),
= 0,77 кал/(моль∙град),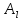 = 0,69 кал/(моль∙град).
= 0,69 кал/(моль∙град).
Параметры
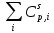 и
и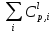 берем из таблицы 51 [9].
берем из таблицы 51 [9].