
- •Температуры начала и конца кристаллизации сплавов
- •Тут получается вроде лол какой-то
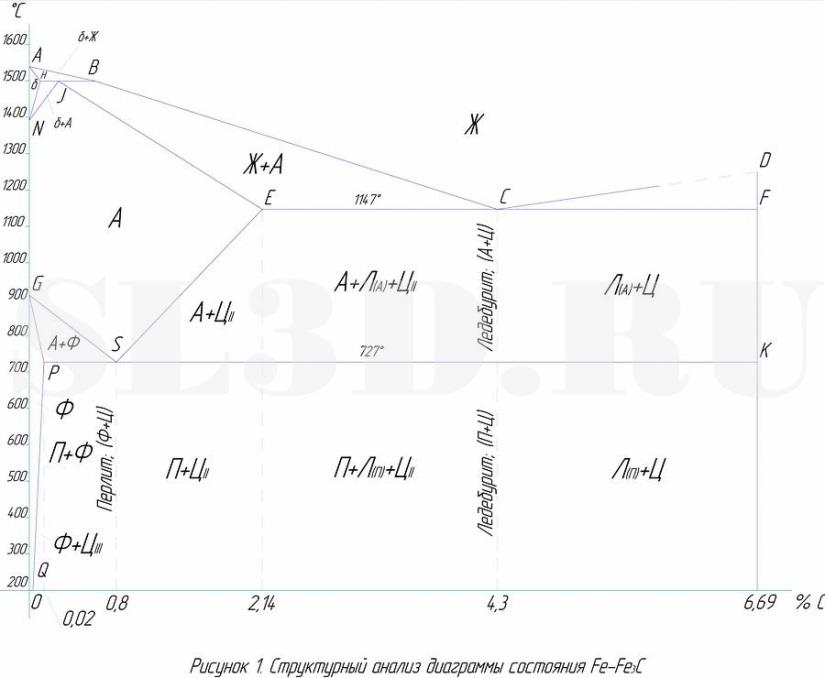
- •Диаграмма Fe - Fe3c
- •1. Общие сведения
- •Процессы при структурообразовании железоуглеродистых сплавов
- •Компоненты и фазы железоуглеродистых сплавов
- •Правило фаз
- •3. Характеристика металлических сплавов.
- •Структуры железоуглеродистых сплавов
- •Диаграмма состояния железо – графит.
- •Процесс графитизации.
3. Характеристика металлических сплавов.
При образовании сплава атомы компонентов вступают в определенные взаимодействия друг с другом. В жидком состояли большинство металлических сплавов представляют собой однородные жидкости, т.е. ЖИДКИЕ растворы. После затвердевания в результате кристаллизации в сплавах могут образовываться в качестве структурных составлявших твердые растворы, химические соединения, физико-химические смеси.
ТВЕРДЫЕ РАСТВОРЫ - однородные сплавы, состоящие из одной фазы переменного состава. Структура твердого раствора, видимая под микроскопом, состоит, как и у чистых металлов, из однородных зерен. При образовании твердых растворов сохраняется кристаллическая решетка одного из компонентов (растворителя), а атомы растворенного компонента (или нескольких) могут либо заметать часть атомов растворителя в узлах кристаллической решетки, либо размещаться между атомами растворителя. В зависимости от характера распределения атомов растворенного компонента в кристаллической решетке растворителя различают три типа твердых растворов: твердые растворы замещения, твердые растворы внедрения и твердые растворы вычитания (для системы железо- углерод характерными являются твердые растворы внедрения).
ТВЕРДЫЕ РАСТВОРЫ ВНЕДРЕНИЯ образуются при условии, если диаметр внедряемого атома (например, углерода, азота или кислорода) намного меньше диаметра атома растворителя (например, железа). Твердые растворы внедрения могут быть только ограниченными.
Химические
соединения чаше всего образуются между
элементами, расположенными далеко друг
от друга в периодической таблице, т.е.
сильно различающимися по своему строению
и свойствам. Соотношение чисел атомов
элементов в химическом соединении
имеет строго определенное значение
(стехиометрическое соотношение
элементов), выражаемое формулой
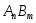 (например,Fe3C).
Атомы в химическом соединении имеют
свою кристаллическую решетку, отличную
от решеток элементов, образовавших это
соединение, с правильным упорядоченным
расположением атомов компонентов в
кристаллической решетке. Свойства
соединений не похожи на свойства исходных
элементов; как и чистые металлы, они
имеют постоянную температуру плавления
(диссоциации). Химические соединения,
как правило, обладают высокой твердостью
и хрупкостью.
(например,Fe3C).
Атомы в химическом соединении имеют
свою кристаллическую решетку, отличную
от решеток элементов, образовавших это
соединение, с правильным упорядоченным
расположением атомов компонентов в
кристаллической решетке. Свойства
соединений не похожи на свойства исходных
элементов; как и чистые металлы, они
имеют постоянную температуру плавления
(диссоциации). Химические соединения,
как правило, обладают высокой твердостью
и хрупкостью.
ФИЗИКО – ХИМИЧЕСКИЕ СМЕСИ – это сплавы, состоящие из компонентов, которые не способны к взаимному растворению в твердом состоянии или растворяются ограниченно. В физико-химических смесях фазы не меняют своих кристаллических решеток. Свойства этих смесей в равновесном состоянии, как правило, имеют промежуточные значения между свойствами исходных компонентов или же их твердых растворов или химических соединений и зависят от их количественного соотношения. По сравнению с металлами эти сплавы имеют значительно более низкую пластичность.
Следует различать фазовый и структурный составы сплавов и, соответственно, диаграммы фазовые и структурные. Первые дают возможность судить о состоянии сплава при любой температуре, т.е. о природе, числе и концентрации (составе) фаз. Вторые – дополнительно отображают форму, величину и расположение фаз, т.е. строение сплава или его структуру. При этом структурными составляющими называют отдельные, структурно обособленные части сплава, имеющие характерное и однообразное строение.
Вышеуказанные диаграммы, в свою очередь, подразделяются на стабильные и метастабильные. Стабильные диаграмм отображают устойчивое равновесное состояние фаз в сплавах. Метастабильные – содержат фазы, которые при определенных внешних воздействиях могут претерпевать изменения, однако в реальных условиях охлаждения сплавов существуют весьма устойчиво.
Для
сплавов железо-углерод, в зависимости
от равновесного состояния, различают
метастабильную диаграмму железо –
цементит (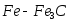 )
и стабильную железо-графит (
)
и стабильную железо-графит (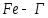 ).
На то, что система железо-графит является
более стабильной, чем система
железо-цементит, указывает тот факт,
что при нагреве до высоких температур
цементит распадается на железо и графит,
т.е. переходит в более стабильное
состояние.
).
На то, что система железо-графит является
более стабильной, чем система
железо-цементит, указывает тот факт,
что при нагреве до высоких температур
цементит распадается на железо и графит,
т.е. переходит в более стабильное
состояние.
Классификация железоуглеродистых сплавов.
В соответствии с диаграммой состояния все железоуглеродистые сплавы можно разделить на две принципиальные группы: стали – сплавы с концентрацией углерода до 2,14 % и белые чугуны – с концентрацией углерода свыше 2,14 %.
В свою очередь, и стали, и чугуны в зависимости от концентрации углерода дополнительно делятся еще на три группы каждая.
Стали с концентрацией углерода 0,02–0,8 % получили название доэвтектоидных сталей. При комнатной температуре структура таких сталей состоит из феррита и перлита. Феррит является не травящейся фазой, поэтому при металлографических исследованиях он выглядит в виде светлых полигональных зерен. Перлит является двухфазной структурой, состоящей из феррита и цементита, имеющего вид пластин или мелких зерен сферической формы. При металлографических исследованиях он выглядит темным. Все эти стали относятся к конструкционным сталям, поскольку из них изготавливают самые разнообразные детали машин и металлоконструкции.
Стали с концентрацией углерода 0,8±0,1 % получили название эвтектоидных сталей. Структура их состоит преимущественно только из перлита. По назначению эти стали могут использоваться и как конструкционные, и как инструментальные.
Стали с концентрацией углерода свыше 0,8 % получили название заэвтектоидных сталей. В структуре этих сталей при комнатной температуре можно заметить перлит и на фоне этой темной структурной составляющей отчетливо просматривается светлая сетка цементита. Все заэвтектоидные стали являются инструментальными сталями.
Чугуны с концентрацией углерода до 4,3 % называются белыми доэвтектичекими чугунами. При комнатной температуре их структура состоит из перлита, ледебурита на перлитной основе и вторичного цементита. При этом перлит выглядит в виде темных довольно крупных зерен, имеющих преимущественно округлую форму. Ледебурит на перлитной основе выглядит в виде мелких темных сферических зерен. Между зернами перлита и скоплениями ледебурита можно заметить светлый ореол, который представляет собой вторичный цементит.
Чугуны с концентрацией углерода 4,3±0,1 % получили название эвтектических белых чугунов. Их структура при комнатной температуре состоит преимущественно из ледебурита на перлитной основе.
При концентрациях углерода свыше 4,3 % образуются заэвтектические белые чугуны, имеющие в своей структуре ледебурит на перлитной основе и первичный цементит. Последний выглядит в виде светлых игл.
Или это лучше, хз
