
лабораторные работы 2010
.pdf
помощью дымососа уходит в атмосферу. Для того, чтобы компенсировать потерю влаги тканью, последняя непрерывно увлажняется при контакте с водой, налитой в нижнюю часть сушильной камеры.
Мощность, потребляемая электронагревателем, регулируются с помощью автотрансформатора 16 и измеряется амперметром 14 и вольтметром 15. Для измерения расхода воздуха используется ротаметр 11.
Температура воздуха контролируется термопарами, установленными до калориметра (1), за ним (3) и за сушильной камерой (4). Для определения влажности воздуха используются два психрометра, составленных из пары термопар - "сухой" и "мокрой", т.е. обернутой влажной тканью. Один психрометр (термопары 1 и 2) установлен в месте забора воздуха из помещения, второй (термопары 4 и 5) - на выходе из сушильной камеры.
3.4 Проведение опыта и обработка результатов
Перед включением установки необходимо убедиться в наличии воды в сушильной камере и стаканчике 13. Далее включается вентилятор и блок питания электронагревателя. Ручкой регулирования на панели блока питания необходимо установить требуемую мощность электрического тока и следить за тем, чтобы она не менялась в течение опыта.
Для получения достоверных результатов необходимо дождаться стационарного режима работы, когда расход воздуха, его параметры на входе и выходе, а также температура всех частей установки остается постоянной.
После достижения стационарного режима необходимо провести регистрацию показаний всех приборов и занести результаты в протокол измерений.
Таблица 3.1 – Протокол измерений
№ |
Время |
Мощность |
|
|
Температура t |
|
Расход |
||
режима |
нагревате- |
сухая |
мокрая |
|
за |
сухая |
мокрая |
возду- |
|
|
|
ля |
на |
на |
|
калори- |
на |
на |
ха |
|
|
входе |
входе |
|
метром |
выходе |
выходе |
||
|
|
|
|
|
|||||
1 |
c |
Вт |
°С |
°С |
|
°С |
°С |
°С |
кг/с |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
21
Опыт заканчивается после записи не менее трех различных режимов работы установки. При окончании опыта необходимо сначала выключить блок питания, затем вентилятор.
Для расчетов используются средние за один режим работы физические величины. Перед проведением необходимых расчетов строится h-d диаграмма для данного режима.
Исходная точка 1 определяется пересечением на h-d диаграмме изотерм соответствующих показаниям "сухой" и "мокрой" термопар перед калориметром (термопары 1 и 2). Точка 2, определящая состояние подогретого в калориметре воздуха, находится построением процесса подогрева от состояния точки 1 до температуры, измеренной термопарой 3. Далее следует построить точку 3, местоположение которой определится пересечением изотерм "сухой" термопары 4 и "мокрой" 5, установленных за сушилкой. Линия 2-3 характеризует процесс увлажнения воздуха в ходе высушивания ткани в сушилке.
Расход воздуха mc , кг/с определяется с помощью тарировочного
графика ротаметра в зависимости от положения поплавка. Расход воздуха за режим подсчитывается:
m = mcτ , кг,
где τ - время в секундах. |
|
|
|
|
|
Количество испаренной влаги за время τ |
нужно подсчитать по |
||||
формуле |
|
|
|
|
|
mво д.п. = 0,001(d3 − d1) , кг , |
(3.9) |
||||
Количество тепла, воспринятое сушильным агентом в калоримет- |
|||||
ре равно: |
|
|
|
|
|
Qк = m(h2 − h1) , |
кДж |
|
(3.10) |
||
Тепловые потери калориметра |
|
|
|
|
|
Qп о т= 0,001N |
эл |
τ − m(h − h ) ,кДж |
(3.11) |
||
к |
|
2 |
1 |
|
|
где 0,001N эл, кВт - мощность, измеренная в опыте.
Действительное количество тепла, затраченное на испарение 1 кг влаги:
q = |
N эл τ |
|
, кДж/кг исп.влаги |
m(d − d ) |
|||
3 |
1 |
|
|
|
|
22 |
|
Для расчета средней массовой теплоемкости используется формула:
C p = |
Qк |
,кДж/(кг К) |
(3.12) |
||
m(t2 |
−t1) |
||||
|
|
|
|||
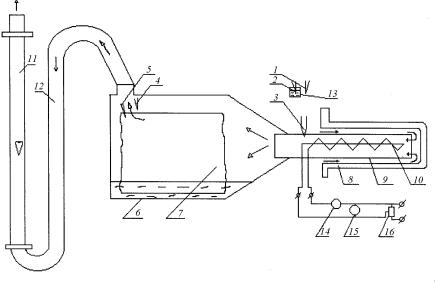
1,2,3,4,5 - термопары; 6 - вода; 7 - ткань; 8 - калориметр (сосуд Дюара); 9 - стеклянная трубка; 10 - электронагреватель; 11 - ротаметр; 12 - соединительный шланг;13 - стаканчик с водой; 14 - амперметр; 15 - вольтметр; 16 - автотрансформатор.
Рисунок 3.3 – Схема установки
После определения по формуле (3.12) изобарной теплоемкости вычисляется изохорная теплоемкость по уравнению Майера:
Cυ = C p − R ,
гдеR = 287 Дж/(кг*К) - газовая постоянная воздуха.
Показатель адиабаты K = C p / Cυ и полученные значения теплоемкостей сравниваются с табличными [1,2].
23
3.5Вопросы для самоподготовки
1.Теплоемкость, удельная теплоемкость.
2.Истинная и средняя теплоемкость.
3.Связь между теплоемкостями C p и Cυ (уравнение Майера).
4.Уравнение первого закона термодинамики для стационарного
потока.
5.Газовая смесь. Закон Дальтона.
6.Температура точки росы.
7.Абсолютная влажность воздуха.
8.Относительная влажность воздуха.
9.Влагосодержание владжного воздуха.
10.Связь между парциальным давлением пара и его влагосодер-
жанием.
11.Плотность влажного воздуха.
12.Энтальпия влажного воздуха.
13.Устройство психрометра.
14.h-d диаграмма влажного воздуха.
15.Нахождение относительной влажности по h-d диаграмме.
16.Процесс нагрева (охлаждения) влажного воздуха в h-d диа-
грамме.
17.Идеальная (теоретическая) сушилка.
18.Нахождение температуры точки росы по h-d диаграмме.
19.Определение парциального давления водяного пара по h-d диаграмме.
3.6Литература для самостоятельной работы
1.Зубарев В.Н., Александров А.А. Охотин В.С. Практикум по технической термодинамике: Учебное пособие для вузов. - М.: Энерго-
атомиздат, 1986. -304 с.
2.Ривкин С.Л. Термодинамические свойства газов. - М.: Энергия,
1964.
3.Кириллин В.А., Сычев В.В., Шейндлин О.В. Техническая термодинамика: Учебник для вузов. - М.: Энергия, 1974.
24
4 ЛАБОРАТОРНАЯ РАБОТА № 3
ИЗОХОРНОЕ НАГРЕВАНИЕ ВОДЫ И ВОДЯНОГО ПАРА
Цель работы:
Целью работы является экспериментальное исследование кривой насыщения водяного пара.
В результате должны быть усвоены особенности фазового перехода в системе вода-пар при различных исходных значениях величины
удельного объема υх , расчетные и экспериментальные методы определения теплоты парообразования.
4.1 Задание на работу
4.1.1Построить кривую насыщения в P −t и P −υ диаграммах, используя табличные и экспериментальные данные.
4.1.2Рассчитать для каждой экспериментальной точки теплоту парообразования по уравнению Клапейрона-Клаузиуса.
4.1.3Построить графические зависимости r(t) по табличным и
экспериментальным данным.
4.2 Описание методики эксперимента
Опытным путем установлено, что каждому давлению соответствует определенная температура кипения данной жидкости, являющаяся одновременно температурой ее насыщенного пара. С повышением давления возрастает температура кипения. В общем виде связь между температурой насыщения и давлением выражается уравнением
Ps = f (ts ) , которое действительно только для области насыщения
(рисунок 4.1, б).
Каждому веществу присуща своя, особая кривая насыщения. Любая точка этой кривой изображает двухфазное состояние вещества, равновесное сосуществование кипящей жидкости и сухого насыщенного пара. Над кривой фазового равновесия располагается область
25
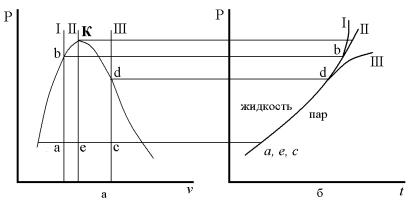
жидкой фазы, а ниже - пар. Кривая оканчивается в критической точке К. Выше ее нет четкой границы, которая разделяла бы вещество на две одновременно и равновесно сосуществующие фазы.
Математическое описание кривой насыщения производится при помощи формулы Клапейрона-Клаузиуса:
dP |
= |
|
r |
, |
(4.1) |
|
T (υ"−υ') |
||||||
dT |
|
|
|
|||
гдеυ" - удельный объем сухого насыщенного пара, м3/кг;
υ' - удельный объем жидкости, находящейся под давлением ее насыщенных паров, м3/кг;
r - удельная теплота фазового перехода, кДж/кг.
В данном случае r - теплота парообразования, показывающая, какое количество теплоты надо сообщить при температуре кипения 1 кг жидкости, чтобы превратить ее в сухой пар.
Рисунок 4.1 – Фазовая диаграмма
Характер изменения теплоты парообразования удобно проследить на фазовой диаграмме в плоскости p −υ , на которой погра-
ничная кривая b - K (рисунок 4.1, а) есть геометрическое место точек,
характеризующих удельный объем υ' жидкости, находящейся с влажным паром в равновесии.
Кривая k-d определяет в каждой точке объем υ′′ сухого насыщенного пара. Из рисунка 4.1,а видно, что с ростом давления, а, следо-
26
вательно, и температуры разность ( υ′′ −υ′ ) уменьшается и стремится к нулю в точке К. Из формулы 4.1. получаем, что
|
r =T( υ′′−υ′) |
dP |
|
||
|
|
. |
(4.2) |
||
|
dT |
||||
Так как |
dP |
> 0 (рис.4.1,в), то с ростом давления и температуры |
|||
|
dT |
|
|
|
|
теплота парообразования r уменьшается и равна нулю в точке К. |
|||||
До тех |
пор, |
пока процесс изохорного |
нагревания протекает в |
||
двухфазной области (участок а-b изохоры I и участок c-d изохоры III на рисунке 4.1, б), давление вещества в каждой точке процесса равняется давлению насыщенного пара при соответствующей температуре.
Если удельный объем вещества меньше критического ( υ < υкр , изохора I), то изохорное нагревание приводит к полной конденсации пара, в результате чего изохора в p-υ диаграмме пересекает нижнюю погра-
ничную кривую в точке "b". При дальнейшем нагревании вещество будет находиться в однофазном (жидком) состоянии и зависимость между температурой и давлением принимает характерный для жидкости вид - резкий рост давления при незначительном изменении темпе-
ратуры. Если же удельный объем вещества в сосуде υ > υкр (изохора
III), то изохора пересекает верхнюю пограничную кривую в точке "d", т.е. вещество переходит в состояние перегретого пара. При изохорном же нагревании вещества, удельный вес которого равен критическому (изохора II), двухфазное состояние сохраняется вплоть до критической точки "К", где происходит переход вещества в однофазное состояние.
4.3 Описание экспериментальной установки
Для проведения опыта используется экспериментальная установка, состоящая из двух толстостенных стальных сосудов, один из которых показан на рисунке 4.2.
27
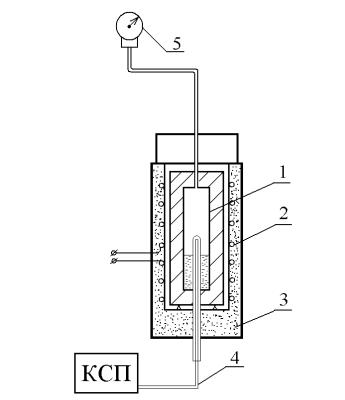
Рисунок 4.2 – Схема экспериментальной установки
В толстостенный сосуд высокого давления 1, изготовленный из нержавеющей стали, залито некоторое количество воды. Снаружи сосуд нагревается электрическим спиральным нагревателем 2. Нагреватель электрически изолирован от сосуда. Сосуд вместе с нагревателем покрыт толстым слоем тепловой изоляции 3 и помещен в металлический кожух.
Температура пара (воды) измеряется хромель-копелевой термопарой 4, горячий спай которой помещен в гильзе, вваренной внутрь сосуда. Для фиксации показаний термопары использован самопишущий потенциометр КСП. Для измерения давления применяется трубчатый манометр 5.
28
4.4 Проведение эксперимента
Включив электронагреватели в обоих сосудах, начинают подогрев воды в них, производя при этом измерение температуры и давления. Для максимального приближения состояния в сосуде к равновесному в каждой точке нагрев ведут медленно, производя одновременные измерения температуры и давления через каждые 10 бар. Количество воды, налитой в сосуды, различно. При этом оно выбрано так, чтобы в одном сосуде удельный объем был меньше критического
( υкр = 0,00317 м3/кг), а в другом сосуде - больше. Поэтому характер изменения давления в сосудах будет различен (рисунок 4.1).
4.5 Обработка результатов опыта
1.В p-t координатах по табличным данным построить кривую насыщения для воды от начальной температуры опыта до критической.
2.На том же графике нанести кривые зависимости P = f (t) для
обоих процессов в 1 и 2 сосуде. При этом необходимо учитывать, что манометр 5 измеряет избыточное давление системы Pизб , а в термодинамические уравнения входит только абсолютное давление Pабс , равное:
Pабс = Pизб + Pб . |
(4.3) |
Атмосферное давление необходимо измерить с помощью лабораторного барометра.
Истинное барометрическое давление вычисляется по формуле:
|
|
Рб = Рбар(1- βрт t) , |
(4.4) |
где Рбар - |
давление, показанное ртутным барометром, градуиро- |
||
|
|
ванным при 0°С; |
|
βрт |
= 1,72 10−4 1/К - коэффициент объемного |
расшире- |
|
t |
ния ртути; |
|
|
- |
температура в помещении, °С. |
|
|
|
|
29 |
|
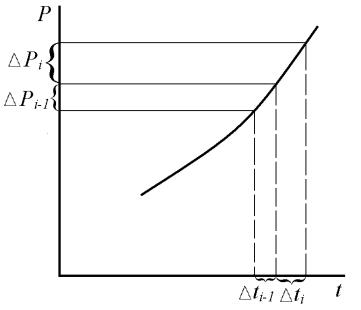
3. На основании формулы Клапейрона-Клаузиуса (4.1) определить приближенную величину теплоты парообразования ri в нескольких точках эксперимента (точки задает преподаватель). Для этого дифференциалы давления и температуры заменяют их конечными приращениями (рисунок 4.3).
Отношение приращения давления к приращению температуры определяют по формуле:
|
∆P |
= |
∆P |
+ ∆P |
|
|
|
|
|
i−1 |
i . |
(4.5) |
|
|
||||||
|
∆T i |
|
∆ti−1 + ∆ti |
|
||
Так как приращения давления на каждом участке равны между собой, то из формулы (4.5) получают
|
∆P |
= |
2∆P |
||
|
|
|
i |
. |
|
|
|
||||
|
∆T i |
|
∆ti−1 + ∆ti |
||
Рисунок 4.3 – График зависимости t от Р
30
