
ТеорИмба
.pdfКачественный анализ. Важнейшей характеристикой любого вещества является положение максимумов полос в ЭМ спектре. Оно определяется только природой вещества и не зависят от его концентрации.
Важнейшим показателем «качества» спектра при этом является ширина полосы. При значительном уширении полосы, полосы соответствующие различным фрагментам молекулы, могут накладываться друг на друга, что в значительной степени затруднит или сделает невозможным их идентификацию.
Количественный анализ. Интенсивность спектральных линий является функцией концентрации вещества и может быть использована в качестве аналитического сигнала. Для удобства в аналитической химии стараются использовать такую характеристику интенсивности спектральной линии, которая была бы прямо пропорциональна концентрации вещества.
Для количественного анализа также важным показателем качества спектра является ширина полосы. При наложении спектральных полос друг на друга значения аналитических сигналов искажаются, что приводит к появлению систематической погрешности при определении содержания вещества.
Инфракрасная спектроскопия
Инфракрасное излучение - это излучение, имеющее частоту меньше, чем частота красного света. Данному излучению соответствуют длины волн от 700 нм до 25000 нм (так называемая ближняя инфракрасная область) и от 25000 до 300000 нм (дальняя ИК-область).
Для перехода атома в возбужденное состояние необходимо, чтобы вещество единовременно поглотило точно фиксированное количество энергии. Из этого следует то, что если на атомы направить излучение с различными частотами, то из всего спектра частот будут избирательно поглощаться только те, которые точно соответствуют энергии, необходимой для перехода атома в какое-либо возбужденное состояние.
Частоты, соответствующие энергетическим переходам, называют резонансными, а явление избирательного поглощения излучения резонансной частоты – явлением резонанса.
7
Возбужденное состояние атома нестабильно, следовательно, он стремится вернуться в основное состояние. Для перехода в основное состояние атом должен испустить фотон с такой же энергией, которая была необходима для перевода его в возбужденное состояние. Такое явление называется эмиссией.
Основные и возбужденные состояния характерны не только для отдельных атомов (где это выражается в переходе электронов на орбитали с большей энергией), но и для двух связанных атомов, отдельной группы атомов или даже молекулы в целом. Данный факт связан с возможностью различных колебательных и вращательных движений атомов и их групп. Усиление или ослабление колебательных движений в соответствии с законами микромира также не может быть плавным. В данном случае присутствует одно состояние с наименьшей энергией (основное) и некоторый набор возбужденных состояний с большей интенсивностью колебаний, а, следовательно, и большей энергией.
Однако для перехода двух связанных атомов с основного на более высокий колебательный энергетический уровень требуется существенно меньшая энергия, чем для перехода электрона в атоме на более высокую орбиталь. Поэтому типичные резонансные частоты излучения, соответствующие колебательновращательным энергетическим переходам связей или частей молекул, находятся в инфракрасной области.
Различные резонансные частоты имеют не только разные пары связанных атомов, но и одинаковые атомы (например, в связи С-Н) в различном окружении (в алкановой цепи, в бензольном кольце или вблизи кислородсодержащих групп). Поэтому определение резонансных частот органического вещества и интенсивностей поглощения излучения на них является эффективным способом анализа не только состава, но и структуры его молекул. Для этого предназначен метод анализа, называющийся инфракрасной (ИК) спектрометрией.
Поглощение веществом инфракрасного излучения обусловлено переходами между колебательными уровнями основного и возбужденного электронного состояния. При этом происходят переходы и между различными вращательными энергетическими уровнями. Поэтому говорят, что ИК-спектры имеют колебательно-вращательную природу.
8
Важно то, что в ИК-спектрах проявляются те колебания, которые сопровождаются изменением дипольного момента молекулы. Колебания двухатомных молекул, таких как О2 и Cl2, дипольные моменты которых равны нулю, а единственно возможным вариантом изменения геометрии является движение атомов вдоль оси связи, называются неактивными в ИК-диапазоне. Для несимметричных двухатомных молекул, имеющих дипольный момент отличный от нуля, колебания атомов относительно оси связи сопровождается поглощением ИКизлучения, и такие колебания называются активными в ИК-диапазоне.
Несмотря на то, что теоретически поглощение должно происходить только при строгом соответствии частоты излучения резонансной частоте атома, связи, или группы атомов в молекуле, на практике это правило соблюдается лишь для сильно разряженных газов.
Колебательные спектры сложных многоатомных молекул богаты полосами поглощения, каждая из которых соответствует возбуждению колебательного состояния определенной части молекулы. Число возможных колебаний молекулы определяется ее структурой. Для молекулы, состоящей из N атомов, число возможных колебаний равно: для нелинейной – 3N-6; для линейной – 3N-5. Некоторые из этих колебаний имеют одинаковые частоты, поэтому соответствующие им полосы поглощения накладываются друг на друга.
В ИК-спектрометрии чаще используется не частота излучения и не длина волны, а так называемое «волновое число».
Волновое число (υ) – число волн излучения, укладывающихся в длину, равную 1 см. ИК-спектр обычно снимается и записывается в координатах пропускание – волновое число.
Пропускание равно отношению интенсивности излучения, прошедшего через вещество к интенсивности излучения падающего на него, выраженному в долях или процентах.
Рассмотрим типы колебательных движений атомов в молекулах. Колебательные движения атомов в молекуле можно разделить на два типа: 1) валентные колебания, когда наблюдается периодическое смещение атомов
вдоль валентной оси связи Х→Y;
9

2) деформационные колебания, при которых происходит изменение величины угла между двумя связями.
Для трехатомных групп состава YXY (например, СН2-групп) характерны 4 типа деформационных колебаний: ножничные, веерные, крутильные и маятниковые (рисунок 1).
Рис. 2. Деформационные колебания групп атомов XYX: а) ножничные; б) веерные; в) крутильные (торзионные); г) маятниковые.
Полосы поглощения, соответствующие веерным и крутильным колебаниям, обычно имеют малую интенсивность. Помимо этого, такие колебания подразделяются на симметричные и асимметричные. Кроме основных резонансных частот существуют составные частоты и обертоны основных колебаний.
Обертоны резонансных частот соответствуют энергии, необходимой для перехода на более высокие колебательные энергетические уровни, и примерно равны основной частоте, умноженной на 2, 3 и так далее. В то же время, даже для первого обертона резонансной частоты (υ об =2 υ) поглощение на данной полосе в десятки раз слабее, чем на основной, поэтому на практике значимы только первый и второй обертоны.
Таким образом, одна группа имеет много резонансных частот, на которых идет поглощение с различной интенсивностью.
Колебания двухатомных молекул
В случае простой двухатомной молекулы А–В присутствует единственный вид колебаний – периодическое растяжение или сжатие вдоль оси валентной связи А→В. Этот процесс приближенно описывается по законам классической физики. В этом случае молекулу рассматривают как гармонический осциллятор с приведенной массой М и силовой константой К. При этом:
M = |
mAmB |
, |
|
||
|
mA + mB |
|
где mA и тB – соответственно масса атомов А и В. 10

При смещении М из положения равновесия на расстояние Δr возникает сила F (рисунок 3), действующая в обратном направлении, пропорциональная изменению расстояния Δr:
F = –KΔr.
Рис. 3. Колебания гармонического осциллятора. При этом частота колебания осциллятора составляет
n = 2p1c 
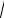 K / M
K / M
Выразив волновое число через частоту колебаний, получим
n- = 21p 
 K / M
K / M
В многоатомных молекулах для отдельных групп атомов (функциональных групп) соотношение приведенной массы и силовой константы связи является практически постоянной величиной. Если это волновое число для какой-либо функциональной группы сильно отличается от параметров остальной части молекулы, то поглощение ЭМИ происходит в узком интервале частот и проявляется в спектрах всех соединений, содержащих эту функциональную группу. Такие полосы в спектрах поглощения называются характеристическими.
По характеристическим полосам поглощения накоплен большой экспериментальный материал, широко используемый для исследований структуры органических соединений.
Влияние массы и силовой константы на частоту колебаний
Частоту колебаний ν определяют два параметра – силовая константа К и приведенная масса М. Из таблицы 2 и 3 видно, что увеличение массы атомов при сохранении порядка связи смещает полосы поглощения в сторону меньших частот,
11

тогда как увеличение значений силовой константы, наоборот, приводит к увеличению частоты колебаний. В многоатомной молекуле дело обстоит намного сложнее, и, тем не менее, эта зависимость помогает грубо оценить области, в которых проявляются отдельные частоты и их характеристичность.
Таблица 2. Зависимость величины волнового числа от приведенной массы
М и при постоянной К. |
|
|
|
Связь |
М, усл. ед. |
К, Н/см |
Волновое число, см-1 |
С-Н |
0,92 |
5,00 |
3000 |
С-С |
6,00 |
4,34 |
1060 |
С-Cl |
9,00 |
3,64 |
700 – 600 |
Таблица 3. Зависимость величины волнового числа от силовой константы К |
|||
при постоянной М. |
|
|
|
Связь |
М, усл. ед. |
К, Н/см |
Волновое число, см-1 |
С-С |
6,0 |
5,0 |
1060 |
С=С |
6,0 |
10,0 |
1600 |
С≡С |
6,0 |
15,0 |
2000 |
С-N |
6,5 |
5,0 |
730 |
С=N |
6,5 |
10,0 |
1650 |
С≡N |
6,5 |
15,0 |
2100 |
Приведенные в таблицах значения волновых чисел рассчитаны приблизительно, так как они зависят не только от М и К, но и от строения молекулы. Практически любое замещение, изменение геометрии молекулы приводит к сдвигу полос поглощения.
Регистрация и интерпретация спектров поглощения органических соединений
По волновым числам типичный ИК-спектр органического вещества может быть условно разделен на четыре участка:
1)более 4000 см-1 – область обертонов и составных частот, редко используется для анализа;
2)4000-1500 см-1 – область валентных колебаний;
12
3)2000-700 см-1 – область деформационных колебаний;
4)1500-400 см-1 – область структурных (скелетных) колебаний – валентных колебаний связи С–С в углеродном скелете, являющихся колебаниями двух отдельных частей молекулы друг относительно друга. Колебания в данной области для сложных веществ часто не поддаются анализу, поскольку структура их необычайно сложна из-за слишком большого количества разных вариаций колеблющихся частей молекулы (анализ возможен лишь для относительно простых веществ или низкомолекулярных производных бензола). Эту область называют областью «отпечатков пальцев» поскольку она строго индивидуальна для каждого вещества и различна даже для очень близких изомеров. Данное явление используется в качественном анализе чистых веществ, поскольку позволяет достоверно определить, что это за вещество путем сравнения его спектра в данной области с эталоном.
Для количественного анализа спектр, построенный в координатах пропускание – волновое число, малопригоден, поскольку высота пика на полосе поглощения и площадь под ним непропорциональны концентрации вещества либо концентрации соответствующей связи или группы в нем.
Как уже было упомянуто ранее, при анализе спектров органических веществ широко используется накопленная справочная информация по резонансным частотам различных функциональных групп в молекуле. Имеющиеся данные сведены в таблицы групповых частот и часто оказываются удобными для качественного анализа строения веществ по инфракрасным спектрам.
Каких-либо строгих правил интерпретации инфракрасных спектров не существует, однако некоторые общие положения могут быть использованы при работе.
Во-первых, требуется точно определить положение полос поглощения в спектре, рассчитав частоты, соответствующие максимуму каждой полосы. Этому должна предшествовать предварительная калибровка прибора по стандартным образцам (например, по полистиролу), так как неправильная настройка может служить источником ошибок.
При предварительном исследовании спектра надо охватывать области валентных и деформационных колебаний групп и, кроме того, область «отпечатков
13
пальцев» (1350–600 см–1), где проявляются частоты, характерные для колебаний конкретных групп.
Появление в спектре полосы поглощения, ожидаемой на основании сведений о строении вещества, еще не является достоверным доказательством наличия в нем соответствующей группы. Необходимо проверить наличие полос поглощения, характерных для этой же группы в других областях спектра. Однако, напротив, отсутствие сильной характеристической полосы поглощения какой-либо группы указывает на отсутствие ее в исследуемом веществе. Так, для области 1750–1650 см–1 характерно сильное поглощение карбонильной группы С=О. Отсутствие поглощения в этой области спектра является доказательством отсутствия данной группы в исследуемом веществе. Если же поглощение в этой области наблюдается, то можно по поглощению в остальных областях спектра определить природу карбонильной группы.
Рассмотрим теперь более подробно характеристические полосы поглощения различных функциональных групп.
Колебания С-Н связи будет зависеть от типа гибридизации атома углерода. Так для sp3-гибридизации валентные колебания метильных групп (-СН3) наблюдаются в виде двух полос поглощения при 2962 и 2872 см-1. Первая – результат антисимметричного валентного колебания (νas CH3). Вторая полоса обусловлена симметричными валентными колебаниями (νs CH3). Наличие нескольких метильных групп приводит к увеличению интенсивности соответствующих полос. Для валентного колебания метиленовых групп (-СН2-) также характерно наличие двух полос поглощения (2962 и 2853 см-1), обусловленных антисимметричными и симметричными валентными колебаниями.
Деформационные колебания связей С-Н проявляется для метильной группы двумя полосами: симметричного деформационного колебания (δs CH3), проявляющееся около 1375 см-1, и антисимметричного деформационного колебание (δas CH3) − в области 1450 см-1. Поглощение при 1375 см-1 является важным критерием подтверждения строения, отсутствуие в спектрах соединений этой полосы говорит о том, что изучаемое соединение не содержит метильной группы.
14

Вметиленовой группе наблюдается четыре типа деформационных колебаний (ножничные, веерные, маятниковые, крутильные) Наиболее информативным из них является поглощение в области 1465 см-1, обусловленное ножничным деформационным колебанием (δs CH2)
Вкачестве примера приведен ИК-спкектр додекана (рисунок 4).
Рис. 4. ИК-спектр додекана.
Валентные колебания C-H (см-1): 2953 (νas CH3), 2870 (νs CH3), 2922 (νas CH2), 2853 (νs CH2);
Деформационные колебания C-H (см-1): 1464 (δs CH2), 1450 (δas CH3), 1379 (δs CH3);
Маятниковое колебание группы CH2: 724 см-1 (pCH2).
Рассмотрим характеристические полосы связи С-Н для углерода, находящегося в sp2-гибридном состоянии, на примере бензольного фрагмента. Для него характерны четыре типа колебаний связей.
Валентные колебания связи С-Н в sp2-гибридном состоянии наблюдаются между 3100 - 3000 см-1. Полосы этих колебаний имеют среднюю интенсивность и обычно представляют собой группу полос;
Скелетные колебания, включая колебания С-С-цикла. Валентные колебания С-С-цикла проявляются в областях 1600 − 1585 и 1500 − 1400 см-1. Полосы скелетных колебаний часто проявляются в виде дублетов в зависимости от природы заместителей в кольце.
Полосы плоскостных колебаний проявляются в области 1300 −1000 см-1.
15

Внеплоскостные деформационные колебания связей С-Н в кольце проявляются в виде интенсивных полос поглощения в области 900 − 675 см-1. Это наиболее информативные полосы поглощения в ИК-спектре ароматических соединений.
Обертоны или составные полосы деформационных колебаний С-Н проявляются в области 2000 − 1650 см-1 в виде полос поглощения с малой интенсивностью.
В качестве примера расмотрим ИК-спкектр о-ксилола (рисунок 5).
Рис. 5. ИК-спектр о-ксилола.
Валентные колебания ароматических С-Н: 3017 см-1; Валентные колебания метильных С-Н: 2970, 1940, 1878 см-1;
Обертоны: 2000 − 1667 см-1; Валентные колебания С-С кольца: 1605, 1497, 1466 см-1;
Плоскостные деформационные колебания С-Н: 1050, 1019 см-1; Внеплоскостные деформационные колебания С-Н: 741 см-1.
Рассмотрим характеристические полосы спиртов.
Гидроксильная группа будет иметь полосы поглощения, связанные с колебаниями связей С-О и О-Н.
Валентные колебания О-Н проявляются в широком интервале частот (3600 − 2500 см-1), Столь широкий диапазон связан с тем, что гидроксильная группа способно образовывать водородные связи. Если водородные связи отсутствуют, а это возможно в разбавленных растворах инертных растворителей, то свободная,
16
