
ConspectMolPhizikaLekzii2013
.pdf
Применение ПНТ к изопроцессам. Изохорический процесс
V=const. Диаграмма этого процесса (изохора) на рисунке 15.
Процесс 1-2 соответствует нагреванию, а процесс 2-1 - охлаждению газа. При изохорическом процессе газ не совершает работы:
и вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии, т.е.
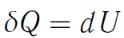 .
.
Рисунок 15.
Согласно формуле (37) для произвольной массы газа
и поэтому
41
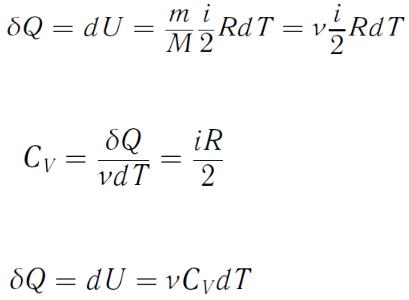
(45),
и тогда молярная теплоемкость при постоянном объеме
(46).
Таким образом,
(47).
42
Изобарический процесс
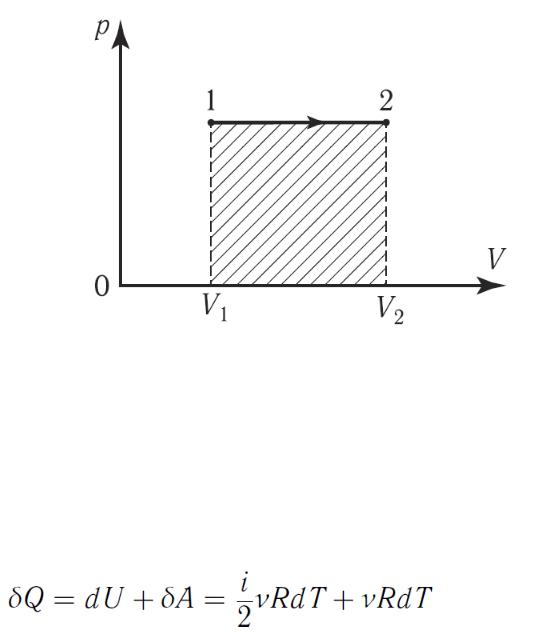
P=const. Диаграмма этого процесса (изобара) на рисунке 16. Он осуществляется при нагревании (процесс 1-2) или охлаждении
(процесс 2-1) газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внешнее давление.
Рисунок 16.
Учитывая, что для произвольной массы газа
U=(i/2) RT, pV= RT,
запишем ПНТ в дифференциальной форме для изобарического процесса:
(48),
Молярная теплоемкость при постоянном давлении
43
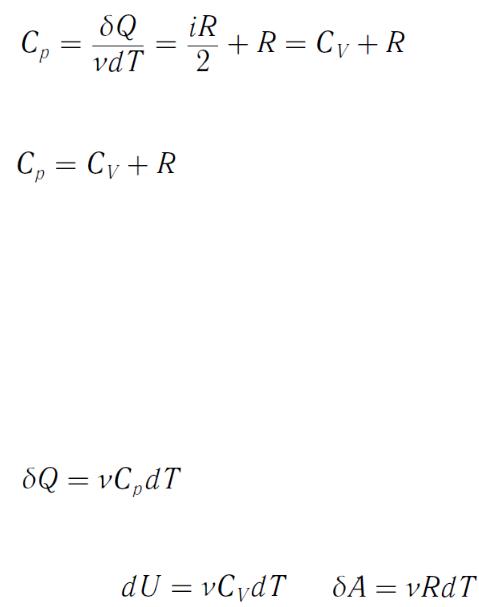
(49).
Выражение
(50)
называется уравнением Майера; оно показывает, что CP всегда больше CV на величину универсальной газовой постоянной R.
Таким образом, физический смысл универсальной газовой постоянной R: она численно равна работе, совершаемой одним молем идеального газа при его изобарическом нагревании на 1 К.
С учетом (49) первое начало термодинамики для изобарического процесса имеет вид
, |
(51) |
кроме того,
, |
. |
44

Изотермический процесс
Т-const. Например, процессы кипения, конденсации, плавления и кристаллизации химически чистых веществ происходят при постоянной температуре, если внешнее давление постоянно.
Рисунок 17.
Для идеального газа при Т=const выполняется закон БойляМариотта
PV=const.
Диаграмма изотермического процесса (изотерма) на рисунке 17.
Внутренняя энергия идеального газа в изотермическом процессе не изменяется, т.е.
dU = νCV dT =0,
так как Т=const и dT=0.
Таким образом, из ПНТ
45

( Q = dU + А)
следует, что Q = А, т.е. вся теплота, сообщаемая газу, расходуется на совершение им работы против внешних сил:
(52),
где =m/M - число молей.
Процесс 1-2 (см. рисунок 17) соответствует изотермическому расширению газа, в этом случае
и 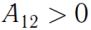 .
.
Обратный процесс 2-1 соответствует изотермическому сжатию газа, для него
и  .
.
46

Адиабатический процесс
Это процесс, при котором отсутствует теплообмен 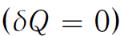 между системой и окружающей средой.
между системой и окружающей средой.
Из ПНТ
для адиабатического процесса следует
т.е. внешняя работа совершается за счет уменьшения внутренней энергии системы.
Учитывая, что
,
работа расширения газа от объема V1 до V2 (температура газа уменьшается от Т1 до Т2):
(53).
Для адиабатического процесса (один моль) ПНТ:
. |
(54) |
Заменив в (54)
,
47
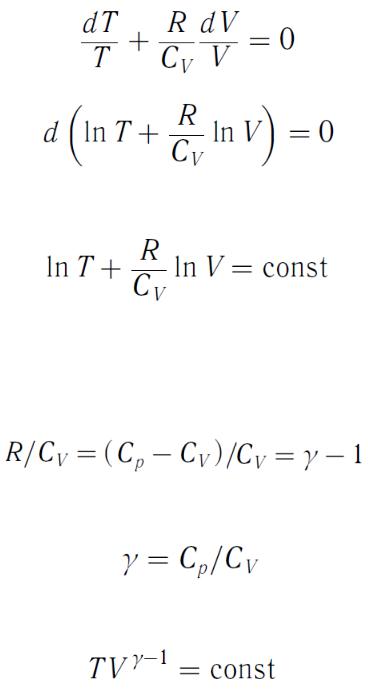
получим
 ;
;
или
;
;
откуда
;
заменим
 ,
,
,
где
получим
,
или используя соотношение
48
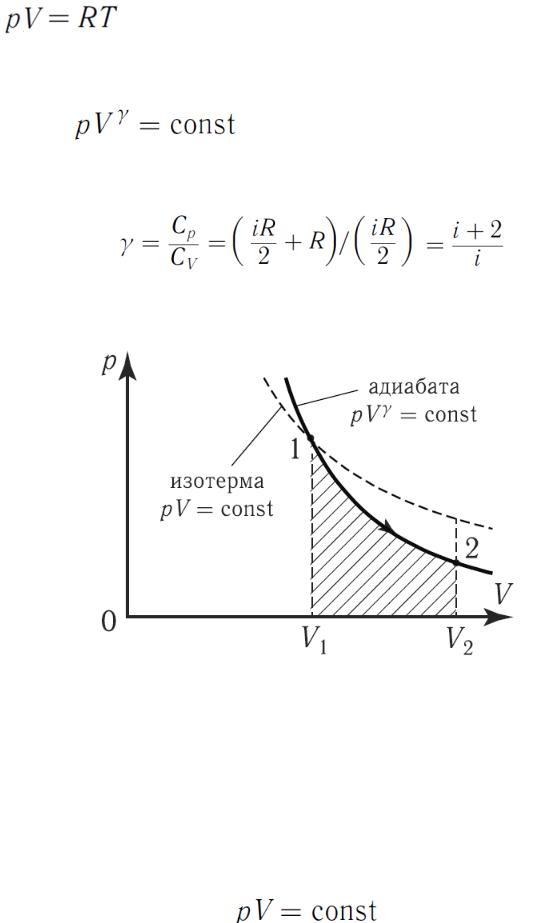
и заменив 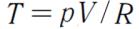
получим
(55).
Это уравнение называют уравнением Пуассона, где
- показатель адиабаты (коэффициент Пуассона).
Рисунок 18.
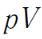 - линия, изображающая адиабатический процесс (рисунок 18), называется адиабатой.
- линия, изображающая адиабатический процесс (рисунок 18), называется адиабатой.
Так как 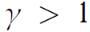 , то адиабата идет круче, чем изотерма, уравнение которой
, то адиабата идет круче, чем изотерма, уравнение которой
.
49
Процесс 1-2 -адиабатическое расширение газа.
В этом случае
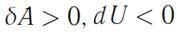 .
.
Процесс 2-1 - адиабатическое сжатие газа.
В этом случае
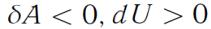 .
.
50
