
- •Работы р.Коха. Их значение в практической микробиологии и инфекционной патологии.
- •Роль отечественных ученых в развитии микробиологической науки (и.И.Мечников, д.И.Ивановский, г.Н.Габричевский, н.Ф.Гамалея, л.А.Зильбер, з.В.Ермольева)
- •Систематика и номенклатура бактерий. Принципы классификации. Понятие о виде как основной номенклатурной единице. Подвид (биовар, хемовар, серовар и др.), культура, популяция. Штамм. Клон.
- •Основные методы исследования морфологии бактерий. Методы микроскопии. Методы окраски микробов и их отдельных структур. (методы Грама, ЦиляНильсена, Бурри-Гинса и др.).
- •Морфология, ультраструктура спирохет. Классификация. Патогенные виды. Методы выявления.
- •8. Облигатные внутриклеточные паразиты: бактерии семейств Ricketsiaceae и Chlamidiaceae. Морфология и ультраструктура. Виды, патогенные для человека.
- •1.R. Prowazekii (1916) – возбудитель эпидемического сыпного тифа и болезни Брилля;
- •4.R. Rickettsii (1922) – возбудитель пятнистой лихорадки Скалистых гор;
- •8.R. Sibirica (1948) – возбудитель северо–азиатского клещевого риккетсиоза;
- •Таксономия.
- •9. Морфология, ультраструктура, классификация микоплазм. Патогенные виды для человека.
- •11. Вирусы бактерий (бактериофаги). Взаимодействие фага с бактериальной клеткой. Культивирование, индикация и титрование фага. Лизогения, фаговая конверсия.
- •12. Типы питания бактерий. Понятие об аутотрофах, гетеротрофах, сапрофитах, прототрофах, ауксотрофах, абсолютных и факультативных паразитах.
- •13. Основные принципы культивирования бактерий. Факторы, влияющие на их рост и размножение. Питательные среды и их классификация.
- •I)Физические
- •II)Химические
- •14. Принципы и методы выделения чистой культуры аэробных бактерий и факультативноанаэробных бактерий.
- •15.Особенности культивирования и выделения чистой культуры анаэробных бактерий. Методы создания анаэробиоза. Микроаэрофилы.
- •1) Посевом в среды, содержащие редуцирующие и легко окисляемые вещества;
- •2) Посевом микроорганизмов в глубину плотных питательных сред;
- •3) Механическим удалением воздуха из сосудов, в которых выращиваются анаэробные микроорганизмы;
- •4) Заменой воздуха в сосудах каким-либо индифферентным газом.
- •16.Методы изучения ферментативной активности бактерий и использование ее для идентификации бактерий.
- •17.Этапы выделения чистых культур бактерий, их идентификация.
- •20. Микрофлора тела человека в различные возрастные периоды. Роль микробов - постоянных обитателей тела человека в физиологических процессах. Причины возникновения дисбактериоза.
- •21. Дисбактериоз. Факторы, влияющие на его формирование, методы изучения. Гнотобионты. Препараты для восстановления нормальной микрофлоры.
- •22. Взаимоотношения между микроорганизмами в ассоциациях: симбиоз, метабиоз, синергизм, антибиотизм. Микробы-антагонисты и их использование в производстве эубиотиков и других лечебных препаратов.
- •23. Понятие об асептике и антисептике. Дезинфекция. Стерилизация. Дробная стерилизация. Методы стерилизации. Контроль качества стерилизации
- •25. Механизмы передачи генетической информации у бактерии (рекомбинации): трансформация, конъюгация, трансдукция. Биологическое значение и практическое применение.
- •26. Микробиологические основы генной инженерии в биотехнологии. Принципы создания гибридных (рекомбинантных) штаммов и их применение в медицине.
- •27. Генетические методы диагностики инфекционных заболеваний: молекулярная гибридизация, полимеразная цепная реакция (пцр).
- •28. Генетика вирусов. Внутривидовой и межвидовой обмен генетическим материалом, его значение в возникновении и течении инфекционных заболеваний???
- •30. Онкогенные вирусы. Современные теории вирусного канцерогенеза. Понятие о протоонкогенах, онкогенах, транспозонах. Рнк-содержащие: семейство Retroviridae, гепатит с.
- •31 .Антибиотики. Классификация,единицы измерения активности.
- •33. Противовирусные (герпетические инфекции, вич) химиотерапевтические препараты и индукторы интерферона. Механизмы их противовирусного действия.
- •34. Ретровирусы. Классификация, особенности структуры и стратегии генома. Заболевания, вызывыемые ретровирусами.
- •1. Период вирусемии.
- •2. Проникновение в клетку-мишень.
- •3. Стадия провируса.
- •4. Активация вирусного генома.
- •5. Фаза персистирующей генерализованной лимфаденопатии.
- •6. Оппортунистические инфекции.
- •Инфекция и иммунитет
- •1. Патогенность и вирулентность микробов. Факторы патогенности: адгезины, ферменты патогенности, факторы иммуносупрессии, микробные токсины. Определение вирулентности, единицы измерения.
- •2. Фазы развития инфекционного процесса: проникновение, адгезия, колонизация, инвазия, повреждение тканей. Динамика развития инфекционного процесса, периоды. Носительство патогенных микробов.
- •3. Инфекция, формы проявления инфекции. Персистенция бактерий, вирусов и др. Микроорганизмов. Понятие о рецидиве, реинфекции, суперинфекции, вторичной инфекции.
- •5. Механические факторы защиты (барьерная функция кожи, слизистых, лимфоузлов). Врожденные механизмы клеточного иммунитета: фагоцитоз, естественные киллеры, дендритические клетки.
- •7. Антигены и их характеристика. Полноценные антигены и гаптены. Изоантигены. Антигенная структура бактериальной клетки (o, VI, k, Hантигены). Групповые и видовые антигены микробов
- •8.Антигенная структура вирусов. Антигены в качестве маркеров вирусов гриппа и вич-вируса. Их роль при лабораторной диагностике инфекций.
- •9. Антитела (иммуноглобулины). Их структура, классы, функции. Неполные антитела. Секреторные иммуноглобулины. Теории антителообразования.
- •10. Понятие о моноклональных антителах. Гибридомная технология для их получения (клеточная инженерия). Применение в медицинской практике.
- •11. Механизмы иммунного ответа. Взаимодействие т- и в-лимфоцитов и макрофагов. Их роль в клеточном и гуморальном иммунитете. Роль цитокинов.
- •12. Противовирусный иммунитет и его особенности. Интерферон, основные свойства, интерфероногены.
- •113. Антитоксины. Принципы получения, очистки, титрования. Применение иммуноглобулинов и антитоксических сывороток в медицине. Побочные действия серотерапии и их профилактика.
- •14. Агглютинины. Реакция агглютинации, ее разновидности. Рига, ронга. Реакция Кумбса (антиглобулиновый тест). Их применение.
- •15. Преципитины. Реакция преципитации, ее разновидности: кольцепреципитация, преципитация в геле, реакция флокуляции, реакция микропреципитации. Применение в медицине.
- •16. Лизины. Реакция бактериолиза и гемолиза. Рск и ее использование в диагностике инфекционных болезней.
- •17. Опсонины. Реакция опсонизации. Роль комплемента в хемотаксисе, опсонизации микробов. Опсонический индекс. Реакция иммобилизации микробов.
- •18. Реакция нейтрализации вирусов, реакция гемагглютинации, реакция торможения гемагглютинации; гемадсорбция, задержки гемадсорбции.
- •19. Гиперчувствительность немедленного типа. Анафилаксия, сывороточная болезнь. Атопии. Механизмы возникновения, методы выявления и предупреждения.
- •20.Гиперчувствительность немедленного типа.Классификация. Сывороточная болезнь, условия ее возникновения, лечение
- •21. Гиперчувствительность замедленного (4-го) типа, механизмы ее возникновения. Инфекционная аллергия. Трансплантационные реакции.
- •22. Практическое использование кожных аллергических проб в диагностике инфекционных болезней.
- •23. Вакцинопрофилактика, типы вакцин, их получение. Адъюванты. Анатоксины, их применение. Вакцинотерапия.
- •24. Серотерапия и серопрофилактика инфекционных болезней, антитоксические и антимикробные сыворотки. Гамма-глобулины гомологичные и гетерологичные, их изготовление и использование.
- •25. Иммунодиагностические реакции с использованием меченых антигенов или антител: реакция иммунофлуоресценции (риф). Применение для экспресс-диагностики инфекционных заболеваний.
- •26. Иммунодиагностические реакции с использованием меченых антигенов или антител: иммуноферментный анализ (ифа).
- •27. Иммуноблотинг как метод серодиагностики инфекционных заболеваний. Выбор метода и принципиальная схема его постановки.
- •Частная
- •5. Псевдомонады. Синегнойная палочка. Биологические свойства. Факторы патогенности. Роль в возникновении внутрибольничных инфекций. Лабораторная диагностика, лечение, профилактика
- •Мероприятия, направленные на источник инфекции:
- •Мероприятия, направленные на прерывание механизма передачи инфекции.
- •Мероприятия, направленные на восприимчивый организм:
- •13. Этиология туляремии. Иммунитет, лабораторная диагностика, лечебные препараты, специфическая профилактика.
- •19. Кампилобактерии, хеликобактерии. Особенности биологии и патогенеза, вызываемых ими заболеваний. Лабораторная диагностика, лечение.
- •20. Возбудитель ботулизма. Характеристика токсинов. Патогенез заболевания. Лабораторная диагностика, специфическая терапия и профилактика.
- •21. Коринебактерии дифтерии. Классификация, свойства. Основные факторы вирулентности, патогенез. Лабораторная диагностика. Иммунитет. Специфическая терапия и профилактика
- •Микобактерии туберкулеза и возбудители микобактериозов, их классификация. Патогенез, лабораторная диагностика, иммунитет, лечебные препараты, специфическая профилактика.
- •23. Возбудитель сифилиса. Патогенез,
- •24. Лептоспиры и вызываемые ими заболевания, лабораторная диагностика, лечебные препараты, специфическая профилактика
- •25. Боррелиозы: болезнь Лайма. Этиология, патогенез, лабораторная диагностика, профилактика.
- •Риккетсии - возбудители эпидемического и эндемического (крысиного) сыпного тифа. Патогенез, иммунитет, лабораторная диагностика. Лечебные препараты, специфическая профилактика.
- •28. Микоплазмы - возбудители пневмонии, острых респираторных заболеваний, уретритов, цервицитов, эндокардитов. Патогенез. Лабораторная диагностика.
- •30. Вирусы гриппа, классификация, изменчивость вирусов гриппа, патогенез, лабораторная диагностика. Иммунитет, специфическая терапия и профилактика.
- •31.Вирус кори, патогенез, иммунитет, специфическая профилактика.
- •32. Вирус паротита. Механизмы заражения. Лабораторная диагностика. Профилактика
- •35. Вирус бешенства, механизм заражения человека, патогенез болезни,лабораторная диагностика. Антирабический гамма-глобулин, антирабическая вакцина, их назначение.
- •36. Понятие об арбовирусных и робовирусных инфекций. Основные возбудители. Вирус клещевого энцефалита. Микробиологическая диагностика. Специфическая профилактика.
- •37.Вирусы гепатитов а и е. Пути передачи возбудителей человеку. Характеристика вирусов. Лабораторная диагностика гепатитаов. Проблема специфической профилактики.
- •38. Вирусы гепатитов в, с ,d, g и пути передачи. Характеристика вирусов. Лабораторная диагностика гепатитов. Профилактика.
- •39. Вирус вич-инфекции: морфология, антигенная структура, механизм заражения, патогенез. Лабораторная диагностика. Лечение. Профилактика,
- •40. Вирус папилломы человека (впч)
- •Виды вакцин против впч: Лечебные вакцины против впч
- •Профилактические вакцины
5. Псевдомонады. Синегнойная палочка. Биологические свойства. Факторы патогенности. Роль в возникновении внутрибольничных инфекций. Лабораторная диагностика, лечение, профилактика
Pseudomonas aeruginosa относится к семейству Pseudomonadaceae. Грам «-»,палочки, Подвижны. Спор не образуют, имеют пили . Могут продуцировать слизь.
Культуральные свойства: облигатные аэробы, которые хорошо растут на простых питательных средах. P. aeruginosa является способность синтезировать водорастворимые пигменты (сине-зеленого цвета), окрашивающие в соответствующий цвет повязки больных .
Биохимические свойства: не ферментирует глюкозу и другие углеводы, обладает протеолитической активностью. Многие штаммы синегнойной палочки продуцируют бактериоцины.
Антигенные свойства: О- и Н-антигены.
Факторы патогенности: 1. Пили, слизь 2. эндотоксин , экзотоксин А , лейкоцидин 3.гемолизины .
Источник: больной. Механизмы заражения: контактный, респираторный, кровяной, фекально – оральный.
Патогенез: проникают через поврежденные ткани. Засевают рану или ожоговую поверхность. Размножаются. Локальные процессы. Бактериемия. Сепсис.
Иммунитет. В сыворотке крови здоровых и переболевших - антитоксические и антибактериальные антитела, однако эти антитела типоспецифические и их роль в защите от повторных заболеваний мало изучена.
Микробиологическая диагностика. Материал для исследования: кровь, гной и раневое отделяемое, моча, мокрота. Основной метод диагностики - бактериологический. При идентификации учитывают рост на агаре, положительный цитохромоксидазный тест. Для внутривидовой идентификации бактерий применяют серотипирование.
Серологический метод (РСК, РПГА.)
Лечение: антибиотики .Тяжелые формы – плазма из крови, иммунизированной поливалентной корпускулярной синегнойной вакциной. Для местного лечения: антисинегнойный гетерологичный иммуноглобулин. Для лечения гнойных инфекций кожи, ожогов – синегнойный бактериофаг.
Профилактика: специфическая – стерилизация, дезинфекция, антисептика. Неспецифическая– иммуномодуляторы. Пассивная специфическая иммунизация гипериммунной плазмой. Для создания активного иммунитета–вакцины(поливалентная корпускулярная синегнойная вакцина,стафило–протейно-синегнойная вакцина.
Занятие: возбудители ВБИ- болезни протекают внутри стационара, при нахождении пациента в течение 28ч.устойчивы к спиртам, аб, дез.ср., характерна природная резистентность.
Эритрогенный токсин:1) пироген 2) нарушает связи между клетками 3) нарушаемость проницаемость мелких клеток сосудов 4) усиливает выработку ИЛ1, он осуществляет связь между макрофагом и т-хэлпером- поликлональная активация т-хэлперов( недифференцированный иммунный ответ)
№6 Эшерихии: физиологическая роль в кишечнике человека, санитарнопоказательное значение, роль в патологии у взрослых и детей. Диареегенные эшерихии, их отличие от условно-патогенных. Лабораторная диагностика энтеральных и парентеральных эшерихиозов
Эшерихиозы — заболевания, возбудителями которых является Escherichia coli. Различают энтеральные (кишечные, эпидемические) эшерихиозы — острые инфекционные болезни, характеризующиеся преимущественным поражением пищеварительного тракта, возбудителями которых являются диареегенные штаммы Е. coli, и парентеральные эшерихиозы, протекающие с поражением любых органов и вызываемые условно-патогенными штаммами
Значение Е. coli. Кишечная палочка — нормальный представитель микрофлоры толстой кишки; выполняет ряд полезных функций, в том числе антагониста патогенных кишечных бактерий, гнилостных бактерий, грибов рода Candida, принимает участие в синтезе витаминов группы В, Е, К2, частично расщепляет клетчатку.
Е. coli используют как санитарно-показательный микроорганизм для выявления фекального загрязнения объектов окружающей среды.
Однако Е. coli может причинить и вред человеку. Условно-патогенные штаммы, обитающие в толстой кишке, при ослаблении иммунной системы организма могут вызвать различные гнойно-воспалительные заболевания за пределами пищеварительного тракта: циститы, отиты, менингиты и даже коли-сепсис. Эти заболевания называют парентеральными эшерихиозами.
Существуют также и безусловно патогенные штаммы Е. coli — диареегенные, или энтеропатогенные, кишечные палочки (ЭПКП), которые, попадая в организм извне, вызывают вспышки заболеваний, именуемых энтеральными (кишечными, эпидемическими) эшерихиозами.Е. coli может быть причиной пищевой токсикоинфекции.
Таксономия. Е. coli — основной представитель рода Escherichia, семейства Enterobacteriaceae, входящего в отдел Gracilicutes.
Морфология и тинкториальные свойства. Е. coli — мелкие грамотрицательные палочки длиной 2—3 мкм, шириной 0,5—0,7 мкм с закругленными концами, в мазках располагаются беспорядочно (рис. 10.1); не образуют спор, некоторые штаммы имеют микрокапсулу; перитрихи; кроме жгутиков, иногда обнаруживаются пили.
Культивирование. Кишечная палочка — факультативный анаэроб; не требовательна к питательным средам, хорошо растет на простых питательных средах при температуре 37 °С и рН среды 7,2—-7,4, вызывая диффузное помутнение жидкой среды и образуя обычные колонии на плотных средах. Для диагностики эшерихиозов широко используют дифференциально-диагностические среды Эндо, Левина и др.
Ферментативная активность. Е. coli обладает высокой ферментативной активностью. Кишечная палочка — представитель семейства Enterobacteriaceae, расщепляющий в течение 24 ч лактозу.
Антигенная структура. Кишечная палочка обладает соматическим (О), жгутиковым (Н) и поверхностным (К) антигенами. Каждый из антигенов неоднороден: О-антиген насчитывает более 170 вариантов, К-антиген — более 100, Н-антиген — более 50. Строение О-антигена определяет принадлежность к серогруппе. Штамм, имеющий свой набор антигенов, свою антигенную формулу, называется серологическим вариантом Е. coli. Например, штамм О55:К5:Н21 относится к серогруппе 055.
Факторы патогенности. Е. coli образует эндотоксин, оказывающий энтеротропное, нейротропное, пирогенное действие (ЭПКП). ЭПКП продуцирует экзотоксин, который, адсорбируясь на эпителии тонкой кишки, вызывает гиперсекрецию воды и хлоридов в просвет тонкой кишки и нарушает обратное всасывание натрия, что приводит к усилению перистальтики, поносу и обезвоживанию. У некоторых диареегенных эшерихий, как и у возбудителей дизентерии, обнаружен инвазивный фактор, способствующий проникновению бактерий внутрь клеток. Патогенность ЭПКП также может проявляться в нефротоксическом действии, возникновении геморрагии. К факторам патогенности относятся также пили и белки, способствующие адгезии, и микрокапсула, препятствующая фагоцитозу. Условно-патогенные и диареегенные кишечные палочки отличаются антигенной структурой и набором факторов патогенности.
Резистентность. Среди других энтеробактерий Е. coli отличается более высокой резистентностью к действию различных факторов окружающей среды.
Эпидемиология энтеральных эшерихиозов (парентеральные эшерихиозы — см. раздел 13.1.7). Источником энтеральных эшерихиозов являются больные люди и животные. Механизм передачи инфекции фекально-оральный, основные пути передачи — пищевой, контактно-бытовой. Заболевание чаще носит характер вспышек.
Патогенез. Входные ворота инфекции — полость рта. Е. coli, попадая в тонкую кишку и обладая тропизмом к клеткам ее эпителия, адсорбируется на них с помощью пилей и белков наружной мембраны. Бактерии размножаются, погибают, освобождая эндотоксин, который усиливает перистальтику кишечника, вызывает диарею, повышение температуры, признаки общей интоксикации. Кроме того, кишечная палочка выделяет экзотоксин, обусловливающий более тяжелую диарею, рвоту и значительное нарушение водно-солевого обмена. ЭПКП, образующие другие факторы патогенности, оказывают соответствующее действие на организм, что и определяет клиническую картину болезни.
Клиническая картина. Инкубационный период продолжается от 2 до 6 дней. Заболевание начинается остро с повышения температуры тела, поноса, рвоты. Развивается обезвоживание, могут появиться кровь в испражнениях, признаки поражения почек. Формы энтеральных эшерихиозов могут быть различные — от бессимптомной до токсико-септической. Колиэнтериты являются одной из причин ранней детской смертности.
Иммунитет после перенесенного заболевания непрочный и непродолжительный.
Микробиологическая диагностика. Основной материал для исследования — испражнения. Диагностика осуществляется с помощью бактериологического метода, при котором не только определяют род и вид выделенной чистой культуры, но и устанавливают принадлежность ее к серогруппе; внутривидовая идентификация заключается в определении серовара; обязательно определение антибиотикограммы.
Лечение. Для лечения заболеваний, вызываемых Е. coli, используют антибиотики.
Профилактика. Проведение санитарно-гигиенических мероприятий.
Патогенез и клинические проявления.
Диареегенные серовары кишечной палочки разделены на 5 групп:
* Энтеропатогенные (ЭПКП);
* Энтеротоксигенные (ЭТКП);
* Энтероинвазивные (ЭИКП);
* Энтерогеморрагические (ЭГКП);
* Энтероадгезивные (ЭАКП).
Кроме вышеперечисленных выделяют диффузноприлипаемые кишечные палочки (пока недостаточно изучены).
Морфологически представители разных групп не отличимы друг от друга; их дифференцируют по антигенной структуре и по факторам патогенности.
ЭПКП – вызывают эшерихиозы у детей до 1 года (чаще у детей, находящихся на искусственном вскармливании). Возбудители поражают эпителий тонкого кишечника: адсорбируясь на поверхности энтероцитов за счет белка наружной мембраны (интимина), размножаются здесь и повреждают микроворсинки, вызывая их отторжение. Развивающаяся при этом воспалительная реакция обусловлена действием эндотоскина, который освобождается при разрушении кишечных палочек. Основные клинические проявления: диарея, рвота, срыгивание пищи, признаки обезвоживания организма, гипотрофия. Течение болезни – тяжелое, может длиться неделями.
ЭТКП вызывают холероподобные заболевания у детей и взрослых. При помощи пилей они прикрепляются к эпителию нижних отделов тонкого кишечника, размножаются благодаря CF (фактор колонизации) и продуцируют 2 типа токсинов: LT (термолабильный, по механизму действия напоминает экзотоксин холерного вибриона) и ST (термостабильный). LT и ST увеличивают в клетках эпителия содержание цАМФ и цГМФ соответственно, что вызывает нарушение транспорта молекулярного железа и повышенному выходу воды из клеток. Это нарушает водно-солевой баланс в кишечнике и приводит к развитию водянистой диареи. Заболевание по характеру течения напоминает легкую форму холеры (в литературе его часто называют диареей путешественников).
ЭИКП вызывают дизентериеподобное заболевание у детей и взрослых. Адсорбируются на клетках эпителия нижних отделов толстой кишки, проникают внутрь клеток, размножаются, выделяют шигеллоподобный токсин и разрушают клетки. Распространяясь по межклеточным пространствам, они поражают соседние клетки, образуя язвы. Клинические симптомы: вначале – водянистая диарея, затем в испражнениях появляется примесь слизи и крови.
ЭГКП – возбудители геморрагической диареи и гемолитического уремического синдрома, поражая преимущественно детей. Возбудители выделяют шигелоподобный цитотоксин, вызывающий разрушение эндотелия сосудов (блокирует синтез белков на рибосомах) кишечника и почек, в результате чего развиваются ишемия и некроз клеток. Клинически наблюдается геморрагический колит (кровавый понос) и гемолитический уремический синдром (гемолитическая анемия и почечная недостаточность), которые протекают тяжело и нередко с летальным исходом.
ЭАКП (описаны в 1985 г.у) способны быстро прикрепляться к поверхности клеток и колонизировать разные отделы кишечника, но чаще поражают толстую кишку. Цитотоксинов они не образуют, в клетки не проникают. Клинически заболевание характеризуется упорным диарейным синдромом.
№7 Сальмонеллы брюшного тифа и паратифов. Патогенез, лабораторная диагностика. Иммунитет. Лечебные препараты, специфическая профилактика, выявление носителей.
Брюшной тиф и паратифы А и В — инфекционные болезни, вызываемые соответственно Salmonella typhi, Salmonella paratyphi, Salmonella schottmuelleri, сопровождающиеся сходными патогенетическими и клиническими проявлениями, характеризующиесяпоражением лимфатической системы кишечника, выраженной интоксикацией.
Таксономия. Возбудители брюшного тифа и паратифов А и В относятся к отделу Gracilicutes, семейству Enterobacteriaceae, роду Salmonella, включающему более 2000 видов.
Морфология и тинкториальные свойства. Сальмонеллы — мелкие, длиной 2—3 мкм, шириной 0,5—0,7 мкм, грамотрицательные палочки с закругленными концами. В мазках располагаются беспорядочно. Не образуют спор, имеют микрокапсулу, перитрихи.
Культивирование. Сальмонеллы — факультативные анаэробы. Они неприхотливы и растут без всяких особенностей на простых питательных средах при температуре 37 °С и рН среды 7,2— 7,4. Элективной средой является, например, желчный бульон. При диагностике брюшного тифа, как и других кишечных инфекций, используют дифференциально-диагностические среды: Эндо, Левина, висмут-сульфитный агар и др.
Ферментативная активность. Биохимическая активность сальмонелл достаточно высока, но они обладают меньшим набором ферментов, чем Е. coli, в частности не сбраживают лактозу. S. typhi менее активна, чем возбудители паратифов: она ферментирует ряд углеводов без образования газа.
Антигенные свойства. Сальмонеллы имеют О- и Н-антигены, состоящие из ряда фракций, или рецепторов. Каждый вид имеет определенный набор фракций. Ф. Кауфман и П.Уайт предложили схему классификации сальмонелл по антигенной структуре, в основу которой положено строение О-антигена. Все виды сальмонелл, имеющие общий, так называемый групповой, рецептор О-антигена, объединены в одну группу. Таких групп насчитывается в настоящее время 65. В схеме также указано строение Н-антигена. Некоторые виды сальмонелл, в том числе S. typhi, имеют поверхностный Vi-антиген — антиген вирулентности, с которым связана устойчивость бактерий к фагоцитозу.
Факторы патогенности. Сальмонеллы образуют эндотоксин, оказывающий энтеротропное, нейротропное и пирогенное действие. Белки наружной мембраны обусловливают адгезивные свойства, устойчивость к фагоцитозу связана с микрокапсулой.
Резистентность. Сальмонеллы довольно устойчивы к низкой температуре — в холодной чистой воде могут сохраняться до полутора лет; очень чувствительны к дезинфицирующим средствам, высокой температуре, УФ-лучам. В пищевых продуктах (мясе, молоке и др.) сальмонеллы могут не только долго сохраняться, но и размножаться.
Эпидемиология. Источником брюшного тифа и паратифов являются больные люди и носители. Механизм передачи инфекции — фекально-оральный. Преобладает водный путь передачи, реже встречаются пищевой и контактно-бытовой пути. Брюшной тиф и паратифы — заболевания, которые регистрируются в разных странах мира. Чаще болеют люди в возрасте от 15 до 30 лет. Наиболее высокая заболеваемость отмечается летом и осенью.
Патогенез. Возбудители попадают в организм через рот, достигают тонкой кишки, в лимфатических образованиях которой размножаются, а затем попадают в кровь. Током крови они разносятся по всему организму, внедряясь в паренхиматозные органы (селезенку, печень, почки, костный мозг). При гибели бактерий освобождается эндотоксин, вызывающий интоксикацию. Из желчного пузыря, где сальмонеллы могут длительно, даже в течение всей жизни сохраняться, они вновь попадают в те же лимфатические образования тонкой кишки. В результате повторного поступления сальмонелл может развиться своеобразная аллергическая реакция, проявляющаяся в виде воспаления, а затем некроза лимфатических образований. Выводятся сальмонеллы из организма с мочой и испражнениями.
Клиническая картина. Клинически брюшной тиф и паратифы не отличимы. Инкубационный период продолжается 12—14 дней. Заболевание обычно начинается остро с повышения температуры тела, проявления слабости, утомляемости, нарушаются сон, аппетит. Для брюшного тифа характерны помрачение сознания (от греч. typhus — дым, туман), бред, галлюцинации, наличие сыпи. Очень тяжелыми осложнениями заболевания являются перитонит, кишечное кровотечение в результате некроза лимфатических образований тонкой кишки.
Иммунитет. После перенесенного заболевания вырабатывается прочный и продолжительный иммунитет.
Микробиологическая диагностика. В качестве материала для исследования используют кровь, мочу, испражнения. Основным методом диагностики является бактериологический, завершающийся внутривидовой идентификацией вьщеленнои чистой культуры возбудителя — определением фаговара. Применяют также серологический метод — реакцию агглютинации Видаля, РИГА.
Лечение. Назначают антибиотики. Применяют также иммуноантибиотикотерапию.
Профилактика. Для профилактики проводят санитарно-гигиенические мероприятия, а также используют вакцинацию в районах с неблагополучной эпидемической обстановкой. Применяют брюшнотифозную химическую и брюшнотифозную спиртовую вакцины, последняя обогащена Vi-антигеном. Для экстренной профилактики в очагах инфекции используют брюшнотифозный бактериофаг (в виде таблеток с кислотоустойчивой оболочкой и в жидком виде).
№8. Возбудители пищевых токсикоинфекций (сальмонеллы, клебсиеллы, протеи, эшерихии, вибрионы и др.) и бактериальных интоксикаций (стафилококки, клостридии). Особенности патогенеза. Лабораторная диагностика. Сальмонеллы – возбудители токсикоинфекций и внутрибольничных сальмонеллезов.
Сальмонеллез — острая кишечная инфекция, характеризующаяся преимущественным поражением желудочно-кишечного тракта, возбудителями которой являются многочисленные бактерии из рода Salmonella (кроме S. typhi, S. paratyphi A, S. schottmuelleri). Род Salmonella содержит более 2000 видов, большая часть которых может стать причиной сальмонеллезов. Чаще других обнаруживаются Salmonella typhimurium, S. enteritidis, S. heidelberg, S. newport.
Таксономия. Возбудители брюшного тифа и паратифов А и В относятся к отделу Gracilicutes, семейству Enterobacteriaceae, роду Salmonella, включающему более 2000 видов.
Эпидемиология. Основной источник заболевания — животные, преимущественно домашние (крупный и мелкий рогатый скот, свиньи и др.) и птицы (куры, утки, гуси и др.). Носителями сальмонелл могут быть и другие представители фауны: мыши, голуби, черепахи, устрицы, тараканы и др. Реже источниками заболевания являются люди — больные и носители. Механизм заражения — фекально-оральный. Основной путь передачи инфекции — пищевой. Факторами передачи могут быть не только мясо животных и птиц, инфицированное при жизни животного либо при его обработке, но и яйца. Наиболее восприимчивы к заболеванию люди со сниженным иммунным статусом (в том числе грудные дети) и больные, получающие антибиотики. Заболевание широко распространено на всех континентах. Подъем заболеваемости наблюдается летом.
Патогенез. Сальмонеллы проникают в организм через рот, достигают тонкого кишечника, где и развертывается патологический процесс. Бактерии благодаря факторам адгезии прикрепляются к слизистой оболочке, проникают в ее глубокие слои, где захватываются макрофагами. Сальмонеллы размножаются и погибают с освобождением эндотоксина, который, помимо общей интоксикации, вызывает диарею и нарушение водно-солевого обмена. Находящаяся в нормальном состоянии микрофлора кишечника в значительной мере препятствует накоплению сальмонелл. В некоторых случаях (при снижении иммунного статуса и высокой вирулентности возбудителя) возможно развитие бактериемии и поражение костей, суставов, мозговых оболочек и других органов.
Клиника. Инкубационный период равен в среднем 12—24 ч. Заболевание характеризуется повышением температуры, тошнотой, рвотой, поносом, болью в животе. Как правило, продолжительность болезни составляет 7 дней. Но в некоторых случаях наблюдается молниеносная токсическая форма, приводящая к смерти больного.
Иммунитет после перенесенного заболевания сохраняется менее года.
Микробиологическая диагностика. В качестве основного материала для исследования используют рвотные массы, испражнения, промывные воды желудка. Применяют бактериологический и серологический (РА, РПГА) методы диагностики.
Лечение сальмонеллеза заключается в промывании желудка, диете, введении жидкостей для нормализации водно-солевого обмена. Антибиотики при формах средней тяжести и легких не назначают, так как их применение приводит к дисбактериозу и в результате более длительному течению болезни; кроме того, очень велико число антибиотикорезистентных сальмонелл.
Профилактика неспецифическая — санитарно-гигиенические мероприятия, заключающиеся, в частности, в правильной кулинарной обработке мяса и яиц.
Возбудители пищевых токсикоинфекций и интоксикаций. Лабораторная диагностика. Особенности патогенеза.
Пищевые токсикоинфекций — острые болезни, возникающие в результате употребления пищи, инфицированной микроорганизмами, и характеризующиеся симптомами гастроэнтерита и нарушением водно-солевого обмена. В том случае, если для развития болезни достаточно попадания в организм с пищей лишь токсинов микробов, говорят о пищевых интоксикациях.
Этиология. Возбудителями пищевых токсикоинфекции являются различные условно-патогенные бактерии — Escherichia coli, Clostridium perfringens, Bacillus cereus, некоторые виды протея, клебсиелл, вибрионов, энтерококков и др.; к возбудителям интоксикаций относятся Clostridium botulinum, стафилококки, некоторые грибы.
Факторы патогенности. Возбудители пищевых токсикоинфекции продуцируют как эндо-, так и экзотоксины. Эндотоксины оказывают энтеротропное, нейротропное действие, повышают температуру тела, вызывают головную боль, недомогание и другие симптомы общей интоксикации. Экзотоксины обладают энтеротоксическими и цитотоксическими свойствами. В результате действия энтеротоксина усиливается секреция жидкости и солей в просвет кишечника, развивается диарея, с чем связано нарушение водно-солевого обмена. Цитотоксический эффект заключается в повреждении клеток эпителия слизистой оболочки пищеварительного тракта, в которой происходят воспалительные изменения. Патогенность возбудителей пищевых токсикоинфекции связана также с наличием капсулы, пилей у некоторых из них, выработкой ферментов агрессии.
Резистентность. Возбудители пищевых токсикоинфекции обладают достаточно высокой устойчивостью к действию различных факторов окружающей среды и могут довольно длительно сохраняться в различных пищевых продуктах. Для их уничтожения требуется длительная термическая обработка. Очень высокой резистентностью характеризуются спорообразующие бактерии — представители родов Bacillus и Clostridium.
Эпидемиология. Острые пищевые токсикоинфекции — заболевания, распространенные повсеместно. Болеют ими люди разных возрастов. Восприимчивость различна и зависит от дозы возбудителя, иммунного статуса человека, употребившего инфицированные продукты. Уровень заболеваемости увеличивается в теплое время года, что связано с благоприятными условиями для размножения микробов в продуктах. Источником инфекции могут быть животные и люди, выделяющие большую часть возбудителей пищевых токсикоинфекции с испражнениями. Из-за широкого распространения возбудителей в почве, воде, на различных предметах источник инфекции чаще всего установить трудно. Механизм передачи инфекции — фекально-оральный. Путь передачи — пищевой. Употребление самых разных продуктов может привести к развитию пищевой токсикоинфекции или интоксикации. В мясе, рыбе могут содержаться, например, протей, молочные продукты (сметана, мороженое, крем) являются наиболее благоприятной питательной средой для стафилококков, но в этих же продуктах, так же как и во многих других, могут находиться и другие микроорганизмы. Нередко продукты, инфицированные микроорганизмами, могут быть внешне не изменены.
Патогенез. Особенностью пищевых токсикоинфекций является способность возбудителей продуцировать экзо- и эндотоксины не только в организме человека, но и в пищевых продуктах, чем и объясняется короткий инкубационный период. Развитие стафилококковой пищевой интоксикации обусловлено лишь попаданием в организм экзотоксина. В результате действия освобождающегося при гибели бактерий эндотоксина повышается температура тела, ухудшается самочувствие, могут возникнуть нарушения сердечно-сосудистой, нервной систем и др. Экзотоксины вызывают поражение пищеварительного тракта и нарушение водно-солевого обмена.
Клиническая картина. Инкубационный период составляет от 2 до 24 ч. Заболевание начинается остро с кратковременного повышения температуры тела, озноба, слабости, появляются тошнота, рвота, боли в животе, понос. Как правило, заболевание продолжается 1—7 дней и заканчивается выздоровлением. Но возможны и молниеносные токсические формы, приводящие к летальному исходу.
Иммунитет. После перенесенного заболевания иммунитет непрочный и непродолжительный.
Микробиологическая диагностика. Материалом для исследования являются рвотные массы, промывные воды желудка, испражнения, остатки пищи. Для диагностики используют бактериологический метод.
Лечение. При острых пищевых токсикоинфекциях прежде всего назначают неспецифическое лечение — промывание желудка. Применение химиопрепаратов при неосЛожненном течении нецелесообразно.
Профилактика. Соблюдение санитарно-гигиенических норм при приготовлении и хранении пищи.
№9Характеристика и классификация шигелл, патогенез, лабораторная диагностика шигеллезов, иммунитет. Эпидемиология, профилактика и лечение дизентерии.
Бактериальная дизентерия, или шигеллез, — инфекционное заболевание, вызываемое бактериями рода Shigella, протекающее с преимущественным поражением толстой кишки. Название рода связано с К.Шиги, открывшего одного из возбудителей дизентерии.
Таксономия и классификация. Возбудители дизентерии относятся к отделу Gracilicutes, семейству Enterobacteriaceae, роду Shigella.
Группа А S dysenteriae
Группа Б S.flexnerii
Группа С S.boydii
Группа Д S. sonnei
Морфология и тинкториальные свойства. Шигеллы — грамотрицательные палочки с закругленными концами, длиной 2—3 мкм, толщиной 0,5—7 мкм (см. рис. 10.1); не образуют спор, не имеют жгутиков, неподвижны. У многих штаммов обнаруживают ворсинки общего типа и половые пили. Некоторые шигеллы обладают микрокапсулой.
Культивирование. Дизентерийные палочки — факультативные анаэробы. Они нетребовательны к питательным средам, хорошо растут при температуре 37 °С и рН среды 7,2—7,4. На плотных средах образуют мелкие прозрачные колонии, в жидких средах —
диффузное помутнение. В качестве среды обогащения для культивирования шигелл чаще всего используют селенитовый бульон.
Ферментативная активность. Шигеллы обладают меньшей ферментативной активностью, чем другие энтеробактерии. Углеводы они сбраживают с образованием кислоты. Важным признаком, позволяющим дифференцировать шигеллы, является их отношение к манниту: S. dysenteriae не ферментируют маннит, представители групп В, С, D маннитпозитивны. Наиболее биохимически активны S. sonnei, которые медленно (в течение 2 сут) могут сбраживать лактозу. На основании отношения S. sonnei к рамнозе, ксилозе и мальтозе различают 7 биохимических вариантов ее.
Антигенная структура. Шигеллы имеют О-антиген, его неоднородность позволяет выделять внутри групп серовары и подсеровары; у некоторых представителей рода обнаруживают К-антиген.
Факторы патогенности. Все дизентерийные палочки образуют эндотоксин, оказывающий энтеротропное, нейротропное, пирогенное действие. Кроме того, S. dysenteriae (серовар I) — шигеллы Григорьева—Шиги — выделяют экзотоксин, оказывающий энтеротоксическое, нейротоксическое, цитотоксическое и нефротоксическое действие на организм, что соответственно нарушает водно-солевой обмен и деятельность ЦНС, приводит к гибели эпителиальных клеток толстой кишки, поражению почечных канальцев. С образованием экзотоксина связано более тяжелое течение дизентерии, вызванной данным возбудителем. Экзотоксин могут выделять и другие виды шигелл. Обнаружен фактор проницаемости RF, в результате действия которого поражаются кровеносные сосуды. К факторам патогенности относятся также инвазивный белок, способствующий их проникновению внутрь эпителиальных клеток, а также пили и белки наружной мембраны, ответственные за адгезию, и микрокапсула.
Резистентность. Шигеллы обладают невысокой устойчивостью к действию различных факторов. Большей резистентностью обладают S. sonnei, которые в водопроводной воде сохраняются до 2'/2 мес, в воде открытых водоемов выживают до V/2 мес. S. sonnei могут не только достаточно долго сохраняться, но и размножаться в продуктах, особенно молочных.
Эпидемиология. Дизентерия — антропонозная инфекция: источником являются больные люди и носители. Механизм передачи инфекций — фекально-оральный. Пути передачи могут быть различные — при дизентерии Зонне преобладает пищевой путь, при дизентерии Флекснера — водный, для дизентерии Григорьева—Шиги характерен контактно-бытовой путь. Дизентерия встречается во многих странах мира. В последние
годы наблюдается резкий подъем заболеваемости этой инфекцией. Болеют люди всех возрастов, но наиболее подвержены дизентерии дети от 1 года до 3 лет. Количество больных увеличивается в июле — сентябре. Различные виды шигелл по отдельным
регионам распространены неравномерно.
Патогенез. Шигеллы через рот попадают в желудочно-кишечный тракт и достигают толстой кишки. Обладая тропизмом к ее эпителию, с помощью пилей и белков наружной мембраны возбудители прикрепляются к клеткам. Благодаря инвазивному фактору они проникают внутрь клеток, размножаются там, в результате чего клетки погибают. В стенке кишечника образуются изъязвления, на месте которых затем формируются рубцы. Эндотоксин, освобождающийся при разрушении бактерий, вызывает общую интоксикацию, усиление перистальтики кишечника, понос. Кровь из образовавшихся язвочек попадает в испражнения. В результате действия экзотоксина наблюдается более выраженное нарушение водно-солевого обмена, деятельности ЦНС, поражение почек.
Клиническая картина. Инкубационный период длится от 1 до 5 дней. Заболевание начинается остро с повышения температуры тела до 38—39 °С, появляются боль в животе, понос. В стуле обнаруживают примесь крови, слизь. Наиболее тяжело протекает дизентерия Григорьева—Шиги.
Иммунитет. После перенесенного заболевания иммунитет не только видо-, но и вариантоспецифичен. Он непродолжителен и непрочен. Нередко заболевание переходит в хроническую форму.
Микробиологическая диагностика. В качестве исследуемого материала берут испражнения больного. Основой диагностики является бактериологический метод, позволяющий идентифицировать возбудителя, определить его чувствительность к
антибиотикам, провести внутривидовую идентификацию (определить биохимический вариант, серо вар или колициногеновар). При затяжном течении дизентерии можно использовать как вспомогательный серологический метод, заключающийся в постановке РА, РНГА (по нарастанию титра антител при повторной постановке реакции можно подтвердить диагноз).
Лечение. Больных тяжелыми формами дизентерии Григорьева—Шиги и Флекснера лечат антибиотиками широкого спектра действия с обязательным учетом антибиотикограммы, так как среди шигелл нередко встречаются не только антибиотикоустойчивые, но и антибиотикозависимые формы. При легких формах дизентерии антибиотики не используют, поскольку их применение приводит к дисбактериозу, что утяжеляет патологический процесс, и нарушению восстановительных процессов в слизистой оболочке толстой кишки.
Профилактика. Единственный препарат, который может быть использован в очагах инфекции с профилактической целью, — дизентерийный бактериофаг. Основную роль играет неспецифическая профилактика.
Клебсиеллы. Свойства. Антигены. Этиологическая роль в возникновении склеромы, озены, пневмонии. Роль внутрибольничной инфекции, лабораторная диагностика.
Название дано в честь Э. Клебса. К роду Klebsiella относятся два вида: Klebsiella pneumoniae и Enterobacter. Первый вид подразделен на два подвида: К. ozenae, К. rinoscleromatis.
Морфологические свойства представители вида Klebsiella pneumoniae - короткие, толстые, неподвижные грамотрицательные палочки, образующие в отличие от других энтеробактерий выраженные полисахаридные капсулы.
Культуральные Клебсиеллы, так же как другие энтеробактерий, нетребовательны к питательным средам. Они ферментируют глюкозу с кислотой и газом и используют ее и цитрат в качестве единственного источника углерода, а аммиак - источника азота. Подвиды клебсиелл различают по биохимическим признакам. В отличие от вида Enterobacter, К. pneumoniae лишены жгутиков, не синтезируют орнитиндекарбоксилазу, ферментируют сорбит. Дифференциация разных видов клебсиелл проводится на основании их неодинаковой способности ферментировать углеводы, образовывать уреазу и лизиндекарбоксилазу, утилизировать цитрат и других признаков. Клебсиеллы образуют слизистые колонии.
Антигены: Клебсиеллы содержат О- и К-антигены.
Патогенность и патогенез. Вирулентность клебсиелл пневмонии обусловлена их адгезией, связанной с капсульным полисахаридом, пилями и белком наружной мембраны, последующим размножением и колонизацией энтероцитов. Капсула также защищает бактерии от действия фагоцитирующих клеток. При разрушении бактериальных клеток освобождается эндотоксин (ЛПС). Кроме того, клебсиеллы пневмонии секретируют термостабильный энтеротоксин, усиливающий выпот жидкости в просвет тонкой кишки, что играет существенную роль в патогенезе ОКЗ, и мембранотоксин с гемолитической активностью. Клебсиеллы являются возбудителями пневмонии, ОКЗ, риносклеромы, озены. Они также могут вызывать поражения мочеполовых органов, мозговых оболочек взрослых и детей, токсико-сеп-тические состояния и ОКЗ у новорожденных. Клебсиеллы могут вызывать внутрибольничные инфекции. Для пневмонии, вызванной К. pneumoniae, характерны образование множественных очагов в дольках легкого с последующим их слиянием и ослизнением пораженной ткани, содержащей большое количество клебсиелл. Возможно образование гнойных очагов в других органах и развитие сепсиса. При склероме, вызванной К. rhinoscleromatis, поражается слизистая оболочка носа (риносклерома), носоглотки, трахеи, бронхов. В тканях образуются гранулемы с последующими склеротическими изменениями. При озене, вызванной К. ozenae, поражается слизистая оболочка носа и придаточных полостей с последующей атрофией носовых раковин и выделением зловонного секрета.
Иммунитет. Клебсиеллы вызывают гуморальный и клеточный иммунный ответ. Однако образующиеся антитела не обладают про-тектиными свойствами. Развитие ГЗТ связано с внутриклеточной локализацией клебсиелл.
Экология и эпидемиология. Клебсиеллез является антропонозной инфекцией. Источник инфекции - больные и носители. Заражение происходит через респираторные пути. Клебсиеллы входят в состав кишечного биоценоза, обнаруживаются на коже и слизистых оболочках. Они устойчивы к факторам окружающей среды и сравнительно долго сохраняются в почве, воде, в помещениях. В молочных продуктах выживают и размножаются при хранении их в холодильниках. При нагревании погибают уже при температуре 65°С, чувствительны к растворам обычных дезинфектантов.
Лабораторная диагностика. Диагноз основывается на результатах микроскопии мазков из исследуемого материала (мокрота, слизь из носа и др.) и выделении чистой культуры возбудителя. Дифференцировка клебсиелл и их идентификация проводится по морфологическим, биохимическим и антигенным признакам. Серодиагностику проводят в РСК с сыворотками больных и О-антигеном клебсиелл.
Профилактика и лечение. Специфическая вакцинопрофилактика клебсиеллезов не разработана. Для лечения применяют антибиотики, из которых цефалоспорины третьего поколения являются наиболее эффективными.
№10 Иерсинии. Чума и иерсиниозы. Биологические свойства возбудителей. Роль отечественных ученых в изучении чумы. Патогенез, иммунитет, методы лабораторной диагностики и специфической профилактики чумы.
Таксономия: Y.pestis вызывает чуму; отдел Gracilicutes, семейство Enterobacteriaceae, род Yersinia. Возбудитель – Yersinia pestis.
Морфологические свойства: грамотрицательные палочки, овоидной формы, окрашиваются биполярно. Подвижны, имеют капсулу, спор не образуют.
Культуральные свойства.
Факультативные анаэробы. Температурный оптимум +25С. Хорошо культивируются на простых питательных средах. Ферментируют большинство углеводов без образования газа. Психофилы - способны менять свой метаболизм в зависимости от температуры и размножаться при низких температурах. Вирулентные штаммы образуют шероховатые (R) колонии, переходные (RS) и сероватые слизистые гладкие авирулентные(S) формы.
Два типа колоний - молодые и зрелые. Молодые с неровными краями. Зрелые колонии крупные, с бурым зернистым центром и неровными краями. На скошенном агаре черед двое суток при +28 С образуют серовато - белый налет, врастающий в среду, на бульоне - нежную поверхностную пленку и хлопковидный осадок.
Биохимические свойства: фенментативная активнсть высокая: ферментация до кислоты ксилозу, синтез плазмокоагулазы, фибринолизина, гемолизина, лецитиназу, сероводород. Рамнозу, мочевину не ферментирует.
Антигенная структура.
Группа белково - полисахаридных и липополисахаридных антигенов: термостабильный соматический О-антиген и термолабильный капсульный V,W антигены. С W-антигеном связывают вирулентность бактерий. Продуцирует факторы патогенности: фибринолизин, плазмокоагулазу, эндотоксин, экзотоксин, капсулу, V,W антигены.
Резистентность: чувствителен к антибиотикам (особенно стрептомицин), нестоек к окружающей среде при высокой температуре.
Патогенные свойства.
Обладает патогенным потенциалом, подавляет функции фагоцитарной системы, подавляет окислительный взрыв в фагоцитах и беспрепятственно в них размножается. Факторы патогенности контролируются плазмидами трех классов. В патогенезе выделяют три основных стадии - лимфогенного заноса, бактеремии, генерализованной септицемии. Имеют адгезины и инвазины, низкомолекулярные протеины (ингибируют бактерицидные факторы), энтеротоксин. Часть факторов контролируется плазмидами вирулентности.
Клинические особенности: Инкубационный период – несколько часов до 8 сут. Различают локальные – кожно-бубонная, бубонная; внешне-диссеминированные – первично-легочная, вторично-легочная и кишечная; генерализованная – первично-септическая, вторично-септическая формы чумы. Региональная лимфоаденопатия, энтероколиты, реактивные артриты, спондилит, лихорадка.
Эпидемиология: Чума - классический природноочаговый зооноз диких животных. Основные носители в природе - сурки, суслики, в городских условиях - крысы. В передаче возбудителя - блохи животных, способные заражать человека.
Иммунитет: клеточно-гуморальный, ограничен по длительности и напряженности.
Лечение: антибиотики –стрептомицин, препараты тетрациклинового ряда.
Профилактика: специфическая профилактика - живая ослабленная чумная вакцина EV. Имеется сухая таблетированная вакцина для перорального применения. Для оценки иммунитета к чуме (естественного постинфекционного и вакцинального) может применяться внутрикожная аллергическая проба с пестином.
Чумной бактериофаг – при идентификации Y.pestis.
Чумная сухая вакцина – высушенная живая культура Y.pestis вакцинного штамма EV, используется для профилактики чумы.
Диагносиика

Дополнительно! Иерсинии псевдотуберкулеза и энтероколита.
Кишечный иерсиниоз — острая инфекционная болезнь, характеризующаяся поражением ЖКТ, тенденцией к генерализации с различных органов и систем.
Возбудитель кишечного иерсиниоза Yersinia enterocolitica.
Таксономия. Y.enterocolitica относится к отделу Gracilicutes, семейству Enterobacteriaceae, роду Yersinia.
Морфологические и тинкториальные свойства. Возбудитель полиморфен: он может иметь форму либо палочки с закругленными концами, либо овоидную с биполярным окрашиванием. Спор не имеет, иногда образует капсулу. Перитрих есть. Некоторые штаммы имеют пили. Грамотрицателен.
Культуральные свойства. Y.enterocolitica — факультативный анаэроб. Наиб. благоприятная темп. 25С. Возбудитель неприхотлив и растет на простых питательных средах.
Биохимическая активность. Биохимическая активность возбудителя высокая. Внутри вида по спектру б/х активности: индолообразованию, утилизации эскулина, реакции Фогеса – Проскауэра подразделяются на 5 хемоваров.
Основные б/х признаки: расщепление мочевины, ферментация сахарозы, отсутствие ферментации рамнозы, продукция орнитиндекарбоксилазы.
Антигенная структура. О- и Н-антигены, у некоторых штаммов обнаружен К-антиген. По 0-антигену различают более 30 серогрупп, из которых от больных чаще всего выделяют представителей серогрупп 03, 09, 05.
Факторы патогенности. Образует термостабильный эндотоксин. Некоторые штаммы выделяют вещество, соответствующее экзотоксину и обладающее энтеро- и цитотоксическим действием. У иерсиний обнаружены также инвазивный белок и белки, препятствующие фагоцитозу. Адгезивная активность иерсиний связана с пилями и белками наружной мембраны.
Резистентность. Чувствителен к высокой температуре, солнечным лучам, дезинфицирующим веществам, но очень устойчив к действию низких температур: хорошо переносит температуру -20 °С.
Эпидемиология. Источники болезни для человека - крысы, мыши, животные и птицы,. Механизм заражения иерсиниозом фекально-оральный, основным путем передачи является алиментарный: болезнь может возникнуть при употреблении фруктов, овощей, молока, мяса. Но возможны также контактный (при контакте людей с больными животными) и водный пути передачи.
Патогенез. Возбудитель попадает в организм через рот, в нижних отделах тонкой кишки прикрепляется к эпителию слизистой оболочки, внедряется в клетки эпителия, вызывая воспаление. Под действием токсинов усиливается перистальтика кишечника и возникает диарея. Иногда в патологический процесс вовлекается аппендикс, развивается аппендицит. Незавершенный фагоцитоз способствует генерализации процесса. У людей со сниженным иммунитетом могут развиться сепсис с образованием вторичных гнойных очагов в мозге, печени и селезенке.
Клиника. Различают гастроэнтероколитическую, аппендикулярную и септическую формы. Инкубационный период составляет от 1 до 4 дней. Болезнь начинается остро с повышения температуры тела до 39С, общей интоксикации, рвоты, болей в животе, поноса. Течение продолжительное.
Микробиологическая диагностика. Используют бактериологический и серологический методы исследования. Цель бактериологического метода являются идентификация возбудителя, определение антибиотикограммы, внутривидовая идентификация (установление серовара, биохимического варианта, фаговара).Материалом для бактериологического метода исследования служат испражнения, ликвор, кровь, моча, иногда червеобразный отросток. Материал для исследования помешают в фосфатный буфер и подвергают холодовому обогащению. Серологическая диагностика проводится постановкой РНГА, с диагностическим титром 1:160. Важное диагностическое значение имеет наблюдение за нарастанием титра антител в динамике.
Лечение. Этиотропная антибиотикотерапия.
№11. Возбудители внутрибольничных (нозокомиальных) инфекций. Причины их возникновения и особенности развития. Возможные пути профилактики.
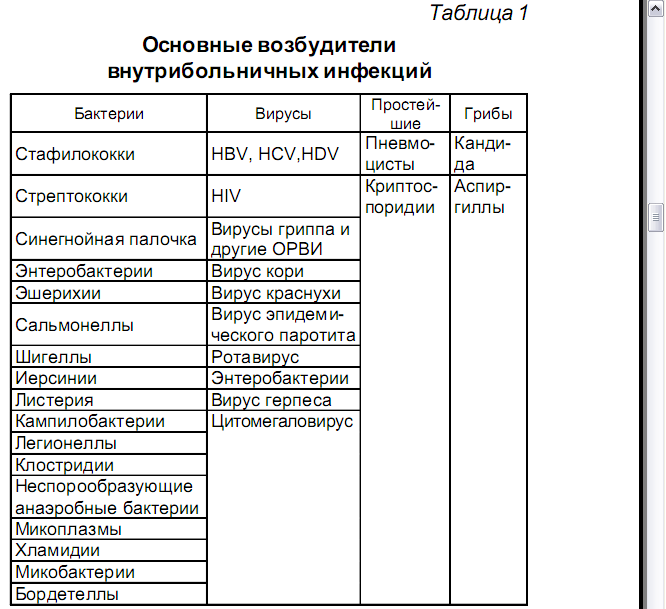
Пути и факторы передачи ВБИ
Естественные – связанные с реализацией эволюционно сложившегося механизма передачи инфекции (воздушно-капельного, воздушно-пылевого, фекально-орального, контактно-бытового и др.):
пищевой (через молоко, растворы для питья, пищевые продукты)
водный
контактный (через предметы ухода за больными, белье)
воздушный
Искусственные – связаны с лечебно-диагностическим процессом в ЛПУ и специфичен для госпитальных условий:
контактный (через руки медицинского персонала)
инструментальный
аппаратный
трансфузионный и др.
Общие подходы к профилактике ВБИ.
Мероприятия по профилактике ВБИ должны быть направлены на разрыв каждого из трех звеньев эпидемического процесса.
