
Патофизиология. Литвицкий. 2013
.pdfэффективность биологического окисления; ведёт к накоплению в клетке избытка Na+.
Действие различных повреждающих агентов на определённые виды клеток вызывает специфические для этих клеток изменения.
Например, влияние разнообразных (химических, физических,
биологических) патогенных факторов значительной силы на мышечные элементы сопровождается развитием контрактуры, на эритроциты — их гемолизом и выходом Hb.
НЕСПЕЦИФИЧЕСКИЕ ИЗМЕНЕНИЯ КЛЕТОК ПРИ ПОВРЕЖДЕНИИ
Неспецифическими (стереотипными, стандартными)
изменениями в клетках обозначают те, которые развиваются при
повреждении различных видов клеток самыми разными
патогенными воздействиями (например, гипоксия, ацидоз, чрезмерная активация свободнорадикальных и перекисных реакций, денатурация молекул белка, повышение проницаемости клеточных мембран,
дисбаланс ионов.
Выявление конкретного спектра выраженных в разной мере специфических и неспецифических изменений в клетках органов и тканей дает возможность судить о характере и силе действия патогенного фактора, о степени и масштабе повреждения, а также об эффективности (или неэффективности) применяемых для лечения медикаментозных и немедикаментозных средств. Например, по изменению активности в плазме крови относительно специфического для клеток миокарда MB-изофермента КФК и содержания миоглобина в сопоставлении с динамикой таких неспецифических показателей как
[K+] (калий выходит из повреждённых кардиомиоцитов) изменений на
191

ЭКГ, показателей сократительной функции различных регионов сердца
можно судить о степени и объёме повреждения сердца при его
инфаркте.
МЕХАНИЗМЫ АДАПТАЦИИ КЛЕТОК ПРИ ИХ ПОВРЕЖДЕНИИ
Действие на клетку патогенных факторов сопровождается активацией (или включением) различных реакций и процессов,
направленных на устранение либо уменьшение степени повреждения и его последствий, а также обеспечивающих устойчивость клеток к повреждению. Совокупность этих реакций обеспечивает приспособление (адаптацию) клетки к изменившимся условиям её жизнедеятельности.
Комплекс адаптивных реакций клеток условно подразделяют на внутриклеточные и межклеточные (рис. 5–21).
Механизмы адаптации клетки при её повреждении
|
Внутриклеточные |
|
|
Межклеточные |
|
|
* Реализуются |
|
* Реализуются |
||
повреждёнными клетками |
неповреждёнными клетками |
||||
Рис. 5–21. Механизмы адаптации клетки при её повреждении.
ВНУТРИКЛЕТОЧНЫЕ АДАПТИВНЫЕ МЕХАНИЗМЫ
К внутриклеточным адаптивным механизмам относят следующие реакции и процессы.
Компенсация нарушений энергетического обеспечения клетки;
192
Защита и репарация мембран и ферментов клетки;
Уменьшение выраженности или устранение дисбаланса ионов и воды в клетке;
Устранение дефектов генетической программы клетки и механизмов её реализации;
Компенсация расстройств механизмов регуляции внутриклеточных процессов;
Снижение функциональной активности клеток;
Регенерация;
Гипертрофия;
Гиперплазия.
КОМПЕНСАЦИЯ НАРУШЕНИЙ ЭНЕРГООБЕСПЕЧЕНИЯ
Механизмы |
компенсации |
нарушений |
энергетического |
обеспечения клетки приведены на рис. 5–22.
|
|
|
|
|
Нарушение энергообеспечения клетки |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Активация ресинтеза |
|
|
Активация ресинтеза АТФ |
|
Активация механизмов транспорта |
|
|
Активация механизмов |
||||||
|
|
в ходе тканевого |
|
энергии АТФ к эффекторным |
|
|
использования энергии |
|||||||
АТФ в ходе гликолиза |
|
|
|
|
|
|||||||||
|
|
дыхания в митохондриях |
|
структурам клетки |
|
|
АТФ |
|||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Снижение интенсивности функции клеток
Снижение интенсивности пластических процессов

 Уменьшение степени/устранение нарушений энергообеспечения клетки
Уменьшение степени/устранение нарушений энергообеспечения клетки
Рис. 5–22. Механизмы компенсации нарушений
энергетического обеспечения клетки при её повреждении.
При повреждении клетки, как правило, в большей или меньшей мере повреждаются митохондрии и снижается ресинтез АТФ в процессе
193

тканевого дыхания. Эти изменения служат сигналом для включения компенсационных механизмов: – увеличения продукции АТФ в системе гликолиза; – повышения активности ферментов, принимающих участие в процессах окисления и фосфорилирования (при слабой или умеренной степени повреждения клеток); – активации ферментов транспорта энергии АТФ (адениннуклеотидтрансферазы, КФК); – повышения эффективности ферментов утилизации энергии АТФ (АТФаз); –
ограничения функциональной активности клетки; – снижения интенсивности пластических процессов в клетке.
ЗАЩИТА МЕМБРАН И ФЕРМЕНТОВ
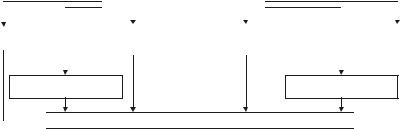
Защиту мембран и ферментов клеток осуществляют указанные на рис. 5–23 механизмы.
 Повреждение мембран и ферментов клетки
Повреждение мембран и ферментов клетки 
Активация факторов |
|
Активация буферных |
|
Активация систем |
|
Активация процессов |
||
АОЗ |
|
систем |
|
детоксикации микросом |
|
репарации субклеточных |
||
|
|
|
|
|
|
|
|
структур |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

 Снижение степени альтерации мембран и ферментов клетки
Снижение степени альтерации мембран и ферментов клетки 
Рис. 5–23. Механизмы защиты мембран и ферментов клетки
при её повреждении.
АОЗ — факторы антиоксидантной защиты.
Ферменты антиоксидантной защиты (СОД, инактивирующая радикалы O2–; каталаза и глутатионпероксидазы, расщепляющие соответственно Н2О2 и липиды) уменьшают патогенные эффекты
194

свободнорадикальных и перекисных реакций; активация буферных систем клетки ведёт к уменьшению внутриклеточного ацидоза
(следствие ацидоза — избыточная гидролитическая активность лизосомальных ферментов); повышение активности ферментов микросом (особенно ферментов эндоплазматической сети) усиливает физико-химическую трансформацию патогенных агентов путём их окисления, восстановления, деметилирования и т.д.; дерепрессия генов имеет следствием активацию синтеза компонентов мембран (белков,
липидов, углеводов) взамен повреждённых или утраченных.
УСТРАНЕНИЕ/УМЕНЬШЕНИЕ СТЕПЕНИ ДИСБАЛАНСА ИОНОВ И ЖИДКОСТИ
Механизмы уменьшения выраженности или устранения
дисбаланса ионов и воды в клетке приведены на рис. 5–24.
|
|
|
|
|
|
Дисбаланс ионов и воды |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Активация буферных систем |
|
Снижение степени нарушения |
|
Снижение степени повреждения |
|
Активация механизмов |
||||||||||
|
|
|
|
|
энергообеспечения клетки |
|
мембран и ферментов клетки |
|
|
трансмембранного |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
переноса ионов и |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
жидкости |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уменьшение степени (устранение) дисбаланса ионов и воды в клетке |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||||
Рис. 5–24. Механизмы уменьшения степени (устранения)
дисбаланса ионов и воды в клетке при её повреждении.
Существенное снижение степени расстройств обмена жидкости и ионов обеспечивают: – активация процессов энергетического
обеспечения ионных насосов; – повышение активности ферментов,
принимающих участие в транспорте ионов; – изменение интенсивности и характера метаболизма (например, усиление гликолиза
195
сопровождается высвобождением K+, содержание которого в повреждённых клетках уменьшено в связи с повышением проницаемости их мембран); – нормализация внутриклеточных буферных систем (например, активация карбонатного, фосфатного,
белкового буферов способствует восстановлению оптимального соотношения в цитозоле и трансмембранного распределения ионов K+, Na+, Ca2+ и других, в частности, путём уменьшения в клетке [Н+]).
Доказано, что уменьшение степени дисбаланса ионов, в свою очередь,
может сопровождаться нормализацией содержания и циркуляции внутриклеточной жидкости, объёма клеток и их органелл.
УСТРАНЕНИЕ ГЕНЕТИЧЕСКИХ ДЕФЕКТОВ
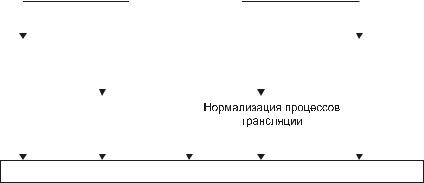
Механизмы устранения дефектов генетической программы клетки и экспрессии генов представлены на рис. 5–25.
|
|
|
|
|
|
Повреждение ДНК |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Устранение “разрывов” |
|
|
Замена повреждённого |
|
|
Обнаружение и устранение |
|||||||||
молекул ДНК |
|
|
участка ДНК нормальным |
|
|
чужеродного или повреждённого |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
фрагмента ДНК |
||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нормализация процессов |
|
|
|
|
|
|
|
|
|
||||
|
|
транскрипции ДНК |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Устранение дефектов генома и механизмов реализации его информации
Рис. 5–25. Устранение дефектов генетической программы
клетки и механизмы её реализации.
Устранение |
мелкомасштабных |
изменений |
в |
геноме |
осуществляют деметилазы. Они удаляют метильные группы и лигазы,
196

устраняют разрывы в цепях ДНК, возникающие под действием ионизирующего излучения, свободных радикалов и др. Особое значение имеет репарация ДНК, как эксцизионная, так и рекомбинационная.
Устранение нарушений механизмов реализации генетической программы клетки может нормализовать нуклео- и цитотомию,
транскрипцию, трансляции и др.
НОРМАЛИЗАЦИЯ |
МЕХАНИЗМОВ |
РЕГУЛЯЦИИ |
ВНУТРИКЛЕТОЧНЫХ ПРОЦЕССОВ
Реакции, компенсирующие нарушения механизмов восприятия
клеткой регулирующих влияний, указаны на рис. 5–26.
|
|
|
|
Нарушение регуляции клетки |
|
|
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изменение числа |
|
Изменение чувствительности |
|
|
Изменение активности |
|||||
рецепторов клетки |
|
рецепторов клетки к БАВ |
|
|
||||||
|
|
внутриклеточных посредников |
||||||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
регуляторных воздействий |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уменьшение степени (устранение) расстройств регуляции клетки
Рис. 5–26. Механизмы компенсации расстройств регуляции
клетки при её повреждении.
Кроме того, в повреждённой клетке расстраиваются механизмы обратной связи в метаболических путях (например, концентрация конечных продуктов по принципу положительной или отрицательной обратной связи изменяет активность ферментов в начале цепочки).
ОПТИМИЗАЦИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ КЛЕТОК
197
Важным механизмом защиты клетки является снижение выраженности или полное прекращение выполнения клеткой её специфических функций. Это позволяет перераспределить ресурсы и тем самым увеличить возможности адаптации клетки для компенсации изменений, вызванных повреждающим фактором. При этом энергия, уходившая на выполнение специфической клеточной функции, позволяет клетке легче скомпенсировать изменения метаболизма, вызванные повреждающим фактором. В результате степень и масштаб повреждения клеток при действии патогенного фактора существенно снижаются, а после прекращения его действия отмечается более интенсивное и полное восстановление клеточных структур и их функции. К главным механизмам, обеспечивающим временное понижение функции клеток, можно отнести: – уменьшение эффекторной импульсации от нервных центров; – снижение числа или чувствительности рецепторов на поверхности клетки; –
внутриклеточное регуляторное подавление метаболических реакций;
– репрессию активности отдельных генов.
ТИПОВЫЕ |
ПРИСПОСОБИТЕЛЬНЫЕ ИЗМЕНЕНИЯ ПРИ |
ПОВРЕЖДЕНИИ КЛЕТОК
Адаптация клеток в условиях повреждения происходит не только на метаболическом и функциональном уровнях. Длительное, повторное или значительное повреждение ведёт к существенным структурным перестройкам в клетке, имеющим адаптивное значение. Такая адаптация к действию повреждающих факторов происходит путём типовых приспособительных изменений клетки или клеточной системы
(атрофия, гипертрофия, гиперплазия, метаплазия, дисплазия).
198
Например, в условиях хронического венозного застоя в печени кислородное голодание гепатоцитов сопровождается их атрофией.
Процессы атрофии, гипертрофии, гиперплазии, а также регенерации рассмотрены в «Приложения» (см. «Справочник терминов» на компакт-
дтске).
БЕЛКИ ТЕПЛОВОГО ШОКА
При воздействии на клетку повреждающих факторов (изменения температуры, гипоксия, химические факторы, инфицирование вирусом и др.) происходит интенсификация синтеза белков теплового шока
(HSP, от Heat Shock Proteins; по-другому, белки стресса). Это может защитить клетку от повреждений и предотвратить её гибель. Наиболее распространены HSP с Mr 70 000 (hsp70) и 90 000 (hsp90).
Механизм действия этих белков многообразен и состоит в регуляции сборки, свёртывания и развёртывания других белков. Таким образом белки стресса предотвращают накопление в клетке белковых агрегатов. Примером повышенной резистентности, обусловленной белками теплового шока, могут служить опухолевые клетки, которые экспрессируют повышенный уровень HSP70, что защищает их от повреждения и гибели.
МЕЖКЛЕТОЧНЫЕ АДАПТИВНЫЕ МЕХАНИЗМЫ
Для межклеточных (системных) механизмов адаптации к повреждению характерно взаимодействие клеток друг с другом. Такое взаимодействие осуществляется несколькими путями: – обменом метаболитами и местными БАВ (например, цитокинами или ионами; –
развитием иммунных реакций; –. изменениями лимфо- и
кровообращения или нейро-эндокринных влияний.
199
ПРИМЕРЫ АДАПТИВНЫХ РЕАКЦИЙ
При системной гипоксии уменьшение содержания кислорода в крови может привести к повреждению клеток, прежде всего мозга.
Это рефлекторно (через раздражение хеморецепторов) стимулирует активность дыхательного центра. В результате увеличивается объём альвеолярной вентиляции, что ликвидирует или уменьшает недостаток кислорода в крови и тканях.
Повреждение клеток в условиях гипогликемии может быть уменьшено в результате адаптивной реакции: увеличения выработки гормонов, способствующих повышению в плазме крови глюкозы
(ГПК) и транспорта её в клетки: глюкагона, адреналина,
глюкокортикоидов, соматотропного гормона (СТГ) и др.
Патогенные факторы антигенный природы активируют иммунные механизмы защиты: система иммунобиологического надзора с помощью фагоцитов, антител и/или T-лимфоцитов инактивирует эндо- и экзогенные антигены, способные повредить клетки организма.
Указанные выше и другие системы в норме обеспечивают адекватное реагирование организма в целом на различные воздействия эндо- и экзогенного происхождения. В условиях патологии они участвуют в реализации механизмов защиты, компенсации и восстановления повреждённых структур и нарушенных функций клеток,
органов и тканей.
ПОВЫШЕНИЕ УСТОЙЧИВОСТИ КЛЕТОК К ПОВРЕЖДЕНИЮ
Мероприятия и средства активного повышения устойчивости
интактных клеток к действию патогенных факторов и стимуляции
200
