
- •Общая характеристика фенолов
- •Физические свойства фенолов
- •Получение фенолов
- •Химические свойства фенолов Кислотные свойства фенолов
- •Таутомерия фенолов
- •2.3 Этерификация фенолов
- •Реакции электрофильного замещения в ароматическом кольце
- •Нитрование фенолов
- •Сульфирование фенолов
- •Нитрозирование фенолов
- •Формилирование фенолов
- •Конденсация фенолов с альдегидами и кетонами
- •Реакция Кольбе
- •Азосочетание
- •Окисление фенолов
Реферат на тему:
«Фенолы»
Преподаватель: Петришек
Ирина Александровна
Выполнил:
студент 2 курса 9 группы
фармацевтического факультета
Владлен Ардисламов
Общая характеристика фенолов
Фенолами называются производные аренов, в которых один или несколько атомов водорода замещены на гидроксильные группы
ОН-группы фенолов называют фенольными гидроксильными группами.
Многие фенолы и их производные представлен в растительном мире (пигменты, дубильные вещества, лигниновые компоненты древесины). Фенолы используются в медицине (является мощным противогрибковым и противобактериальным антисептиком; при попадании в организм человека в достаточном количестве вызывает отравление с поражением большинства органов и систем), в фармацевтической промышленности, в производстве полимеров, красителей, душистых веществ, средств защиты растений. Фенолы и их производные используются в нефтяной промышленности (в качестве антиполяримезаторов). Гидрохинон применяется в качестве косметического средства для устранения дефектов кожи, в качестве ингибитора реакции свободнорадикальной полимеризации метилметакрилата входит в состав стоматологических композиционных материалов химического отверждения. Пирокатехин применяют в фотографии как проявитель, в производстве красителей, лекарственных веществ (например, адреналина).
По числу гидроксильных групп в ароматическом кольце различают одно и многоатомные фенолы. Для большинства фенолов и некоторых их гомологов используются тривиальные названия, принятые номенклатурой ИЮПАК.
Представители:
Фенол:

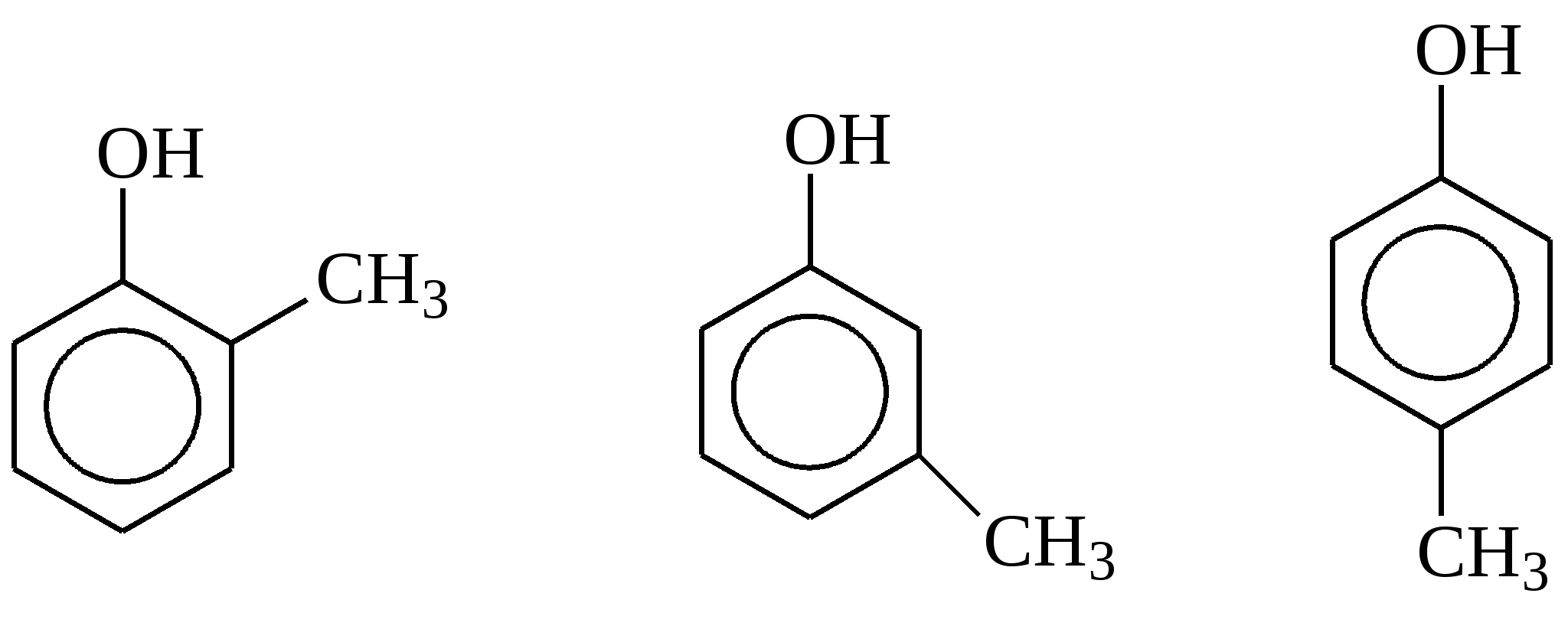
О-Крезол м-Крезол п-Крезол
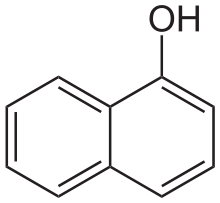
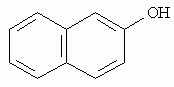
а-нафтол b-нафтол
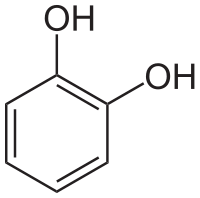
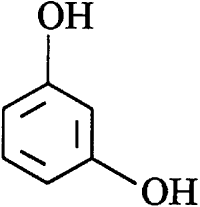
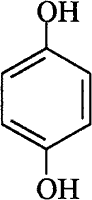
Пирокатехин Резорцин Гидрохинон

Пирогаллол
Физические свойства фенолов
Фенол и его низшие гомологи представляют собой бесцветные низкоплавкие кристаллические вещества или жидкости с довольно сильным характерным запахом. Запах фенола в воздухе при низких концентрациях (4мг/м3). Двух- и трехатомные фенолы- твердые вещества, без запаха, с достаточно высокими температурами плавления. Фенолы менее летучи чем спирты с близкой молекулярной массой, так как образуют более прочные межмолекулярные водородные связи.
Фенол умеренно растворим в воде (8.2% при 15С*). Другие одноатомные фенолы в воде малорастворимы, но легко растворяются в эфире, бензоле, спирте и хлороформе. Увеличение числа гидроксильных групп обуславливает повышение растворимости многоатомных фенолов в воде. В полярных многоатомных растворителяхмногоатомные фенолы так же ххорошо растворимы.
Фенолы и особенно нафтолы относятся к высокотоксичным веществам. Их выброс в водоемы причиняет непоправимый вред природе.
Получение фенолов
Кумольный метод (Сергеева)
Большую часть фенола в настоящее время производят из изопропилбензола – кумола. Окислением кумола воздухом получают гидроперекись кумола, разлагающуюся под действием водных растворов минеральных кислот на фенол и ацетон. Кумол синтезируют из бензола и пропилена.

Кумол
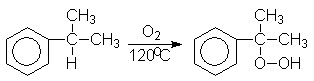
Гидроперекись кумола
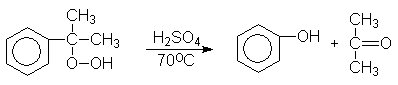
Механизм:
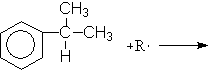
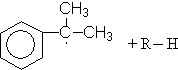
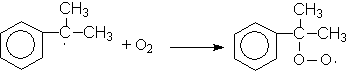 (М
3)
(М
3)
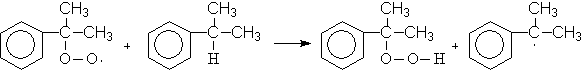
и т.д.
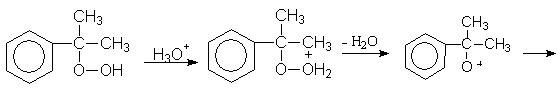 (М
4)
(М
4)
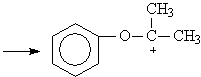
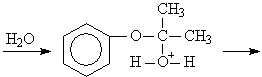
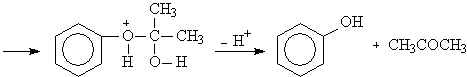
Аналогично ведет себя гидроперекись втор-бутила.
Гидролиз арилгалогенидов
Хлор в хлорбензоле малоподвижен и поэтому гидролиз ведут 8%-ным раствором NaOH в автоклаве при 250оС в присутствии солей меди:
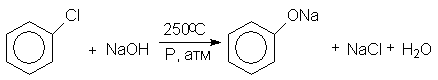
Феноксид натрия

По методу Рашига хлорбензол получают окислением бензола в присутствии хлороводорода:
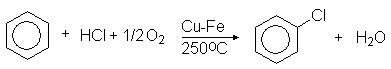
Гидролиз хлорбензола осуществляют перегретым паром в присутствии медного катализатора. Образующийся при этом хлороводород возвращают на первую стадию процесса:
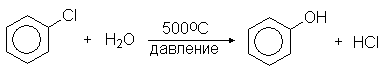
Гидролиз в присутствии щелочи проходит при более низкой температуре, но при этом теряется ценная соляная кислота, сохраняющаяся в методе Рашига.
Сплавление арилсульфонатов со щелочью
При сплавлении со щелочью арилсульфонаты претерпевают реакцию замещения:
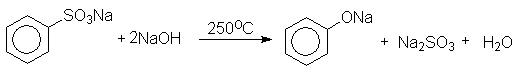
Бензолсульфокислота Бензолсульфонат натрия
Превращение фенолята натрия в фенол осуществляется с помощью диоксида серы, который образуется на второй стадии:
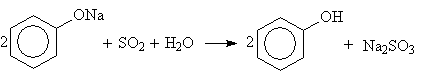
Фенол получают в виде водного раствора, из которого его выделяют дистилляцией. Этот метод синтеза фенола является самым старым (1890 г.). Метод используется для получения и других фенолов, например:
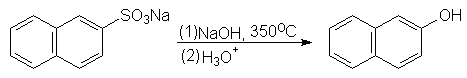
Разложение солей диазония
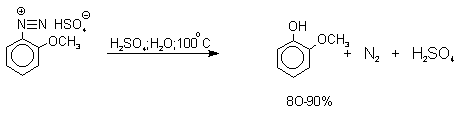
Прямое окисление бензола
С6Н6+О2 (боксит, 300-750С*) С6Н5ОН
Сложность данного превращения заключалась в том, что бензол окисляется легче, чем фенол. Известно как каталиитическое окисление кислородом воздуха (на схеме реакции), так и с применением различных комбинаций окислителей (пероксиды) и катализаторов (соли меди, железа, титана и т.д.).
Выделение из природного сырья
Фенолы выделяют из каменноугольной смолы при перегонке и химической обработке, получая смесь фенолов; из отходов переработки нефти.
