|
37.Растворимость
газов в жидкостях. Закон Генри-Дальтона.
Закон распределения.
З.Генри-Дальтона:При
некотором определенном давлении и
постоянной температуре растворяется
в жидкости определенное количество
газа, зависящее также и от свойств
жидкости. При увеличении или уменьшении
давления газовой атмосферы на жидкость
с сохранением той же температуры
увеличивается или уменьшается в таком
же отношении количество растворенного
газа.
Согласно
закону распределения, вещество,
растворенное в двух несмешивающихся
или ограниченно смешивающихся
жидкостях, распределяется между ними
в постоянном отношении. Это отношение
для идеальных систем зависит только
от температуры, природы вещества и не
зависит от концентрации. Из этого
закона следует, что при одновременном
растворении нескольких веществ каждое
из них распределяется между обеими
жидкими фазами таким образом, как
будто в системе нет никаких других
веществ, подлежащих распределению.
Закон распределения справедлив лишь
в том случае, если распределяемое
вещество в обеих фазах находится в
одной и той же форме. Константа
распределения вещества. Постоянная
величина, выражающая отношение
концентраций распределяемого вещества,
находящегося в обеих фазах (после
наступления равновесия) в одной и той
же форме, называется константой
распределения: 
где
Р о — константа распределения: [А] о
—концентрация вещества в фазе
органического растворителя, моль/л;
[А] В — концентрация вещества в водной
фазе, моль/
|
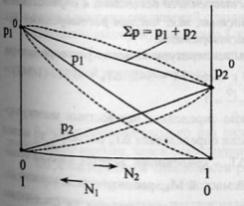 38.Законы
Рауля.Особенность
растворов: давление пара растворителя
над раствором ниже, чем над чистым
растворителем. Первый
закон.Давление
пара растворителя над раствором
пропорционально мольной доле
растворителя в растворе.или Относительно
понижение давление пара растворителя
над раствором равно мольной доли
растворенного вещества.Введем
обозначения: 38.Законы
Рауля.Особенность
растворов: давление пара растворителя
над раствором ниже, чем над чистым
растворителем. Первый
закон.Давление
пара растворителя над раствором
пропорционально мольной доле
растворителя в растворе.или Относительно
понижение давление пара растворителя
над раствором равно мольной доли
растворенного вещества.Введем
обозначения: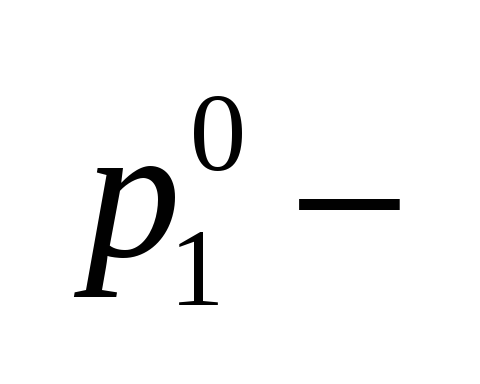 давление пара растворителя над чистым
растворителем;
давление пара растворителя над чистым
растворителем; давление пара растворителя над
раствором;
давление пара растворителя над
раствором; абсолютное понижение давления;
абсолютное понижение давления;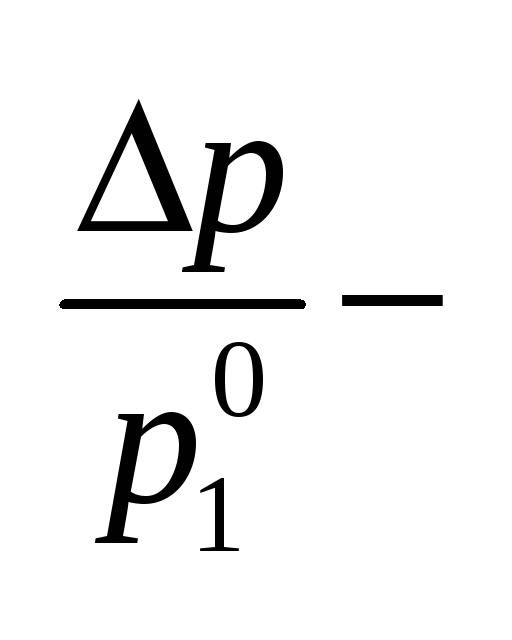 относительное понижение давления.
относительное понижение давления.
 Если
система полностью подчиняется закону,
на графике наблюдаются прямолинейные
зависимости. Однако в реальных системах
наблюдаются отклонения. Температура
замерзания раствора ниже температуры
замерзания чистого растворителя, а
температура кипения – выше.Второй
закон.Повышение
температуры кипения раствора и
понижение температуры его замерзания
пропорциональны моляльной концентрации
раствора. Если
система полностью подчиняется закону,
на графике наблюдаются прямолинейные
зависимости. Однако в реальных системах
наблюдаются отклонения. Температура
замерзания раствора ниже температуры
замерзания чистого растворителя, а
температура кипения – выше.Второй
закон.Повышение
температуры кипения раствора и
понижение температуры его замерзания
пропорциональны моляльной концентрации
раствора.
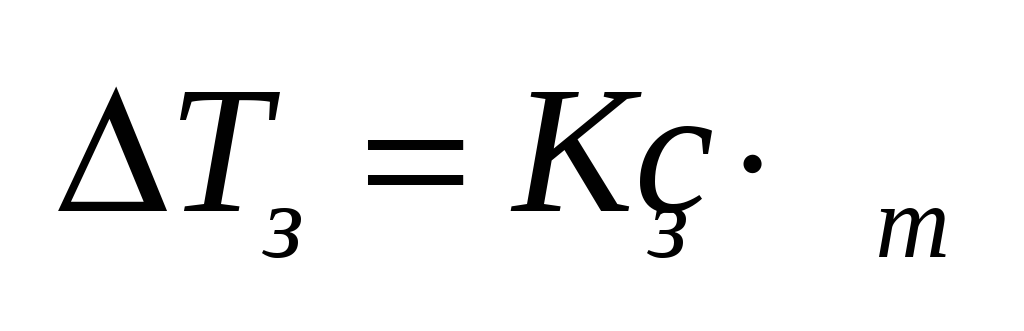 К – константа, характеризующая
растворитель.
К – константа, характеризующая
растворитель. не зависит от природы вещества, а
определяется природой растворителя
и моляльностью, т.е. числом растворенных
молекул в определенном количестве
растворителя.С помощью законов Рауля
можно определять неизвестные
молекулярные массы растворенных
веществ.
не зависит от природы вещества, а
определяется природой растворителя
и моляльностью, т.е. числом растворенных
молекул в определенном количестве
растворителя.С помощью законов Рауля
можно определять неизвестные
молекулярные массы растворенных
веществ.
|
39.Электролитическая
диссоциация. Степень диссоциации.
Слабые электролиты.Электролиты
– вещества, которые в растворе или
расплаве состоят полностью или частично
из ионов.Они не подчиняются законам
Рауля: их растворы замерзают при более
низких температурах, а кипят при более
высоких температурах, чем растворы
неэлектролитов той же моляльной
концентрации.Электролитическая
диссоциация.Теорию
ЭД предложил шведский ученый Аррениус.
«Электролиты, растворяясть в воде,
распадаются на ионы (заряженные
частицы). При этом каждый ион ведет
себя как самостоятельная частица.В
результате диссоциации концентрация
увеличивается (число частиц в единице
объема).»Академик Каблуков дополнил
теорию ЭД: «основная причина диссоциации
на ионы – взаимодействие с полярными
молекулами воды».Согласно закону
Кулона, сила притяжения между зарядами
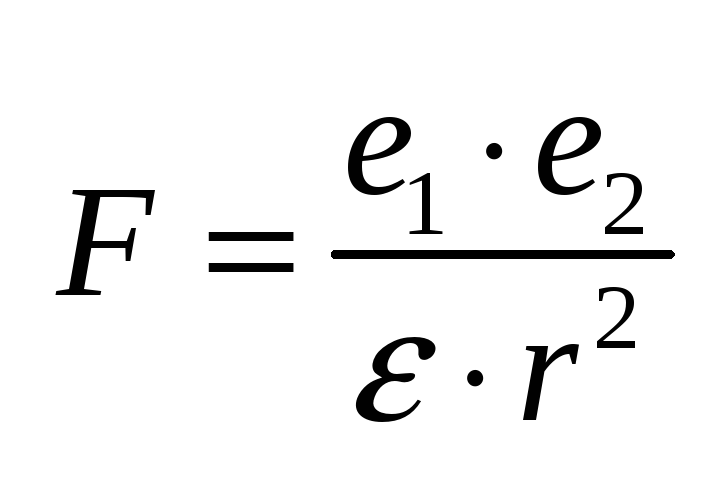
 показывает, во сколько раз сила в
данной среде меньше, чем в вакууме.Об
ионизирующей способности растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в
показывает, во сколько раз сила в
данной среде меньше, чем в вакууме.Об
ионизирующей способности растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в
 По способности диссоциации электролиты
делятся на слабые
и сильные.
Сильные диссоциируют полностью –
процесс необратим. Процесс диссоциации
слабых обратим (в растворах содержатся
как ионы, так и недиссоциированные
молекулы).Степень
диссоциации
- доля растворенного электролита,
распавшегося на ионы. Для сильных -
По способности диссоциации электролиты
делятся на слабые
и сильные.
Сильные диссоциируют полностью –
процесс необратим. Процесс диссоциации
слабых обратим (в растворах содержатся
как ионы, так и недиссоциированные
молекулы).Степень
диссоциации
- доля растворенного электролита,
распавшегося на ионы. Для сильных -
 для слабых
для слабых
 На практике СД определяют путем
измерения электропроводимости
раствора. Различают удельную
электропроводимость
На практике СД определяют путем
измерения электропроводимости
раствора. Различают удельную
электропроводимость
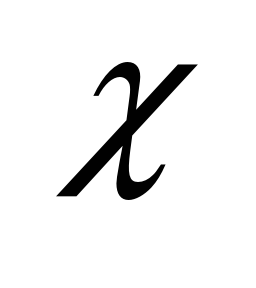 и эквивалентную
и эквивалентную
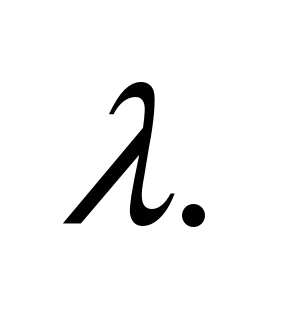  повышается с увеличением разбавления
до некоторой предельной величины,
когда все молекулы распадаются на
ионы
повышается с увеличением разбавления
до некоторой предельной величины,
когда все молекулы распадаются на
ионы
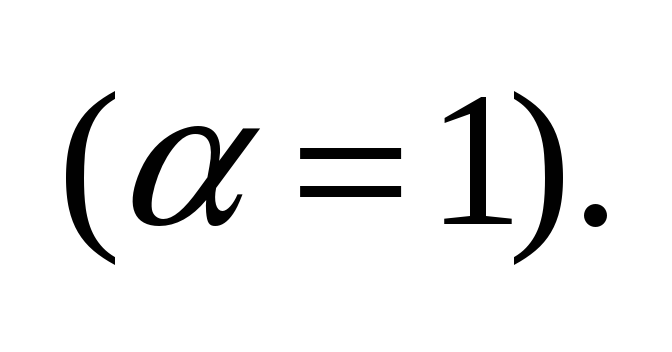 При этом предельное значение
эквивалентной электропроводимости
– электропроводимость
при бесконечном разбавлении
-
При этом предельное значение
эквивалентной электропроводимости
– электропроводимость
при бесконечном разбавлении
-
 Для слабых электролитов выполняется
Для слабых электролитов выполняется
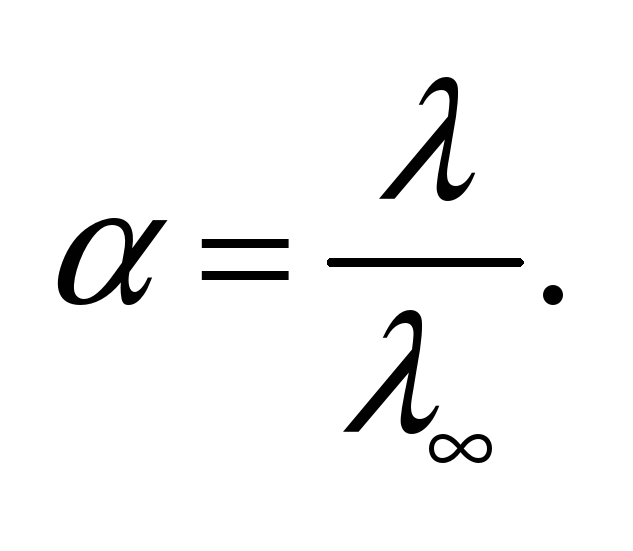
|
|
40.Константа
диссоциации. Закон разведения
Оствальда.Электролитическая
диссоциация.Теорию
ЭД предложил шведский ученый Аррениус.
«Электролиты, растворяясть в воде,
распадаются на ионы (заряженные
частицы). При этом каждый ион ведет
себя как самостоятельная частица.В
результате диссоциации концентрация
увеличивается (число частиц в единице
объема).»Академик Каблуков дополнил
теорию ЭД: «основная причина диссоциации
на ионы – взаимодействие с полярными
молекулами воды».Согласно закону
Кулона, сила притяжения между зарядами
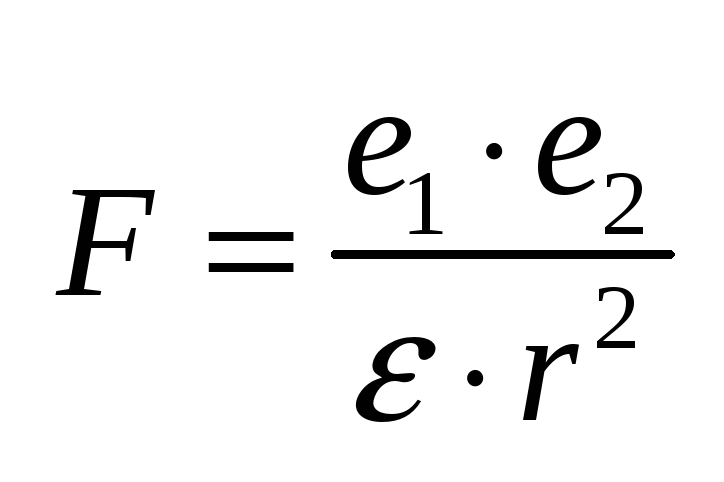
 показывает, во сколько раз сила в
данной среде меньше, чем в вакууме.Об
ионизирующей способности растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в
показывает, во сколько раз сила в
данной среде меньше, чем в вакууме.Об
ионизирующей способности растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в
 Константа
диссоциации в
случае разбавленного электролита:
Константа
диссоциации в
случае разбавленного электролита:
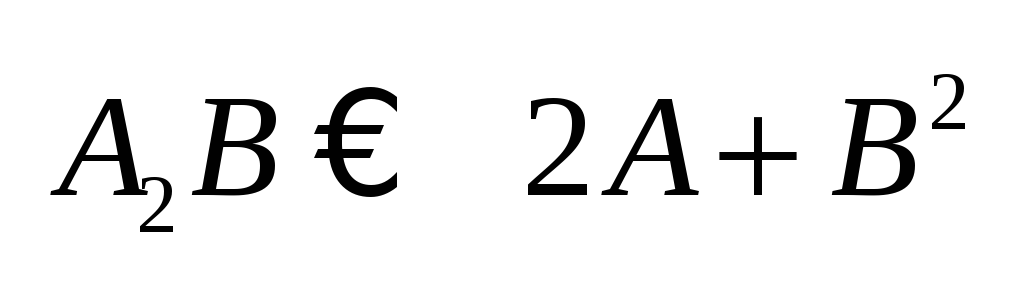
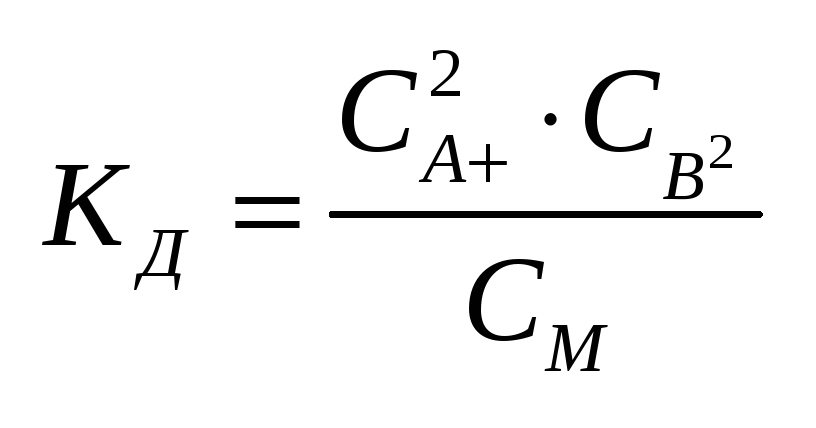 См – концентрация недиссоциированных
молекул.При стандартных условиях
См – концентрация недиссоциированных
молекул.При стандартных условиях
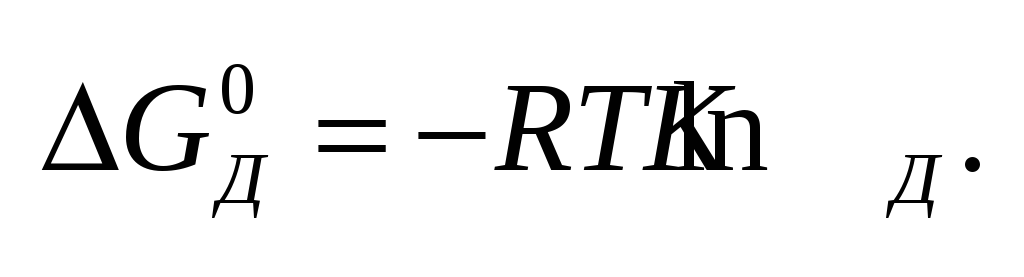 Константа
диссоциации
в одном и том же растворителе при
постоянной температуре – величина
постоянная, она свойственна данному
электролиту.Степень
диссоциации
характеризует состояние электролита
в растворе данной концентрации и
меняется с изменением ее.При повышении
концентрации раствора Константа
диссоциации
в одном и том же растворителе при
постоянной температуре – величина
постоянная, она свойственна данному
электролиту.Степень
диссоциации
характеризует состояние электролита
в растворе данной концентрации и
меняется с изменением ее.При повышении
концентрации раствора
 уменьшается. Закон
разведения Оствальда.С
разбавлением раствора степень
диссоциации его увеличивается.Выражает
зависимость между
уменьшается. Закон
разведения Оствальда.С
разбавлением раствора степень
диссоциации его увеличивается.Выражает
зависимость между
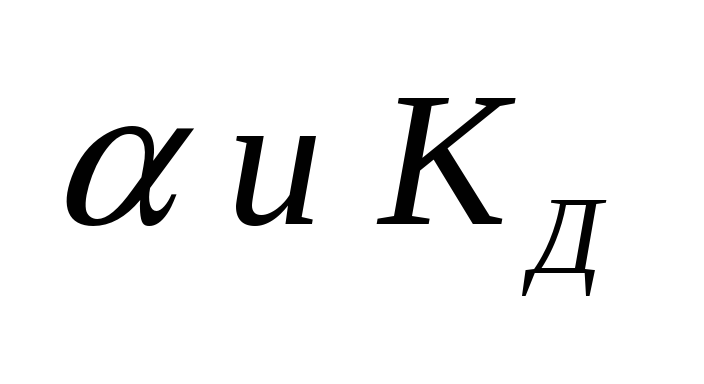
 Также
можно установить связь и между Также
можно установить связь и между

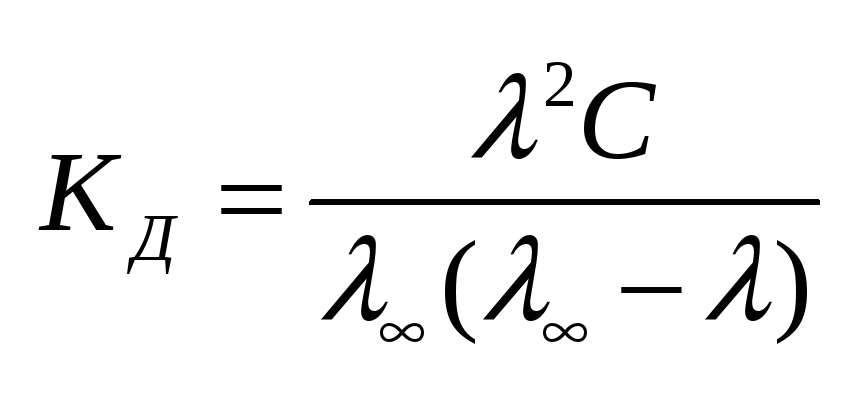 Сильные
электролиты: почти все соли, большинство
кислот и гидроксиды металлов.Электролиты
средней
силы: Сильные
электролиты: почти все соли, большинство
кислот и гидроксиды металлов.Электролиты
средней
силы:
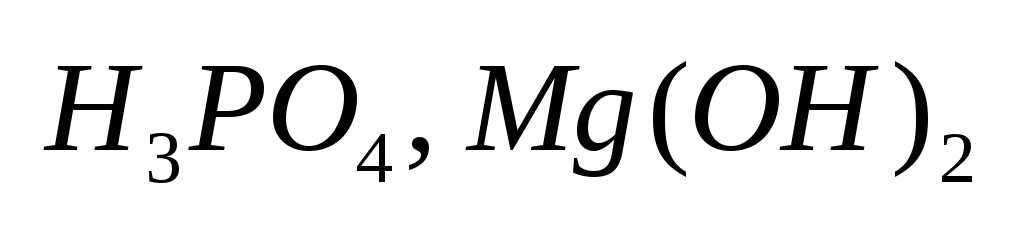 Слабые
электролиты: почти все органические
кислоты, вода. Слабые
электролиты: почти все органические
кислоты, вода.
|
41.Сильные
электролиты. Понятие активности и
коэффициента активности.Электролиты
– вещества, которые в растворе или
расплаве состоят полностью или частично
из ионов.Они не подчиняются законам
Рауля: их растворы замерзают при более
низких температурах, а кипят при более
высоких температурах, чем растворы
неэлектролитов той же моляльной
концентрации.По способности диссоциации
электролиты делятся на слабые
и сильные.
Сильные диссоциируют полностью –
процесс необратим. Процесс диссоциации
слабых обратим (в растворах содержатся
как ионы, так и недиссоциированные
молекулы).Сильные
электролиты не только в разбавленных,
но и в концентрированных растворах
диссоциируют практически нацело.Степень
диссоциации примерно равна 1.Если
условно взять какой-либо ион за центр
и провести вокруг сферу произвольного
радиуса, можно заметить, что каждый
ион окружается как бы роем других
ионов – ионной
атмосферой.
Ионная
атмосфера препятсвует передвижению
ионов в растворе, что приводит к
уменьшению электропроводимости
раствора.Разбавление увеличивает
расстояния между ионами, уменьшает
из взаимодействие, что приводит к
увеличению электропроводности за
счет роста скорости ионов, а не за счет
роста степени диссоциации.Для растворов
сильных электролитов введено понятие
активности
(или активной концентрации). Активность
– величина, подстановка которой вместо
концентрации в термодинамические
уравнения, действительные для идеальных
систем, позволяет использовать их для
реальных систем.
 с – концентрация, «гамма» - коэффициент
активности.Активность учитывает все
виды взаимодействия между ионами. В
качестве стандартного
– принимают состояние полной
диссоциации, при отсутствии осложняющего
воздействия ионов друг на друга.
с – концентрация, «гамма» - коэффициент
активности.Активность учитывает все
виды взаимодействия между ионами. В
качестве стандартного
– принимают состояние полной
диссоциации, при отсутствии осложняющего
воздействия ионов друг на друга.
|
42.Электролитическая
диссоциация воды. Ионное произведение
воды. Водородный показатель. Понятие
об индикаторах.Электролиты
– вещ-ва, которые в растворе или
расплаве состоят полностью или частично
из ионов.Они не подчиняются законам
Рауля: их растворы замерзают при более
низких темп-рах, а кипят при более
высоких темп-рах. Электролитическая
диссоциация.Теорию
ЭД предложил шведский ученый Аррениус.
«Электролиты, растворяясть в воде,
распадаются на ионы (заряженные
частицы). При этом каждый ион ведет
себя как самост.частица.В результате
диссоциации концентрация
увелич-ся).»Академик Каблуков дополнил
теорию ЭД: «основная причина диссоциации
на ионы – взаимодействие с полярными
молекулами воды».Согласно закону
Кулона, сила притяжения между зарядами
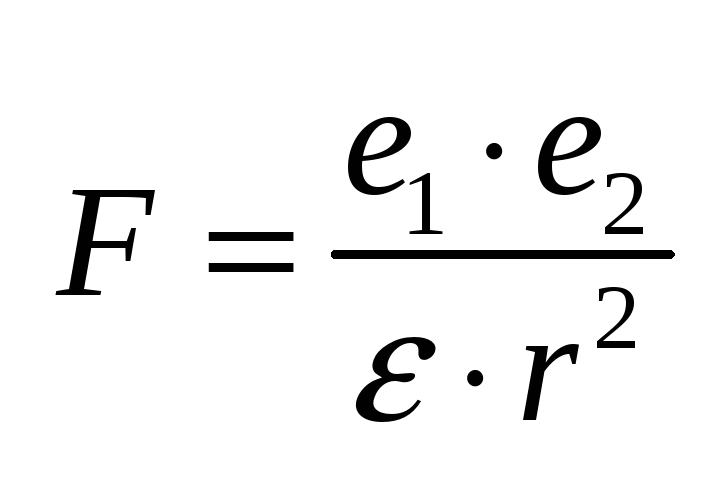 .Об
ионизирующей спос-сти растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в .Об
ионизирующей спос-сти растворителей
судят по их диэлектрической проницаемости:
чем она выше, тем энергичнее протекает
процесс ЭД.Кроме воды, электролиты
диссоциируют в
 По способности диссоциации электролиты
делятся на слабые
и сильные.
Сильные диссоциируют полностью –
процесс необратим. Процесс диссоциации
слабых обратим (в растворах содержатся
как ионы, так и недиссоциированные
молекулы).Степень
диссоциации
- доля растворенного электролита,
распавшегося на ионы. Для сильных -
По способности диссоциации электролиты
делятся на слабые
и сильные.
Сильные диссоциируют полностью –
процесс необратим. Процесс диссоциации
слабых обратим (в растворах содержатся
как ионы, так и недиссоциированные
молекулы).Степень
диссоциации
- доля растворенного электролита,
распавшегося на ионы. Для сильных -
 для слабых
для слабых
 На практике СД определяют путем
измерения электропроводимости
раствора. Различают удельную
электропроводимость
На практике СД определяют путем
измерения электропроводимости
раствора. Различают удельную
электропроводимость
 и эквивалентную
и эквивалентную
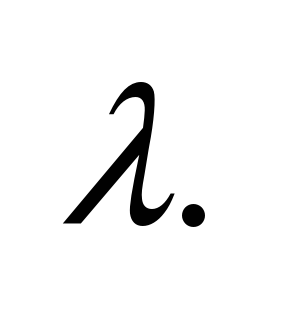
 повышается с увеличением разбавления
до некоторой предельной величины,
когда все молекулы распадаются на
ионы
повышается с увеличением разбавления
до некоторой предельной величины,
когда все молекулы распадаются на
ионы
 При этом предельное знач.экв-ной
электропроводимости – электропроводимость
при бесконечном разбавлении
-
При этом предельное знач.экв-ной
электропроводимости – электропроводимость
при бесконечном разбавлении
-
 Для слабых электролитов
Для слабых электролитов
|
|
43.Гидролиз
солей. Константа и степень
гидролиза.Гидролиз
- разложение солей под действием
воды.Вторая
формулировка.
Процесс, обратный нейтрализации,
приводящий к образованию кислоты и
основания.Нейтрализация
– реакция между кислотой и основанием.1.
Гидролиза нет
-если
сильное основание и сильная кислота.
-если
нерастворимые вещества («н» в таблице).
Пример.
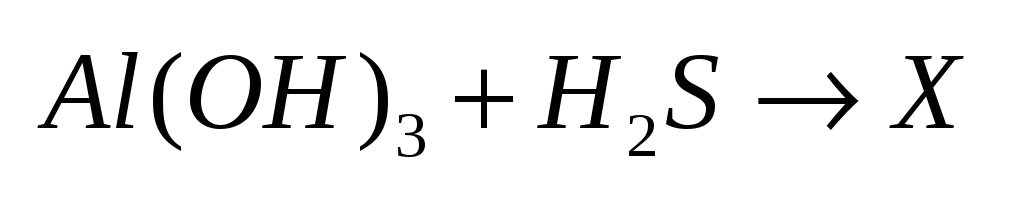
2.
Полный гидролиз
-если
слабая кислота и слабое основание.
-если
«-» в таблице растворимости.
Пример.
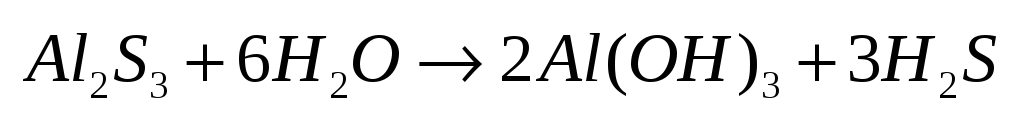
3.
-если сильное основание и слабая
кислота.
-если
слабое основание и сильная кислота.
Пример.
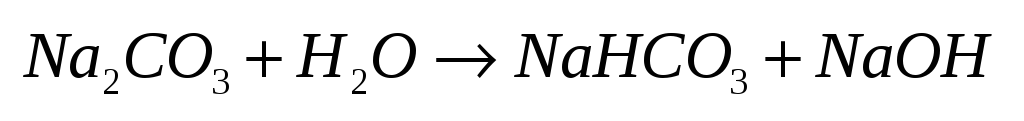
Константа
гидролиза:

Степень
гидролиза
– применяется для характеристики
реакций гидролиза.

Степень
возрастает с ростом температуры и с
уменьшением концентрации (разбавлением).
|
44.Окислительно-восстановительные
реакции. Ионно-электронный метод
подбора коэффициентов в
окислительно-восстановительных
реакциях.Любая
ОВР состоит из процессов окисления и
восстановления.Окисление
– отдача
электронов веществом, т.е повышение
степени окисления элемента.Пример.
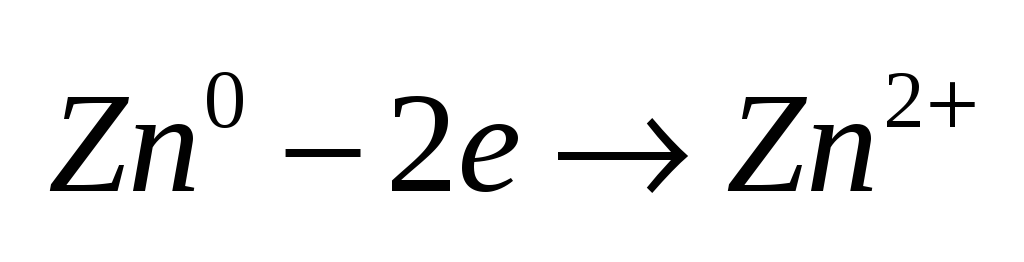 Вещества,
отдающие электроны, называют
восстановителями.Типичные
восстановители: водород, металлы,
углерод.Восстановление
– смещение
электронов к веществу или понижение
степени окисления.Пример. Вещества,
отдающие электроны, называют
восстановителями.Типичные
восстановители: водород, металлы,
углерод.Восстановление
– смещение
электронов к веществу или понижение
степени окисления.Пример.
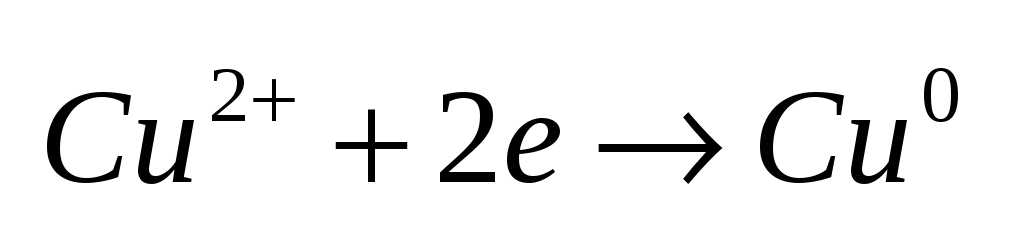 Вещества,
принимающие электроны, называют
окислителями.Типичные
окислители: галогены, водород, соединения
кислорода Вещества,
принимающие электроны, называют
окислителями.Типичные
окислители: галогены, водород, соединения
кислорода
 Существуют
реакции межмолекулярные
(окислители и восстановители – разные
вещества) и внутримолекулярные
(окислители и восстановители – атомы
одной молекулы). Существуют
реакции межмолекулярные
(окислители и восстановители – разные
вещества) и внутримолекулярные
(окислители и восстановители – атомы
одной молекулы).
Пример.
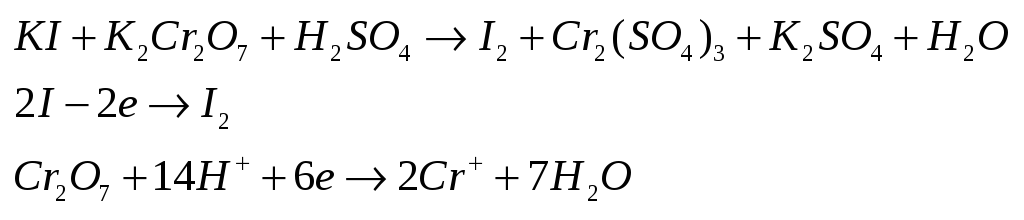 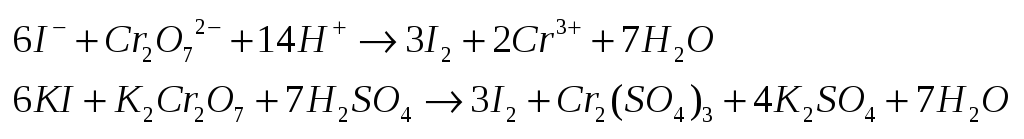
|
45.Возникновения
скачка потенциала на границе раздела
«металл-расствор». Равновесный
электродный потенциал.Электрохимия
– область
физической химии, охватывающая
химические процессы, сопровождающиеся
возникновением электрического тока,
либо вызванные действием электрического
тока.Электрод
– проводник 1 рода, погруженный в
раствор электролита в условиях
прохождения через него тока. В объеме
металла устанавливается подвижное
равновесие: Ме=Men++
n*ē.
При погружении электрода в воду катионы
металла гидратируются полярными
молекулами воды и переходят в раствор,
Men++
mH2O=Meрn+m*H2O.
Поверхность электрода заряжается
отрицательно за счет оставшихся
электронов, из-за этого перешедшие в
раствор катионы не могут отойти от
электрода. Катионы и электроны создают
двойной
электрический слой
(его толщина зависит от концентрации
раствора, температуры, заряда металла).
Пограничный слой жидкости заряжается
положительно, поверхность металла
отрицательно, возникает скачок
электрического потенциала – электродный
потенциал.Потенциал,
отвечающий состоянию равновесия,
когда скорость перехода ионов в раствор
равна скорости их осаждения –
равновесный
потенциал.Для
всех металлов, погружаемых в чистую
воду, качественно наблюдается одинаковая
картина: металл заряжается отрицательно,
прилегающий слой жидкости –
положительно.Данный скачок можно
охарактеризовать реакцией:
 Рассмотрим
погружение в раствор активного и
неактивного металла.1. Активный металл
посылает большое число ионов в раствор,
равновесная концентрация его ионов
трудно достижима => металл будет
заряжаться отрицательно.2.
Равновесная концентрация очень мала
=> электроду сообщается положительный
заряд, а оставшиеся анионы создают
отрицательный заряд у прилегающего
слоя. Рассмотрим
погружение в раствор активного и
неактивного металла.1. Активный металл
посылает большое число ионов в раствор,
равновесная концентрация его ионов
трудно достижима => металл будет
заряжаться отрицательно.2.
Равновесная концентрация очень мала
=> электроду сообщается положительный
заряд, а оставшиеся анионы создают
отрицательный заряд у прилегающего
слоя.
|
|
|
|
|
|
 46.Медно-цинковый
гальванический элемент Якоби-Даниэля.
Процессы на электродах. Понятие
ЭДС.Гальванический элемент
– любое устройство, дающее возможность
получать электрический ток за счет
проведения той или иной химической
реакции.Рассмотрим систему, в которой
медь и цинк в виде пластинок помещены
в растворы своих солей, разделенных
перегородкой – диафрагмой.
При разомкнутой цепи электроды
приобретают равновесные потенциалы,
которые отличаются по знаку и по
величине. При ее замыкании электроны
от цинкового электрода перемещаются
к медному. На электродах нарушается
равновесие: 46.Медно-цинковый
гальванический элемент Якоби-Даниэля.
Процессы на электродах. Понятие
ЭДС.Гальванический элемент
– любое устройство, дающее возможность
получать электрический ток за счет
проведения той или иной химической
реакции.Рассмотрим систему, в которой
медь и цинк в виде пластинок помещены
в растворы своих солей, разделенных
перегородкой – диафрагмой.
При разомкнутой цепи электроды
приобретают равновесные потенциалы,
которые отличаются по знаку и по
величине. При ее замыкании электроны
от цинкового электрода перемещаются
к медному. На электродах нарушается
равновесие:
 Получают
развитие две реакции: на катоде –
окисление Zn=Zn2++2ē,
на аноде – восстановление
Cu2++2ē=Сu0.Суммарная
реакция: Получают
развитие две реакции: на катоде –
окисление Zn=Zn2++2ē,
на аноде – восстановление
Cu2++2ē=Сu0.Суммарная
реакция:
 Гальванический
элемент на основе такой реакции был
предложен русским ученым Якоби.
Создателем является и ученый Даниэль.В
связи с восстановлением катионов у
медного электрода накапливается
избыток анионов SO22-,
а у цинкового электрода их недостаток.
Эти анионы начинают перемещаться
через полупроницаемую перегородку,
замыкая цепь.Причина
возникновения тока
– разность потенциалов на электродах.
ЭДС
элемента
– максимальная разность потенциалов,
отвечающая обратимым условиям работы
гальванического элемента. Она равна
алгебраической сумме отдельных скачков
потенциалов на границах раздела фаз,
образующих элемент. Очевидно, чем
больше ЭДС, тем быстрее протекает
реакция окисления-восстновления.Гальваническая
цепь
– последовательная совокупность
скачков потенциалов на поверхностях
раздела, отвечающих данному
гальваническому элементу. В данном
случае цепь записывается: Гальванический
элемент на основе такой реакции был
предложен русским ученым Якоби.
Создателем является и ученый Даниэль.В
связи с восстановлением катионов у
медного электрода накапливается
избыток анионов SO22-,
а у цинкового электрода их недостаток.
Эти анионы начинают перемещаться
через полупроницаемую перегородку,
замыкая цепь.Причина
возникновения тока
– разность потенциалов на электродах.
ЭДС
элемента
– максимальная разность потенциалов,
отвечающая обратимым условиям работы
гальванического элемента. Она равна
алгебраической сумме отдельных скачков
потенциалов на границах раздела фаз,
образующих элемент. Очевидно, чем
больше ЭДС, тем быстрее протекает
реакция окисления-восстновления.Гальваническая
цепь
– последовательная совокупность
скачков потенциалов на поверхностях
раздела, отвечающих данному
гальваническому элементу. В данном
случае цепь записывается:
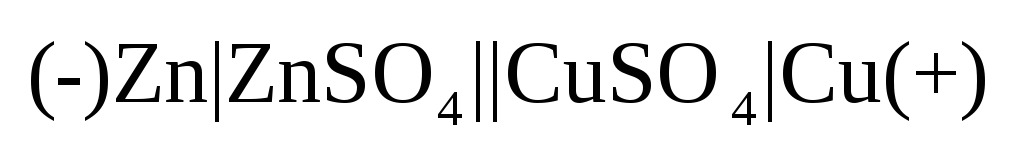
 1
и 3 – скачки на границах «электрод-электролит»,
2 – на границе электролита, 4 – на
границе двух металлов.Величиной 1
и 3 – скачки на границах «электрод-электролит»,
2 – на границе электролита, 4 – на
границе двух металлов.Величиной
 можно пренебречь.
можно пренебречь.
|
47.Зависимость
ЭДС гальванического элемента от
природы реагирующих веществ, температуры
и концентрации. Стандартная
ЭДС.Гальванический элемент
– любое устройство, дающее возможность
получать электрический ток за счет
проведения той или иной химической
реакции.Влияние
природы реагирующих веществ.Пусть
протекает реакция:
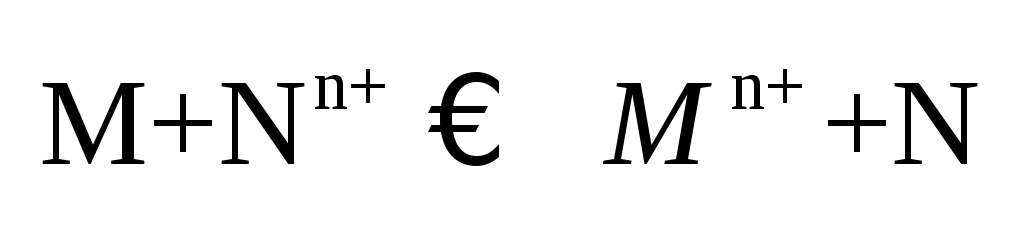 Максимальная полезная работа:
Максимальная полезная работа:

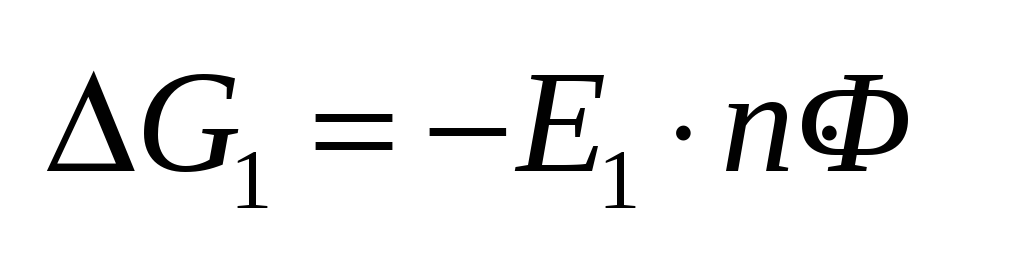
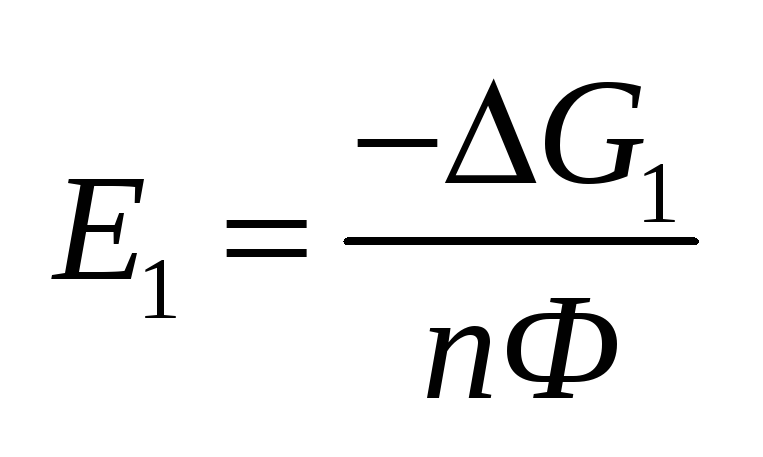 Реакция2: Реакция2:
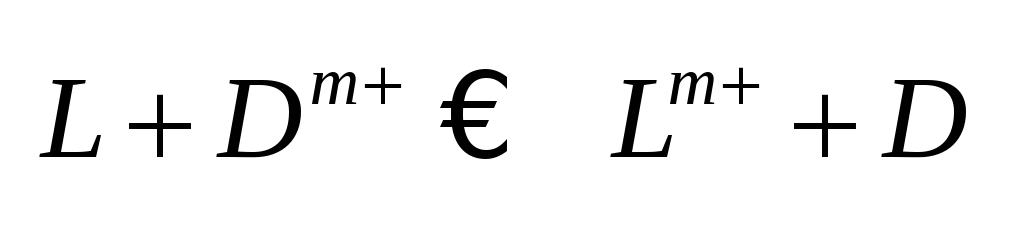
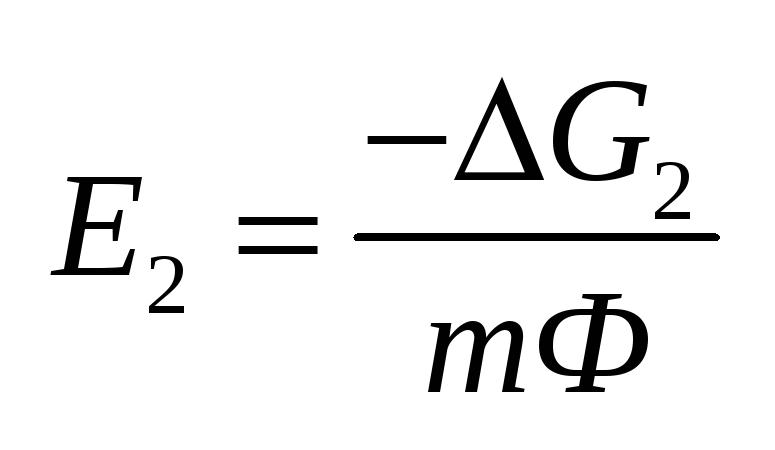 Вывод.
В зависимости от природы веществ, ЭДС
будет меняться.Влияние
температуры.Согласно
уравнению Гиббса-Гельмгольца, работа
реакции. При наличии исходных
термохимических данных можно рассчитать
ЭДС. 2)Зависимость от температуры: Вывод.
В зависимости от природы веществ, ЭДС
будет меняться.Влияние
температуры.Согласно
уравнению Гиббса-Гельмгольца, работа
реакции. При наличии исходных
термохимических данных можно рассчитать
ЭДС. 2)Зависимость от температуры:
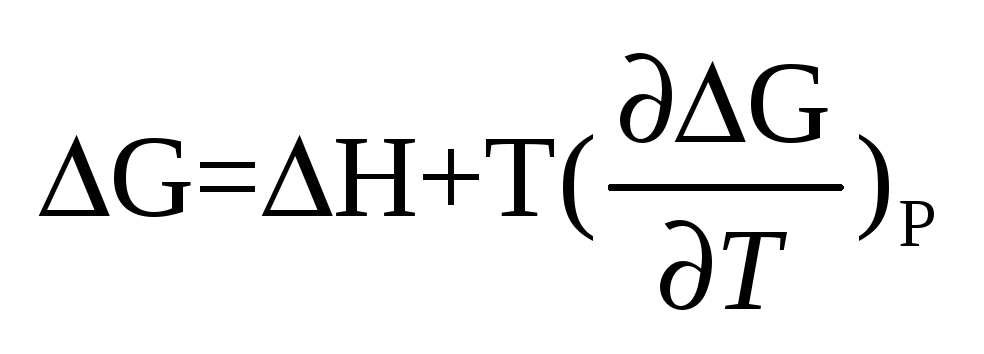 Сделаем
подстановки: Сделаем
подстановки:


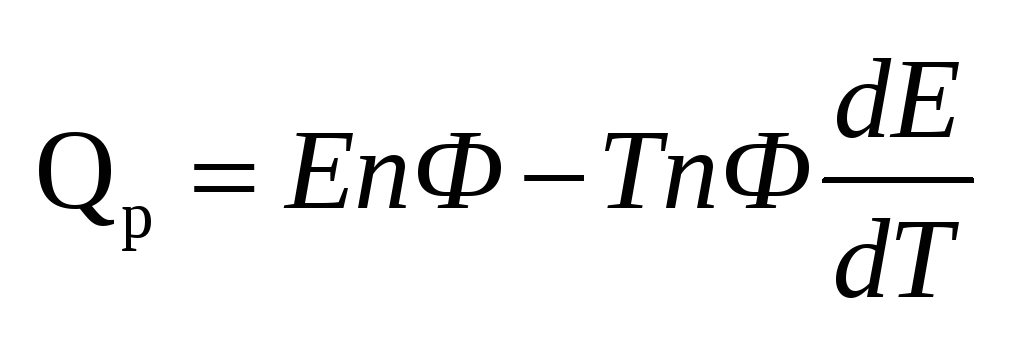
 Qp
– теплота реакции, которая выделяется
или поглощается при ее необратимом
проведении. Если реакция протекает
обратимо, то часть энергии реакции
превращается в работу А, а часть q
остается в виде теплоты в элементе,
q
характеризует связанную энергию.Определив
градиент ЭДС, можно вычислить изменение
энтропии для реакции.Если q<0, Qp
– теплота реакции, которая выделяется
или поглощается при ее необратимом
проведении. Если реакция протекает
обратимо, то часть энергии реакции
превращается в работу А, а часть q
остается в виде теплоты в элементе,
q
характеризует связанную энергию.Определив
градиент ЭДС, можно вычислить изменение
энтропии для реакции.Если q<0,
 т.е. ЭДС уменьшается с ростом
температуры.Если q>0,
т.е. ЭДС уменьшается с ростом
температуры.Если q>0,
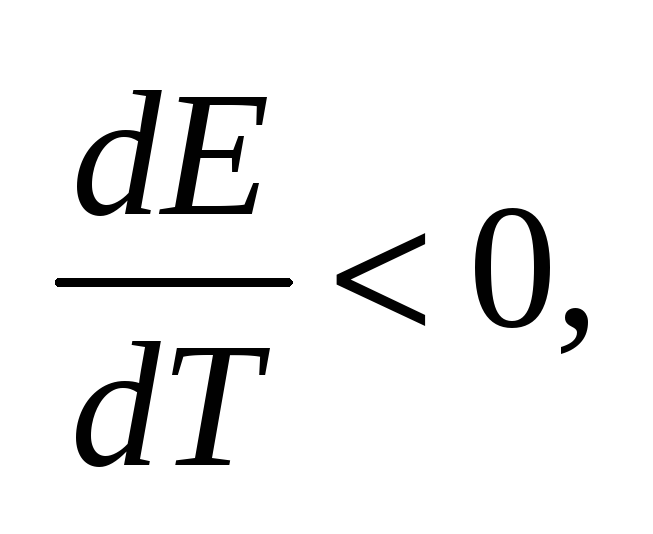 т.е. ЭДС растет с ростом температуры.Для
гальванических элементов q
подбирают малом, чтобы
т.е. ЭДС растет с ростом температуры.Для
гальванических элементов q
подбирают малом, чтобы
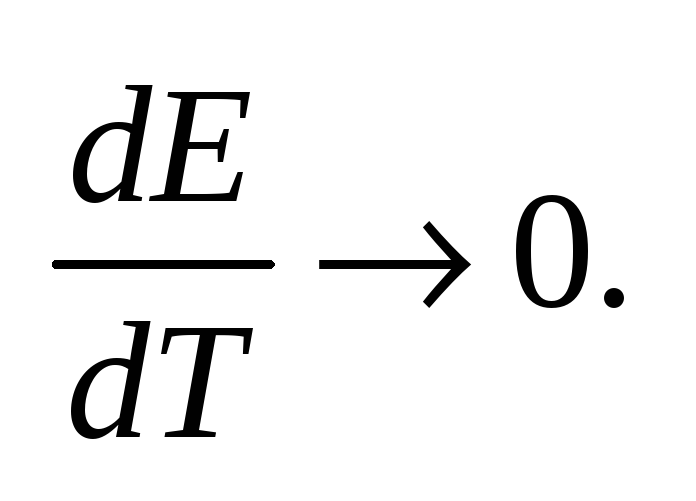 Влияние
концентрации.Пусть реакция Влияние
концентрации.Пусть реакция
 Изотерма
реакции: Изотерма
реакции:
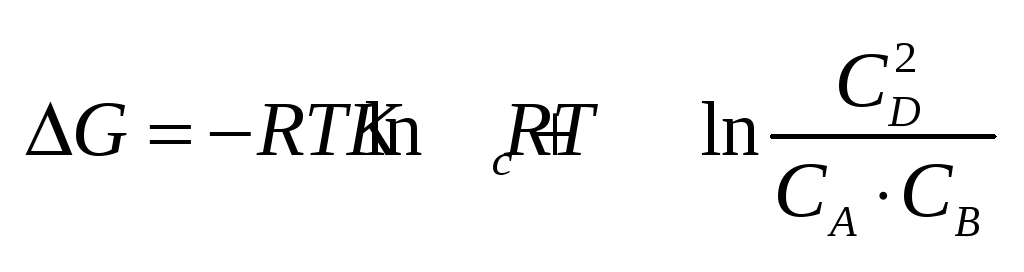 Преобразуем
и получим: Преобразуем
и получим:
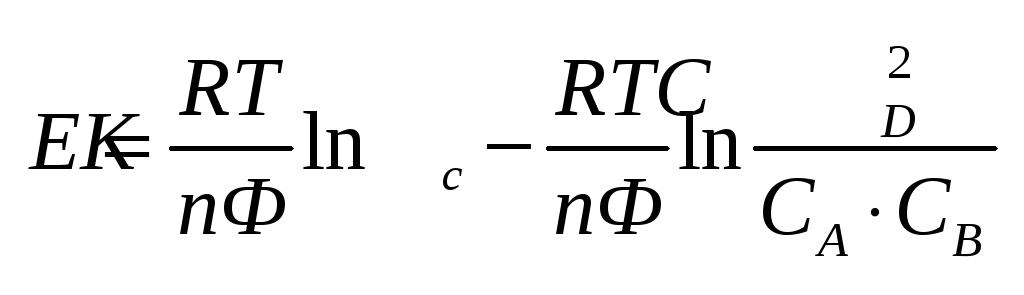 Обозначим
первое слагаемое за Обозначим
первое слагаемое за
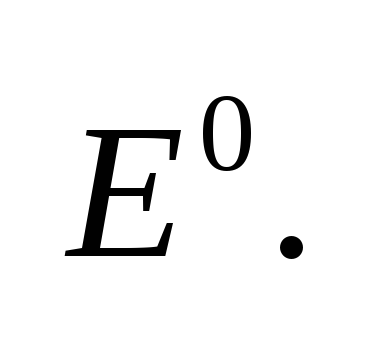 Это
стандартная
ЭДС,
она отвечает случаю равенства единице
концентраций всех участвующих веществ,
т.е. стандартному изменению свободной
энергии реакции Это
стандартная
ЭДС,
она отвечает случаю равенства единице
концентраций всех участвующих веществ,
т.е. стандартному изменению свободной
энергии реакции
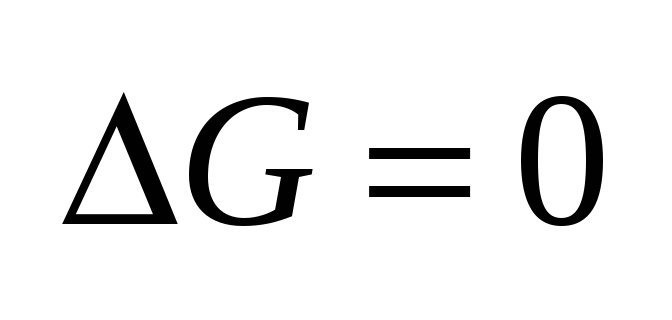
|
48.Стандартный
водородный электрод. Формула Нернста.
Стандартный потенциал. Ряд напряжений.В
настоящее время невозможно рассчитать
или экспериментально определить
абсолютное значение потенциала на
отдельно взятом электроде (абсолютный
электродный потенциал).Поэтому
значение потенциала на электроде
всегда определяется по отношению к
эталонному электроду, потенциал
которого условно принимается за нуль.В
электрохимии таким электродом является
нормальный
водородный элемент.Его
устройство: в стеклянный сосуд сложной
формы залит раствор серной кислоты
такой концентрации, что
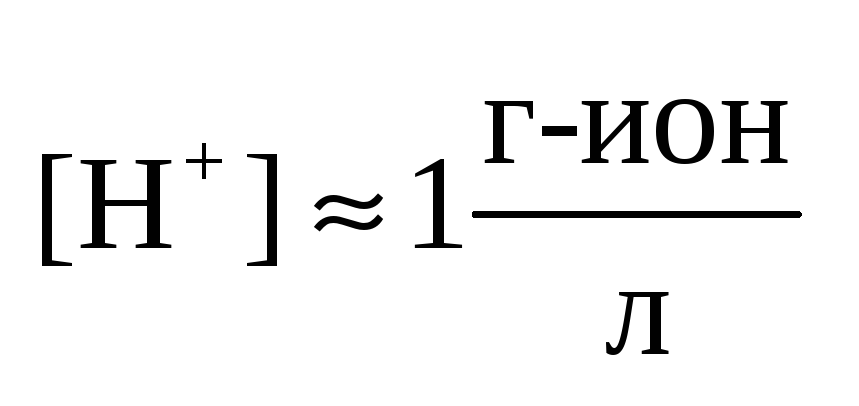 В него опущена платиновая пластинка,
покрытая платиновой
чернью. Снизу в сосуд подается
газообразный водород. Насыщенная им
пластина ведет себя как водородный
электрод. То есть имеет место равновесие:
(губчатая пластина) – платиновый
электрод, Р=1атм. Водород омывает
платину, растворяется в ней. Насыщенная
водородом платина начинает вести себя
как водородный электрод, т.е.
В него опущена платиновая пластинка,
покрытая платиновой
чернью. Снизу в сосуд подается
газообразный водород. Насыщенная им
пластина ведет себя как водородный
электрод. То есть имеет место равновесие:
(губчатая пластина) – платиновый
электрод, Р=1атм. Водород омывает
платину, растворяется в ней. Насыщенная
водородом платина начинает вести себя
как водородный электрод, т.е.
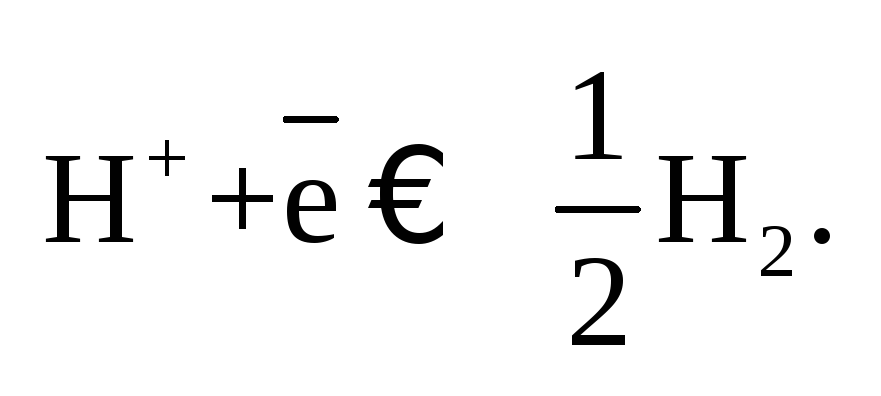 Скачок
потенциала на границе Скачок
потенциала на границе
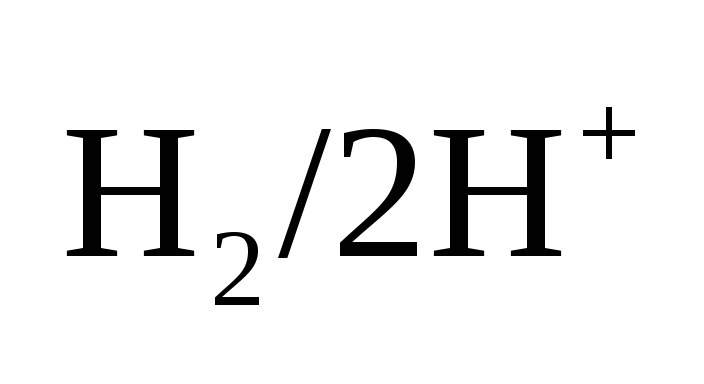 имеет определенную величину, которую
принимают за 0.За условную величину,
характеризующую потенциал электрода,
принимают ЭДС гальванического элемента,
составленного из этого электрода и
НВЭ.Стандартный потенциал металла –
ЭДС гальванического элемента, состоящего
из данного электрода, погруженного в
раствор, где активность ионов металла
равна 1, и из СВЭ. Уравнение Нернста
(T=298К):
имеет определенную величину, которую
принимают за 0.За условную величину,
характеризующую потенциал электрода,
принимают ЭДС гальванического элемента,
составленного из этого электрода и
НВЭ.Стандартный потенциал металла –
ЭДС гальванического элемента, состоящего
из данного электрода, погруженного в
раствор, где активность ионов металла
равна 1, и из СВЭ. Уравнение Нернста
(T=298К):
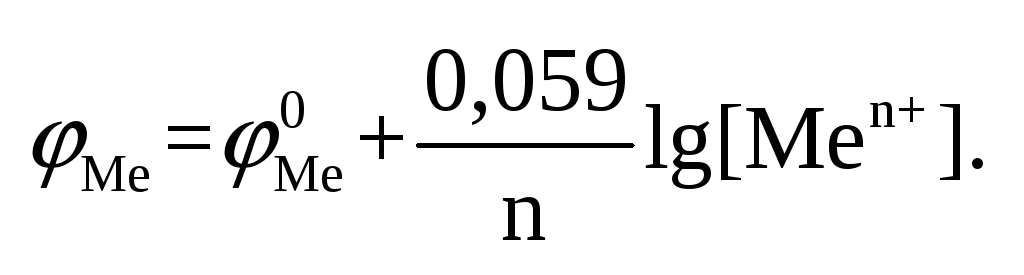 Если расположить все металлы в ряд
по алгебраической величине их
стандартных потенциалов, получим ряд
напряжений.Отрицательный
потенциал принадлежит электродам,
которые заряжаются отрицательно по
отношению к НВЭ.Положительный –
электрод заряжается положительно по
отношению к НВЭ.
Если расположить все металлы в ряд
по алгебраической величине их
стандартных потенциалов, получим ряд
напряжений.Отрицательный
потенциал принадлежит электродам,
которые заряжаются отрицательно по
отношению к НВЭ.Положительный –
электрод заряжается положительно по
отношению к НВЭ.
|
|
  49.Типы
электродов. Окислительно-восстановительный
электроды.Электрод
– проводник 1 рода, погруженный в
раствор электролита в условиях
прохождения через него тока. Три
типа:
электроды первого, второго и третьего
рода.Электроды
1-го рода.Металлы,
погруженные в растворы своих солей.солей: 49.Типы
электродов. Окислительно-восстановительный
электроды.Электрод
– проводник 1 рода, погруженный в
раствор электролита в условиях
прохождения через него тока. Три
типа:
электроды первого, второго и третьего
рода.Электроды
1-го рода.Металлы,
погруженные в растворы своих солей.солей:
 Электроды
2-го рода.Металл
погружен в насыщенный раствор своей
малорастворимой соли, к которой
добавлена другая соль с тем же анионом,но
хорошо растворимая.Пример. Электроды
2-го рода.Металл
погружен в насыщенный раствор своей
малорастворимой соли, к которой
добавлена другая соль с тем же анионом,но
хорошо растворимая.Пример.
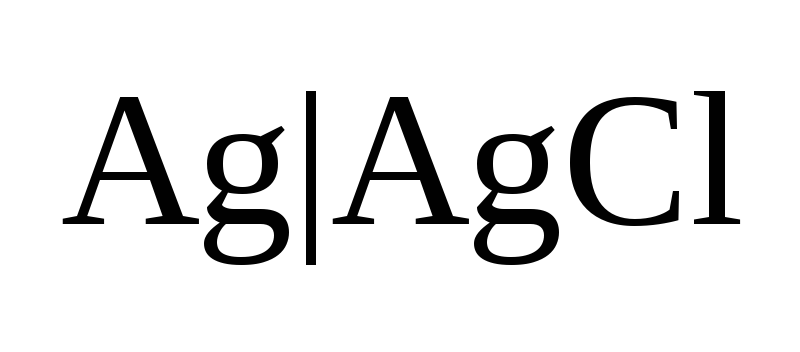 Процессы
на электроде: Процессы
на электроде:
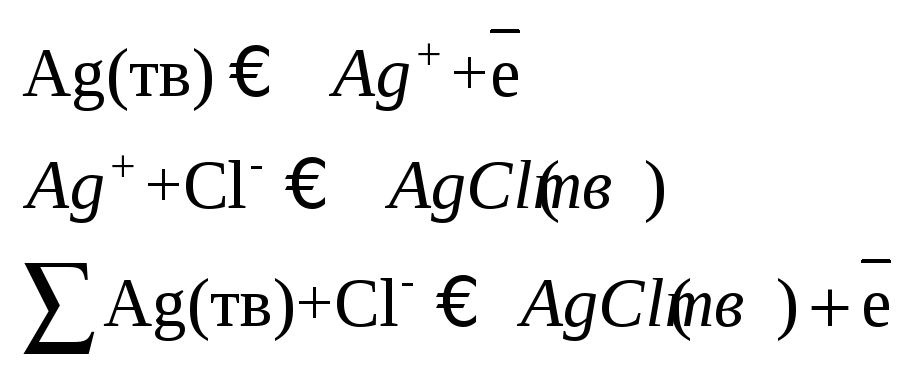 Электроды
3-го рода (газовые электроды).Известны
водородный, кислородный и хлорный
электроды. Потенциал газового электрода
зависит как от активности ионов, так
и от давления газа.Кроме электродов
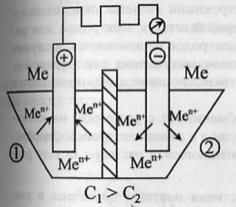
существуют
цепи (концентрационные
и альмагамные). Концентрационная
цепь.В
сосуд помещены 2 одинаковых электрода
и залиты раствором, содержащим ионы
металла.При замыкании цепи получают
развитие процессы, приводящие к
выравниванию концентрации всех
растворов.ЭДС элемента: Электроды
3-го рода (газовые электроды).Известны
водородный, кислородный и хлорный
электроды. Потенциал газового электрода
зависит как от активности ионов, так
и от давления газа.Кроме электродов
существуют
цепи (концентрационные
и альмагамные). Концентрационная
цепь.В
сосуд помещены 2 одинаковых электрода
и залиты раствором, содержащим ионы
металла.При замыкании цепи получают
развитие процессы, приводящие к
выравниванию концентрации всех
растворов.ЭДС элемента:
 Альмагамные
цепи.Альмагама
– сплав металла со ртутью, остающийся
жидким при комнатной температуре.В
сосуд залиты альмагамы с различной
концентрацией металла и электролит,
содержащий ионы металла.При работе
элемента: окисление в первом отделе,
восстновление – во втором.Процессы
продолжаются до выравнивания
концентраций электролитов и альмагам.В
принципе любой электрод
окислительно-восстановительный,
но этот термин применяется только в
том случае, если материал электродов
не изменяется, а служит лишь источником
или приемником электронов.Эти электроды,
таким образом, обеспечивают отвод/подвод
электронов.Имеются таблицы стандартных
окислительно-восстановительных
потенциалов. Альмагамные
цепи.Альмагама
– сплав металла со ртутью, остающийся
жидким при комнатной температуре.В
сосуд залиты альмагамы с различной
концентрацией металла и электролит,
содержащий ионы металла.При работе
элемента: окисление в первом отделе,
восстновление – во втором.Процессы
продолжаются до выравнивания
концентраций электролитов и альмагам.В
принципе любой электрод
окислительно-восстановительный,
но этот термин применяется только в
том случае, если материал электродов
не изменяется, а служит лишь источником
или приемником электронов.Эти электроды,
таким образом, обеспечивают отвод/подвод
электронов.Имеются таблицы стандартных
окислительно-восстановительных
потенциалов.
|
50.Электролиз.
Последовательность разряда ионов на
катоде и аноде. Электролиз
- это окислительно-восстановительный
процесс, протекающий при прохождении
постоянного тока через раствор или
расплав электролита.Сущность
электролиза:
на катоде(-) идет процесс восстановления,
на аноде(+) – процесс окисления.Пример.
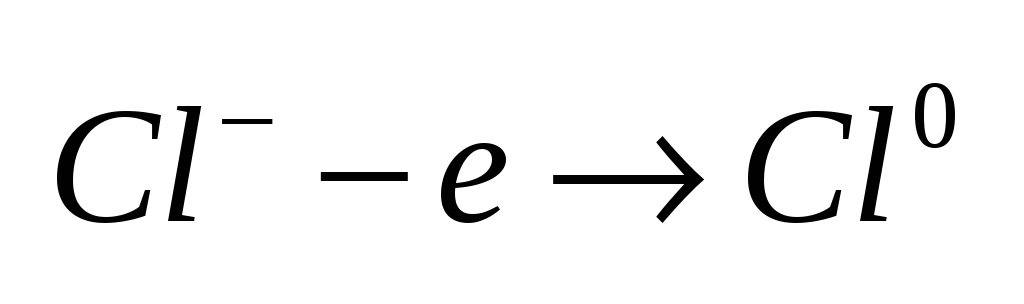 Различают
первичные
(электронный) и вторичные
(химический) процессы.Последовательность
разряда ионов в водных растворах.Вода
частично ионизирована. Различают
первичные
(электронный) и вторичные
(химический) процессы.Последовательность
разряда ионов в водных растворах.Вода
частично ионизирована.
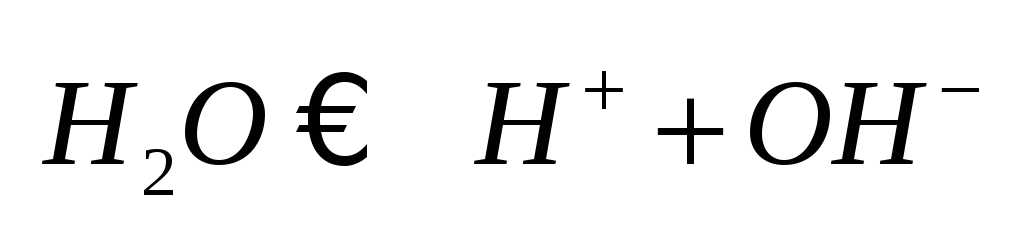 На катоде в первую очередь восстанавливается
тот катион, потенциал которого более
положителен.Все металлы можно разделить
на 3
группы.1-я
группа
– с наименьшей алгебраической величиной
На катоде в первую очередь восстанавливается
тот катион, потенциал которого более
положителен.Все металлы можно разделить
на 3
группы.1-я
группа
– с наименьшей алгебраической величиной
 от Li до Al (включительно). При электролизе
водных растворов, содержащих ионы
металлов 1-й группы на катоде идет
только процесс восстановление катионов
Н+.2-я
группа
- со средней алгебраической величиной
от Li до Al (включительно). При электролизе
водных растворов, содержащих ионы
металлов 1-й группы на катоде идет
только процесс восстановление катионов
Н+.2-я
группа
- со средней алгебраической величиной
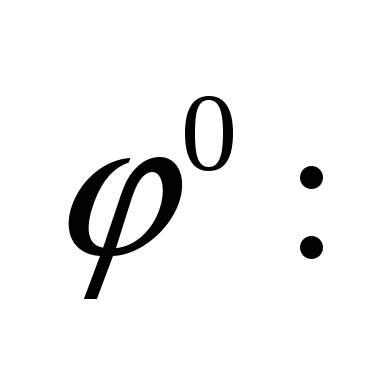 от Mn
до Fe
(Fe3+).
При электолизе водных растворов,
содержащих ионы Ме 2ой группы на катоде
идут 2 процесса: Men++nē®Me°,
H++ē®H.
от Mn
до Fe
(Fe3+).
При электолизе водных растворов,
содержащих ионы Ме 2ой группы на катоде
идут 2 процесса: Men++nē®Me°,
H++ē®H.
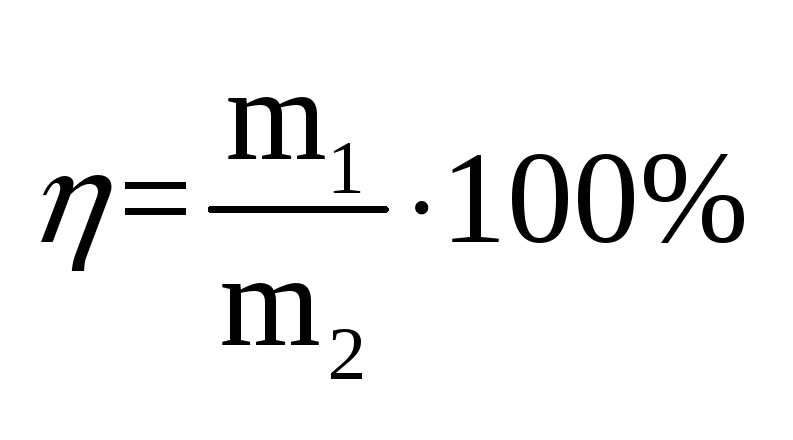 - выход по току, отношение практически
полученного на катоде вещества к
теоретически возможному, которое
должно было бы выделиться по закону
Фарадея.3-я
группа
– с наибольшей алгебраической величиной
- выход по току, отношение практически
полученного на катоде вещества к
теоретически возможному, которое
должно было бы выделиться по закону
Фарадея.3-я
группа
– с наибольшей алгебраической величиной
 все
Ме, расположенные в ряду напряжений
после водорода. На катоде – только
восстановление катионов Ме, Меn++nē®Ме°.
Порядок окисления анионов на аноде:
на аноде в 1-ю очередь окисляется анион, все
Ме, расположенные в ряду напряжений
после водорода. На катоде – только
восстановление катионов Ме, Меn++nē®Ме°.
Порядок окисления анионов на аноде:
на аноде в 1-ю очередь окисляется анион,
 которого более отрицателен.В случае
нерастворимого анода (графит, уголь,
Pt, Au, Ir) в первую очередь окисляются
анионы бескислородных кислот. Если
этих ионов нет, то если среда щелочная,
окисляются анионы гидроксила. Если
среда кислая или нейтральная, то имеет
место прямое окисление воды.В случае
растворимого анода, имеет место
процесс:
которого более отрицателен.В случае
нерастворимого анода (графит, уголь,
Pt, Au, Ir) в первую очередь окисляются
анионы бескислородных кислот. Если
этих ионов нет, то если среда щелочная,
окисляются анионы гидроксила. Если
среда кислая или нейтральная, то имеет
место прямое окисление воды.В случае
растворимого анода, имеет место
процесс:

|
51.Законы
Фарадея. Выход по току.Первый закон:
при электролизе данного электролита
количества веществ, выделяющихся на
электродах, прямо пропорционально
количеству электричества, прошедшему
через электролит.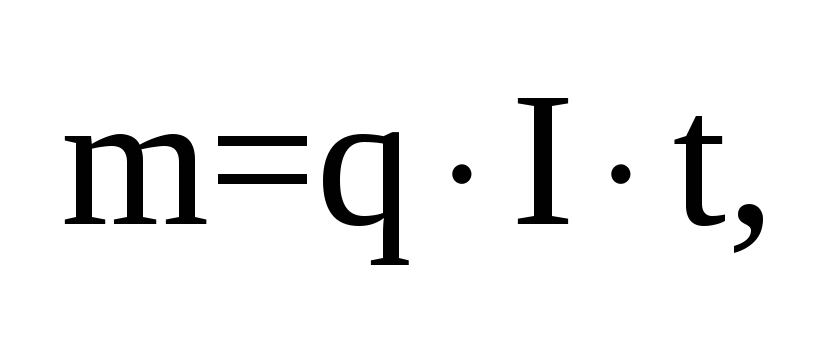 q
– электрохимический
эквивалент.Второй
закон:
при электролизе различных электролитов
одинаковые количества электричества
выделяют на электродах такие количества
веществ, которые прямо пропорциональны
их химическим эквивалентам.Пример.
При прохождении 1 фарадея (96500 Кл)
электричества на электродах выделяется
1 г-экв вещества.В формулу первого
закона следует ввести поправочный
сомножитель – выход по току.Закон
Фарадея:
q
– электрохимический
эквивалент.Второй
закон:
при электролизе различных электролитов
одинаковые количества электричества
выделяют на электродах такие количества
веществ, которые прямо пропорциональны
их химическим эквивалентам.Пример.
При прохождении 1 фарадея (96500 Кл)
электричества на электродах выделяется
1 г-экв вещества.В формулу первого
закона следует ввести поправочный
сомножитель – выход по току.Закон
Фарадея:
 Электрический
эквивалент
q
– количество вещества в мг, выделяющееся
на электродах при прохождении 1 Кл
электричества.Вторая
формулировка. Электрический эквивалент
q
– количество вещества в г, выделяющееся
на электродах при прохождении 1 А*ч
электричества.q=Э/Ф,
Э – г-экв.Удельный
расход энергии при электролизе:
W=U*I*t/m=U/(q*η),
[Вт*ч/г].
Электрический
эквивалент
q
– количество вещества в мг, выделяющееся
на электродах при прохождении 1 Кл
электричества.Вторая
формулировка. Электрический эквивалент
q
– количество вещества в г, выделяющееся
на электродах при прохождении 1 А*ч
электричества.q=Э/Ф,
Э – г-экв.Удельный
расход энергии при электролизе:
W=U*I*t/m=U/(q*η),
[Вт*ч/г].
|
|
59.Адсорбция
и абсорбция.
Адсорбция-процесс
изменения концентрации у поверхности
раздела двух фаз, а в более узком и
употребительном- это повышение
концентрации одного вещества у
поверхности раздела двух фаз, из
которых одна обычно является твердым
телом.
Поглощаемое
вещество, ещё находящееся в объёме
фазы, называют адсорбтив, поглощённое
— адсорбат. В более узком смысле под
адсорбцией часто понимают поглощение
примеси из газа или жидкости твёрдым
веществом — адсорбентом. При этом,
как и в общем случае адсорбции,
происходит концентрирование примеси
на границе раздела адсорбент-жидкость
либо адсорбент-газ. Процесс, обратный
адсорбции, то есть перенос вещества
с поверхности раздела фаз в объём
фазы, называется десорбция.
Абсорбция-
поглощения сорбата всем объёмом
сорбента. Абсорбция — частный случай
сорбции.
Абсорбция,
как правило, означает поглощение газов
в объёме жидкости или реже твёрдого
тела. Поглощение твёрдым абсорбентом,
например, водорода палладием, называют
окклюзией. Для процесса поглощения
молекул газа или жидкости поверхностью
твёрдого тела в русском языке
используется термин адсорбция.
На
практике абсорбции подвергают не
отдельные газы, а газовые смеси,
составные части которых поглощаются
|
|
53.Основные
методы борьбы с коррозией.Коррозия –
самопроизвольно
протекающий процесс поверхностного
окисления металла в результате его
химического или электрохимического
взаимодействия с окружающей средой.В
результате коррозии металл из свободного
состояния переходит в связанное.
Потери от коррозии велики: десятки
миллиардов долларов в индустриально-развитых
странах.Методы
борьбы различны:
-антикоррозийное
легирование
металла
– введение
в металл добавок, чтобы повысить
стойкость основного металла.защитные
покрытия
(металлические и неметаллические).металлические
наносятся под давлением сжатого
воздуха. характерно покрытие листового
материала тонким слоем другого
материала.неметаллические – лаки
,краски, битум, солидол.-ингибиторы
коррозии.вещества,
замедляющие процесс разрушения
металла.Пример.
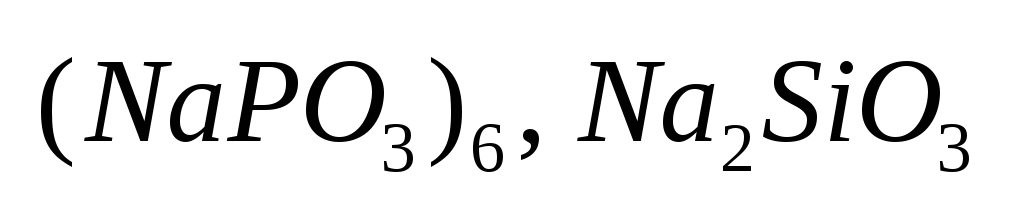 -электрозащита.защищаемый
металл приводят в контакт с менее
благородным металлом (цинк или
магний). -электрозащита.защищаемый
металл приводят в контакт с менее
благородным металлом (цинк или
магний).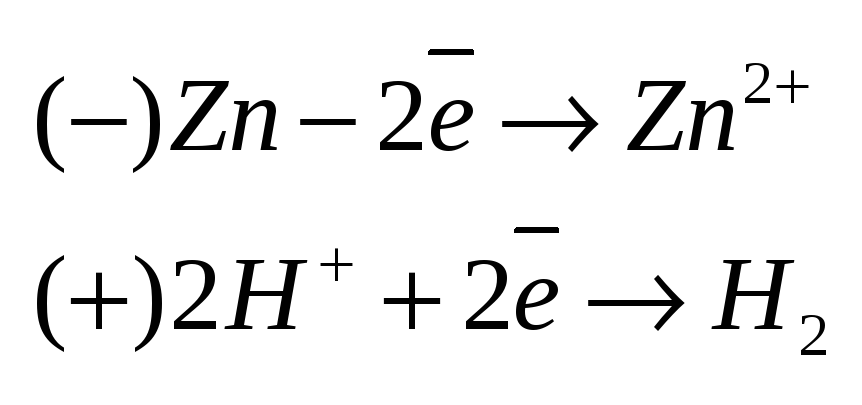 Поток
электронов направляется к защищаемому
металлу.Этот вид защиты используется
для магистральных труб, корпусов
кораблей и т.д. Поток
электронов направляется к защищаемому
металлу.Этот вид защиты используется
для магистральных труб, корпусов
кораблей и т.д.
|
|
  52.Коррозия
металлов. Химическая и электрохимическая
коррозия.Коррозия – самопроизвольно
протекающий процесс поверхностного
окисления металла в результате его
химического или электрохимического
взаимодействия с окружающей средой.В
результате коррозии металл из свободного
состояния переходит в связанное.
Потери от коррозии велики: десятки
миллиардов долларов в индустриально-развитых
странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены). 52.Коррозия
металлов. Химическая и электрохимическая
коррозия.Коррозия – самопроизвольно
протекающий процесс поверхностного
окисления металла в результате его
химического или электрохимического
взаимодействия с окружающей средой.В
результате коррозии металл из свободного
состояния переходит в связанное.
Потери от коррозии велики: десятки
миллиардов долларов в индустриально-развитых
странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены).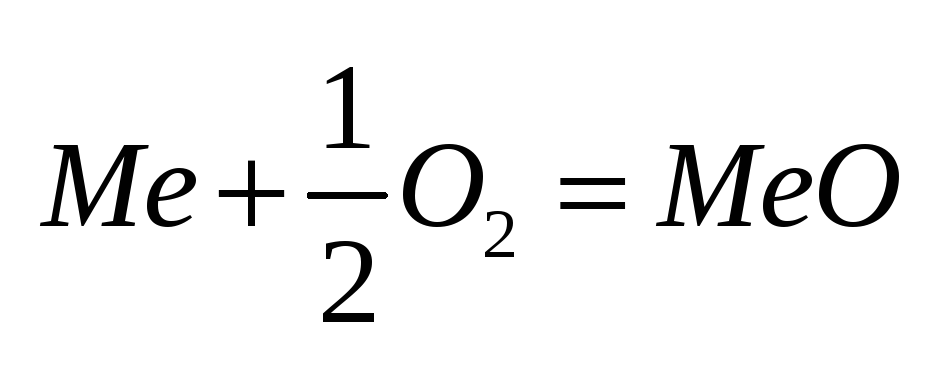 На поверхности металла образуется
твердая пленка оксида.Скорость
окисления зависит от прочности пленки
(наличия или отсутствия трещин). Если
пленка растягивается, трещины образуются
легко. Если сжимается – гораздо
труднее.Это зависит от отношения
мольных объемов окислителя и металла.
На поверхности металла образуется
твердая пленка оксида.Скорость
окисления зависит от прочности пленки
(наличия или отсутствия трещин). Если
пленка растягивается, трещины образуются
легко. Если сжимается – гораздо
труднее.Это зависит от отношения
мольных объемов окислителя и металла.
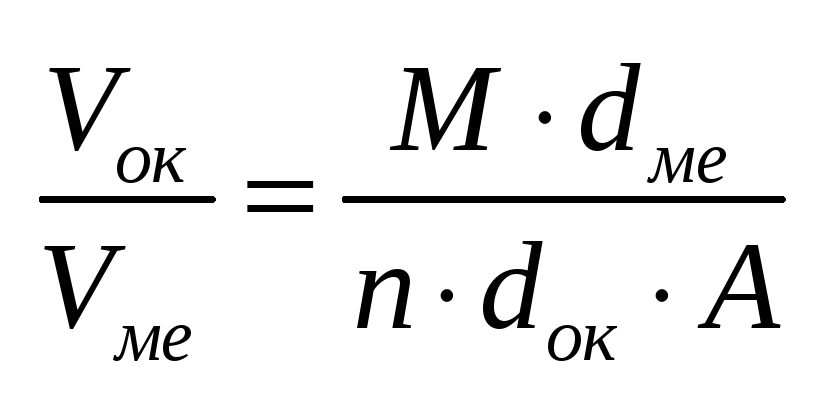 М – молекулярная масса оксида, d
– плотность, n
– число атомов в молекуле оксида, А –
атомная масса металла.Если отношение
<1
=> пленка растягивается, если >1
=> сжимается.Некоторые металлы
(железо, алюминий, хром, нержавеющая
сталь) могут подвергаться пассивации
(образование на поверхности под
действием реагентов слоев, препятствующих
коррозии).Пример.
М – молекулярная масса оксида, d
– плотность, n
– число атомов в молекуле оксида, А –
атомная масса металла.Если отношение
<1
=> пленка растягивается, если >1
=> сжимается.Некоторые металлы
(железо, алюминий, хром, нержавеющая
сталь) могут подвергаться пассивации
(образование на поверхности под
действием реагентов слоев, препятствующих
коррозии).Пример.
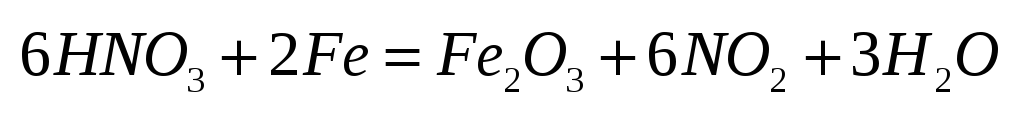 Активными
газами, вызывающими газовую коррозию
являются – хлор, фтор, кислород,
сероводород.Жидкостная
коррозия – разрушение металла в жидкой
непроводящей среде (нефть, бензин,
керосин, смазочные масла). Скорость
невелика.Электрохимическая
коррозия (гальванокоррозия и
электрокоррозия).Гальванокоррозия.
При
протекании процесса разрушающийся
металл является отрицательным
электродом.Рассмотрим пример.На
границе «металл-жидкость» образуется
слой ионов железа, удерживаемых
отрицательно заряженным металлом у
своей поверхности. Ионы железа
удерживают на расстоянии ионы водорода,
не давая им восстановиться за счет
электронов железа. Отсюда, коррозионная
стойкость химически чистого железа.В
случае технического железа (содержит
примеси) происходит восстановление
ионов водорода (пример примесей –
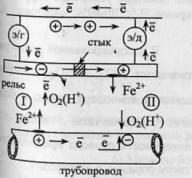
углерод).Электрокоррозия.Идет
процесс электролиза под действием
тока от внешнего источника.Рассмотрим
пример.Коррозия
стального трубопровода в почве под
действием электрических токов.
Возникают 2 участка: 1. где рельс
(источник тока) играет роль катода
(-), а участок провода под ним – роль
анода (+).2. справа от стыка. рельс –
анод, провод – катод.Слева от стыка
разрушается трубопровод, справа –
рельс.Разрушение происходит локально
– на ограниченном участке. Активными
газами, вызывающими газовую коррозию
являются – хлор, фтор, кислород,
сероводород.Жидкостная
коррозия – разрушение металла в жидкой
непроводящей среде (нефть, бензин,
керосин, смазочные масла). Скорость
невелика.Электрохимическая
коррозия (гальванокоррозия и
электрокоррозия).Гальванокоррозия.
При
протекании процесса разрушающийся
металл является отрицательным
электродом.Рассмотрим пример.На
границе «металл-жидкость» образуется
слой ионов железа, удерживаемых
отрицательно заряженным металлом у
своей поверхности. Ионы железа
удерживают на расстоянии ионы водорода,
не давая им восстановиться за счет
электронов железа. Отсюда, коррозионная
стойкость химически чистого железа.В
случае технического железа (содержит
примеси) происходит восстановление
ионов водорода (пример примесей –
углерод).Электрокоррозия.Идет
процесс электролиза под действием
тока от внешнего источника.Рассмотрим
пример.Коррозия
стального трубопровода в почве под
действием электрических токов.
Возникают 2 участка: 1. где рельс
(источник тока) играет роль катода
(-), а участок провода под ним – роль
анода (+).2. справа от стыка. рельс –
анод, провод – катод.Слева от стыка
разрушается трубопровод, справа –
рельс.Разрушение происходит локально
– на ограниченном участке.
|
|
54.Кристаллическое
состояние вещества. Химическая связь
в кристаллах.Твердые
вещества могут находиться в аморфном
или кристаллическом состояниях.Вещества
в аморфном состоянии не имеют четкой
структуры, их иногда называют
«переохлажденными жидкостями с
аномально высокой вязкостью».Кристаллические
структуры.Наименьшая
структурная единица – элементарная
ячейка. В зависимости от решеток и
углов между характеристическими осями
различают 7 основных видов (кубическая,
ромбоэдрическая и пр.).Тип кристаллической
системы определяется природой и
размерами частиц, видом химических
связей между ними, температурой и
другими факторами.Многие соединения
могут существовать в двух и более
кристаллических структурах. Это
явление – полиморфизм.Все
кристаллы можно разделить по видам
химической связи.
Стоит отметить, что существуют кристаллы
со смешанными связями.1.
Молекулярная связь.В
узлах кристаллических решеток находятся
молекулы, между которыми дейтсвуют
вандерваальсовы силы, имеющие невысокую
энергию.Для кристаллов с молекулярными
связями характерны низкие температуры
плавления и высокая сжимаемость.2.
Ковалентная связь.В
узлах кристаллов располагаются атомы,
образующие прочные ковалентные
связи.Это обуславливает высокую
энергию решетки.Кристаллы с ковалентной
связью - диэлектрики или полупроводники.
Типичными примеры: алмаз и кремний.3.
Ионная связь.Структурные
единицы – положительно и отрицательно
заряженные ионы, между которыми
происходит электростатическое
взаимодействие, характеризуемое
высокой энергией.Кристаллы с ионной
связью при низких температурах являются
диэлектриками. При температурах
близких к температуре плавления они
становятся проводниками электричества.4.
Металлическая связь.Специфические
свойства металлов (высокая проводимость,
теплопроводность, ковкость, пластичность,
металлический блеск) можно объяснить
особым типом связи – металлическая.Во
всех узлах кристаллической решётки
расположены положительные ионы
металла. Между ними беспорядочно
движутся валентные электроны,
отщепившиеся от атомов при образовании
ионов. Эти электроны удерживают вместе
положительные ионы, в противном случае
решётка распалась бы под действием
сил отталкивания между ионами.
5.
Смешанная связь.Тот
или иной вид связи встречается редко,
обычно – наложение двух или более
связей.
|
55.
Составные
части системы и компоненты. Правило
фаз.
Правило
фаз записывается следующим образом:
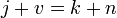
где
j — число фаз (например, агрегатных
состояний вещества);
v —
число степеней свободы, то есть
независимых параметров (температура,
давление, концентрация компонентов),
которые полностью определяют состояние
системы при равновесии и которые можно
менять без изменения числа и природы
фаз;
k —
число компонентов системы — число
входящих в систему индивидуальных
веществ за вычетом числа химических
уравнений, связывающих эти вещества.
Иначе говоря, это минимальное количество
веществ, из которых можно приготовить
каждую фазу системы.
n —
число переменных, характеризующих
влияние внешних условий на равновесие
системы.
При
переменных давлении и температуре
правило фаз сводится к выражению:
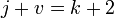
В
случае однокомпонентной системы оно
упрощается до:
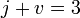 , ,
Отсюда
видно, например, что в однокомпонентной
системе три фазы (j=3) могут сосуществовать
при числе степеней свободы v, равном
нулю, то есть при фиксированных давлении
и температуре, что соответствует
тройной
точке
на фазовой диаграмме. Две фазы (j=2)
сосуществуют при произвольном
измененнии либо давления, либо
температуры, когда вторая из этих
переменных не является независимой
(v=1), то есть двухфазному равновесию
на фазовой диаграмме соответствует
линия. Если фаза одна (j=1), число степеней
свободы системы равно двум, то есть
температура и давление могут менятся
независимо в пределах некоторой
области на фазовой диаграмме —
пока система не окажется на одной из
линий двухфазного равновесия.
Иногда
правило фаз записывают следующим
образом:
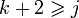
то
есть при равновесии число фаз в системе
меньше либо равно числу компонентов
плюс 2.
|
|
5  6.Сущность
термографического анализа. Кривые
нагревания и охлаждения.Термографический
анализ
– кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния)
строят исходя из кривых охлаждения,
которые изображаются в координатах:
температура(Оу), время(Ох). Рассмотрим
кривые
охлаждения
двух систем. Система I
в интервале t1-t2
не испытывает никаких фазовых
превращений, температура меняется
монотонно. Кривая II
отвечают охлаждению воды от 150
o
C
(пар при атмосферном давлении) до 0
o
C
и ниже. При 100
o
C
наблюдается горизонтальный участок,
отвечающий фазовому переходу –
процессу конденсации пара, температура
поддерживается низменной, пока не
исчезнет весь пар. Постоянство
температуры обеспечивается за счёт
выделения в процессе конденсации пара
теплоты испарения воды. От 100
o
C
до 0
o
C
наблюдается монотонный ход кривой
охлаждения – остывает жидкая вода.
При 0
o
C
наблюдается второй горизонтальный
участок, отвечающий фазовому переходу
– процессу кристаллизации. Температура
поддерживается постоянной за счет
выделения теплоты плавления.Рассмотрим
кривые
охлаждения
чистого металла (I)
и сплава с так называемой эвтектикой
(II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc,
отвечающая процессу кристаллизации
металла. При
tпл
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.Кривая II
отвечает охлаждению сплава А-В. От “а”
до “a’
“ температура меняется монотонно,
остывает жидкая фаза. При достижении
точки a’
из жидкой фазы начинают выпадать
кристаллы А – одного из компонентов
сплава, при этом жидкая фаза за счет
этого начнет обогащаться компонентом
В. Таким образом, в интервале a’-b
в равновесии находятся жидкая
и твердая фазы различного состава,
площадки на кривой охлаждения не
наблюдается. За счет выделения при
кристаллизации А теплоты плавления
этого компонента темп охлаждения
сплава замедляется, и на кривой
наблюдается перелом. Выпадение
кристаллов А продолжается до тех пор,
пока жидкая фаза не достигнет так
называемого “эвтектического состава”.
Основной особенностью эвтектического
сплава является то, что он кристаллизуется
подобно чистому компоненту – на кривой
охлаждения наблюдается площадка. Из
жидкой фазы одновременно выпадают
кристаллы А и В и, таким образом при
tЕ
(отрезок bc)
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Отрезок
cd
отвечают охлаждению твердого
сплава.Остановки в падении температуры
могут наблюдаться и на кривой охлаждения
уже твердого металла, указываю на
переходы металла из одной аллотропной
формы в другую. 6.Сущность
термографического анализа. Кривые
нагревания и охлаждения.Термографический
анализ
– кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния)
строят исходя из кривых охлаждения,
которые изображаются в координатах:
температура(Оу), время(Ох). Рассмотрим
кривые
охлаждения
двух систем. Система I
в интервале t1-t2
не испытывает никаких фазовых
превращений, температура меняется
монотонно. Кривая II
отвечают охлаждению воды от 150
o
C
(пар при атмосферном давлении) до 0
o
C
и ниже. При 100
o
C
наблюдается горизонтальный участок,
отвечающий фазовому переходу –
процессу конденсации пара, температура
поддерживается низменной, пока не
исчезнет весь пар. Постоянство
температуры обеспечивается за счёт
выделения в процессе конденсации пара
теплоты испарения воды. От 100
o
C
до 0
o
C
наблюдается монотонный ход кривой
охлаждения – остывает жидкая вода.
При 0
o
C
наблюдается второй горизонтальный
участок, отвечающий фазовому переходу
– процессу кристаллизации. Температура
поддерживается постоянной за счет
выделения теплоты плавления.Рассмотрим
кривые
охлаждения
чистого металла (I)
и сплава с так называемой эвтектикой
(II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc,
отвечающая процессу кристаллизации
металла. При
tпл
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.Кривая II
отвечает охлаждению сплава А-В. От “а”
до “a’
“ температура меняется монотонно,
остывает жидкая фаза. При достижении
точки a’
из жидкой фазы начинают выпадать
кристаллы А – одного из компонентов
сплава, при этом жидкая фаза за счет
этого начнет обогащаться компонентом
В. Таким образом, в интервале a’-b
в равновесии находятся жидкая
и твердая фазы различного состава,
площадки на кривой охлаждения не
наблюдается. За счет выделения при
кристаллизации А теплоты плавления
этого компонента темп охлаждения
сплава замедляется, и на кривой
наблюдается перелом. Выпадение
кристаллов А продолжается до тех пор,
пока жидкая фаза не достигнет так
называемого “эвтектического состава”.
Основной особенностью эвтектического
сплава является то, что он кристаллизуется
подобно чистому компоненту – на кривой
охлаждения наблюдается площадка. Из
жидкой фазы одновременно выпадают
кристаллы А и В и, таким образом при
tЕ
(отрезок bc)
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Отрезок
cd
отвечают охлаждению твердого
сплава.Остановки в падении температуры
могут наблюдаться и на кривой охлаждения
уже твердого металла, указываю на
переходы металла из одной аллотропной
формы в другую.
|
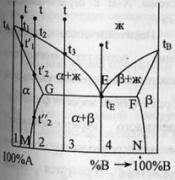 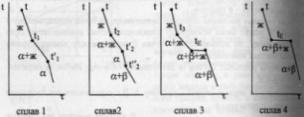 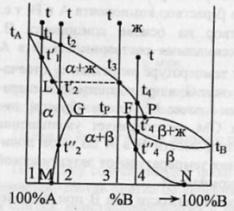 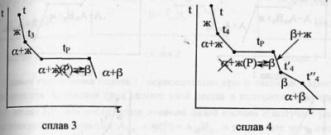 57.
Диаграмма плавкости бинарной системы
с ограниченными твердыми растворами.
Диаграмма состояния системы
- диаграмма, указывающая, в каких
фазовых состояниях находится система
в зависимости от условий: температура,
давление и состав. Диаграммы
плавкости
– частный вид диаграмм состояния.Для
данных систем характерны полная
взаимная растворимость компонентов
в жидком состоянии и ограниченная - в
твердом. Если твердые растворы образуют
эвтектику,
то точка нонвариантного равновесия
Е лежит ниже t
плавления чистых компонентов,если же
перитектику,то
нонвариантная точка P
лежит между t
плавления чистых компонентов.Пример.
Cu-Ag,Pb-Sn;
Hg-Cd.Рассмотрим
первый случай.Система А-В с
ограничен.тв.р-рами- с эвтектикой.
В системе имеется 2 твердых раствора:
α - р-р компонентов В в А и β- р-р компонента
А в В.Max
растворимость В в А при t
эвтектики tЕ
отвечает точке G,
а при комнат.t
– точке M.
Линия GM
характеризует уменьшение растворимости
В в А по мере понижения t
от эвтектич-й до комнат-й.Линия
FN-снижение
растворимости А в В при понижении t
от tЕ
до
комнат-й.Кривые охлаждения 4
сплавов:1,2,3,4.На кривой охлаждения
сплава
1
имееются 2 перегиба,отвечающих началу
и концу выделения кристаллов тв.р-ра
α.На кривой охлаждения сплава
2
дополнительно наблюдается слабо
выраженный перегиб при t”2,отвечающий
частичному распаду в тв.состоянии
кристаллов α с выделением кристаллов
тв.р-ра β. Кривая охлаждения сплава
3:
при t3
из жид.фазы выделяются кристаллы
тв.р-ра α,жид.фаза при понижении от t3
до
tЕ
меняет свой состав по линии
t3Е,т.е.обогащается
компонентом В.Как только жид.фаза
достигнет состава Е,начинается
кристаллизация эвтектики-мех.смеси
2 тв.фаз-тв.р-ра α состава G
и тв.р-ра β состава F,на
кривой охлаждения наблюдается
площадка.Сплав
4
точно отвечает эвтектич.составу,кривая
охлаждения его подобна кривой охлаждения
чистого компонента. Система А-В с
ограничен.тв.р-рами- с перитектикой(т.Р).
Перитектическое превращение-результат
химического взаимодействия ранее
выпавшей тв.фазы с жид.фазой определенного
(перитектического) состава.В результате
этого взаимодействия образуется новая
тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4.
Кривые охлаждения 1 и 2 полностью похожи
на эвтектические.Кривая
охлаждения 3:в
интервале t
от t
до t3
идет охлаждение жид.фазы,и t
изменяется монотонно.При t3
из жид.фазы выпадают кристаллы тв.р-ра
α, на кривой охлаждения-перегиб.В
интервале t3-tP
жид.фаза меняет свой состав по линии
t3Е,а
тв.фаза по линии LG.Как
только жид.фаза достигнет состава
P(перитектического),получает
развитие перитектическая реакция.В
результате этой реакции исчезает
жид.фаза и ниже tP
наблюдается смесь 2 тв.фаз-тв.р-ров α
и β.На кривой охлаждения наблюдается
площадка,т.к. имеет место нонвариантное
превращение:С=К-Ф+1=2-3+1=0.Для сплава
4
при tP
в результате перитектической реакции
исчезает тв.р-ра α.В интервале tP
–t’4
из жид.фазы выпадают кристаллы тв.р-ра
β. От t’4
до t”4
происходит охлпждение тв.фазы β, а при
t”4
тв.р-р β частично распадается-с
выделением кристаллов тв.р-ра α. 57.
Диаграмма плавкости бинарной системы
с ограниченными твердыми растворами.
Диаграмма состояния системы
- диаграмма, указывающая, в каких
фазовых состояниях находится система
в зависимости от условий: температура,
давление и состав. Диаграммы
плавкости
– частный вид диаграмм состояния.Для
данных систем характерны полная
взаимная растворимость компонентов
в жидком состоянии и ограниченная - в
твердом. Если твердые растворы образуют
эвтектику,
то точка нонвариантного равновесия
Е лежит ниже t
плавления чистых компонентов,если же
перитектику,то
нонвариантная точка P
лежит между t
плавления чистых компонентов.Пример.
Cu-Ag,Pb-Sn;
Hg-Cd.Рассмотрим
первый случай.Система А-В с
ограничен.тв.р-рами- с эвтектикой.
В системе имеется 2 твердых раствора:
α - р-р компонентов В в А и β- р-р компонента
А в В.Max
растворимость В в А при t
эвтектики tЕ
отвечает точке G,
а при комнат.t
– точке M.
Линия GM
характеризует уменьшение растворимости
В в А по мере понижения t
от эвтектич-й до комнат-й.Линия
FN-снижение
растворимости А в В при понижении t
от tЕ
до
комнат-й.Кривые охлаждения 4
сплавов:1,2,3,4.На кривой охлаждения
сплава
1
имееются 2 перегиба,отвечающих началу
и концу выделения кристаллов тв.р-ра
α.На кривой охлаждения сплава
2
дополнительно наблюдается слабо
выраженный перегиб при t”2,отвечающий
частичному распаду в тв.состоянии
кристаллов α с выделением кристаллов
тв.р-ра β. Кривая охлаждения сплава
3:
при t3
из жид.фазы выделяются кристаллы
тв.р-ра α,жид.фаза при понижении от t3
до
tЕ
меняет свой состав по линии
t3Е,т.е.обогащается
компонентом В.Как только жид.фаза
достигнет состава Е,начинается
кристаллизация эвтектики-мех.смеси
2 тв.фаз-тв.р-ра α состава G
и тв.р-ра β состава F,на
кривой охлаждения наблюдается
площадка.Сплав
4
точно отвечает эвтектич.составу,кривая
охлаждения его подобна кривой охлаждения
чистого компонента. Система А-В с
ограничен.тв.р-рами- с перитектикой(т.Р).
Перитектическое превращение-результат
химического взаимодействия ранее
выпавшей тв.фазы с жид.фазой определенного
(перитектического) состава.В результате
этого взаимодействия образуется новая
тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4.
Кривые охлаждения 1 и 2 полностью похожи
на эвтектические.Кривая
охлаждения 3:в
интервале t
от t
до t3
идет охлаждение жид.фазы,и t
изменяется монотонно.При t3
из жид.фазы выпадают кристаллы тв.р-ра
α, на кривой охлаждения-перегиб.В
интервале t3-tP
жид.фаза меняет свой состав по линии
t3Е,а
тв.фаза по линии LG.Как
только жид.фаза достигнет состава
P(перитектического),получает
развитие перитектическая реакция.В
результате этой реакции исчезает
жид.фаза и ниже tP
наблюдается смесь 2 тв.фаз-тв.р-ров α
и β.На кривой охлаждения наблюдается
площадка,т.к. имеет место нонвариантное
превращение:С=К-Ф+1=2-3+1=0.Для сплава
4
при tP
в результате перитектической реакции
исчезает тв.р-ра α.В интервале tP
–t’4
из жид.фазы выпадают кристаллы тв.р-ра
β. От t’4
до t”4
происходит охлпждение тв.фазы β, а при
t”4
тв.р-р β частично распадается-с
выделением кристаллов тв.р-ра α.
|
58.Поверхностные
явления. Понятие поверхностного
натяжения.Поверхностное натяжение
– избыток свободной энергии в
поверхностном слое, отнесенный к
 поверхности поглощающего тела.
поверхности поглощающего тела.
 Поверхностное
растяжение растворов зависит от
природы растворителя и растворенного
вещества, от концентрации последнего
и от температуры. Поверхностное
натяжение как функция концентрации
растворенного вещества при Т-const
- изотерма
поверхностного натяжения. Поверхностное
растяжение растворов зависит от
природы растворителя и растворенного
вещества, от концентрации последнего
и от температуры. Поверхностное
натяжение как функция концентрации
растворенного вещества при Т-const
- изотерма
поверхностного натяжения.
 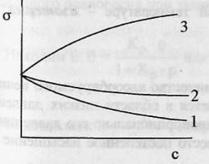 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
C
в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности. 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
C
в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.
Пове́рхностные
явле́ния —
совокупность явлений, обусловленных
особыми свойствами тонких слоёв
вещества на границе соприкосновения
фаз. К поверхностным явлениям относятся
процессы, происходящие на границе
раздела фаз, в межфазном поверхностном
слое и возникающие в результате
взаимодействия сопряжённых фаз.
Поверхностные
явления обусловлены тем, что в
поверхностных слоях на межфазных
границах вследствие различного состава
и строения соприкасающихся фаз и
соответственно из-за различия в связях
поверхностных атомов
и молекул
со стороны разных фаз существует
ненасыщенное поле межатомных,
межмолекулярных сил. Вследствие этого
атомы и молекулы в поверхностных слоях
образуют особую структуру, а вещество
принимает особое состояние, отличающееся
от его состояния в объеме фаз различными
свойствами. Поверхностные
явления изучаются
коллоидной
химией.

|
|
|
|
|
|
|
60.Поверхностное
натяжение растворов. Изотерма
адсорбции.Поверхностное натяжение
– избыток свободной энергии в
поверхностном слое, отнесенный к
 поверхности поглощающего тела.
поверхности поглощающего тела.
 Поверхностное
растяжение растворов зависит от
природы растворителя и растворенного
вещества, от концентрации последнего
и от температуры. Поверхностное
натяжение как функция концентрации
растворенного вещества при Т-const
- изотерма
поверхностного натяжения. Поверхностное
растяжение растворов зависит от
природы растворителя и растворенного
вещества, от концентрации последнего
и от температуры. Поверхностное
натяжение как функция концентрации
растворенного вещества при Т-const
- изотерма
поверхностного натяжения.
 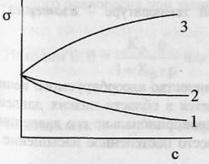 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции. 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции.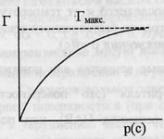 С
ростом давления увеличивается
количество адсорбируемого вещества.Лэнгмюр
при выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало.
3. адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения
адсорбента адсорбатом: С
ростом давления увеличивается
количество адсорбируемого вещества.Лэнгмюр
при выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало.
3. адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения
адсорбента адсорбатом:
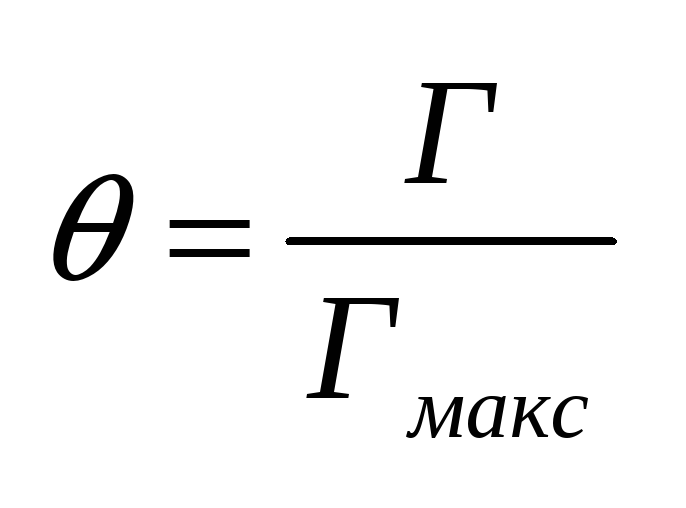 Скорость
адсорбции: Скорость
адсорбции:

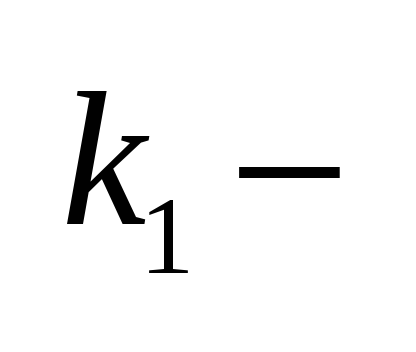 константа скорости адсорбции.Скорость
десорбции:
константа скорости адсорбции.Скорость
десорбции:

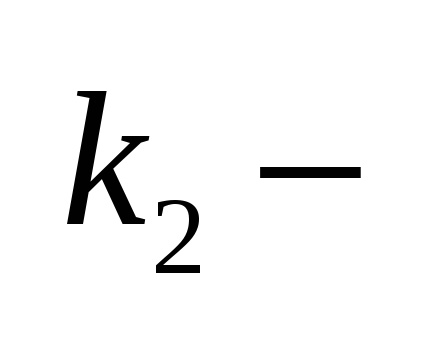 константа скорости десорбции.Адсорбционное
равновесие наступает при
константа скорости десорбции.Адсорбционное
равновесие наступает при
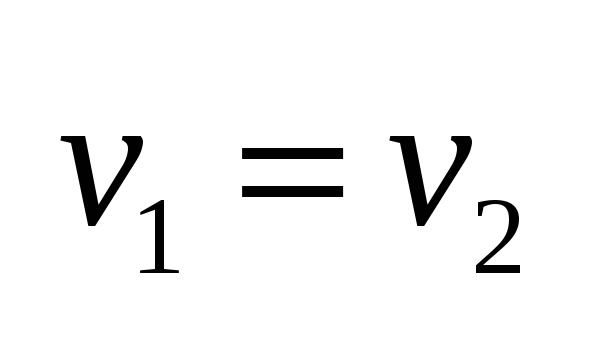 Уравнение
изотермы хорошо передает зависимости
в области низких и области высоких
давлений, но не всегда оправдывается
в промежуточной области.Процесс
адсорбции экзотермичен: поглощение
вещества протекает с выделением
теплоты, десорбция – с поглощением
теплоты.Если адсорбируются несколько
газов: Уравнение
изотермы хорошо передает зависимости
в области низких и области высоких
давлений, но не всегда оправдывается
в промежуточной области.Процесс
адсорбции экзотермичен: поглощение
вещества протекает с выделением
теплоты, десорбция – с поглощением
теплоты.Если адсорбируются несколько
газов:
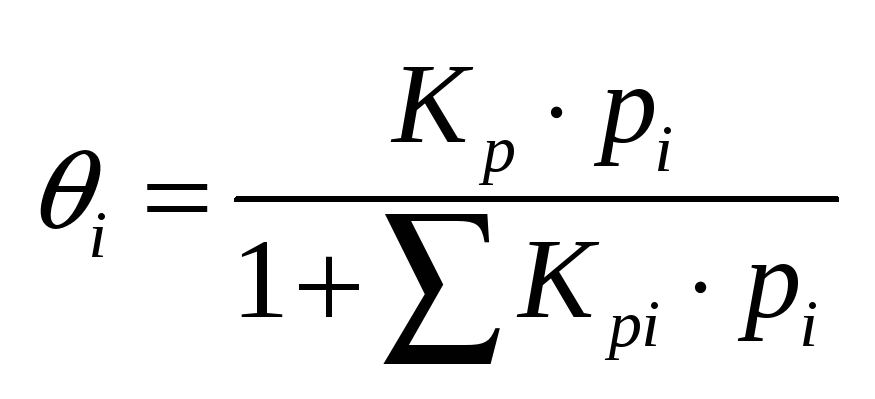 Для
адсорбции на неоднородной поверхностибыло
предложено эмпирическое уравнение
Фрейндлиха. Для
адсорбции на неоднородной поверхностибыло
предложено эмпирическое уравнение
Фрейндлиха.
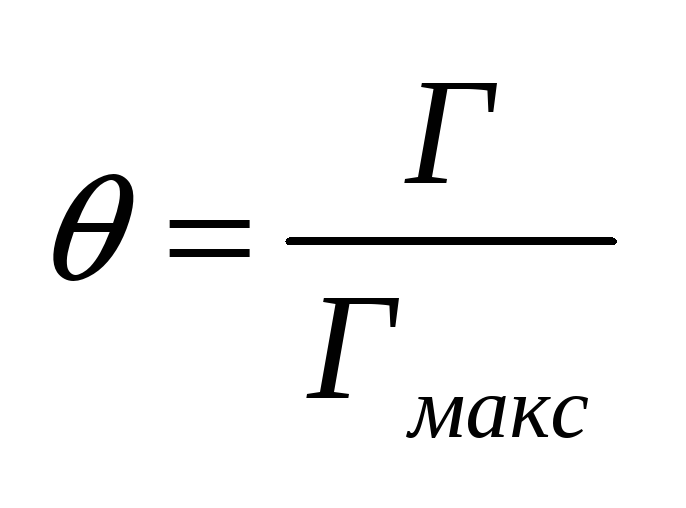
 к
и n
– коэффициенты, постоянные для данного
адсорбента и газа при данной
температуре.Уравнение Фрейндлиха,
наоборот, не отражает особенностей
изотермы в области высоких и низких
давлений, но для области промежуточных
давлений согласуются с опытными
данными. к
и n
– коэффициенты, постоянные для данного
адсорбента и газа при данной
температуре.Уравнение Фрейндлиха,
наоборот, не отражает особенностей
изотермы в области высоких и низких
давлений, но для области промежуточных
давлений согласуются с опытными
данными.
|
|
61.
Полимеры. Методы получения.
Полимеры—
неорганические и органические, аморфные
и кристаллические вещества, состоящие
из «мономерных звеньев», соединённых
в длинные макромолекулы химическими
или координационными связями. Полимер —
это высокомолекулярное соединение:
количество мономерных звеньев в
полимере (степень полимеризации)
должно быть достаточно велико. Во
многих случаях количество звеньев
может считаться достаточным, чтобы
отнести молекулу к полимерам, если
при добавлении очередного мономерного
звена молекулярные свойства не
изменяются.[1]
Как правило, полимеры — вещества с
молекулярной массой от нескольких
тысяч до нескольких миллионов
Полимеризация
и поликонденсация
Синтетические
полимеры получают в результате реакций
полимеризации и поликонденсации.
Полимеризация
—
это процесс соединения друг с другом
большого числа молекул мономера за
счет кратных связей (С = С, С = О и др.)
или раскрытия циклов, содержащих
гетероатомы (О, N, S). При полимеризации
обычно не происходит образования
низкомолекулярных побочных продуктов,
вследствие чего полимер и мономер
имеют один и тот же элементный
состав,
Поликонденсация
—
зто процесс соединения друг с другом
молекул одного или нескольких мономеров,
содержащих две и да более функциональные
группы (ОН, СО, СОС, NHS и др.) способные
к химическому взаимодействию, при
котором происходит отщепление
низкомолекулярных продуктов. Полимеры,
получаемые поликонденсационным
способом, по элементному составу не
соответствуют исходным мономерам.
Полимеризация
мономеров с кратными связями протекает
по законам цепных реакций в результате
разрыва непредельных связей.
Макромолекула при цепной полимеризации
образуется очень быстро и сразу же
приобретает конечные размеры, т. е не
возрастает при увеличении длительности
процесса.
Полимеризация мономеров
циклического строения происходит за
счет раскрытия цикла и в ряде случаев
пропекает не по цепному, а по ступенчатому
механизму. Макромолекула при ступенчатой
полимеризации образуется постепенно,
т. е. сначала образуется димер затем
тример и т.д., поэтому молекулярная
масса полимера растет со временем.
Принципиальное отличие ценной
полимеризации от ступенчатой и от
поликонденсации состоит в том, что на
разных стадиях процесса реакционная
смесь всегда состоит из мономера и
полимера и не содержит ди-, три-,
тетрамеров. С увеличением продолжительности
реакции растет лишь число макромолекул
полимера, а мономер расходуется
постепенно. Молекулярная масса полимера
не зависит от степени завершенности
реакции или, что то же, от конверсии
мономера, которая определяет только
выход полимера.
|
62.
Материалы,
получаемые на основе полимеров
1.На
основе полимеров получают волокна
путем продавливания растворов или
расплавов через фильеры с последующим
затвердеванием -
это полиамиды, полиакрилонитрилы и
др.2.
Полимерные пленки получают продавливанием
через фильеры с щелевидными отверстиями
или нанесением на движущую ленту. Их
используют как электроизоляционный
и упаковочный материал, основы магнитных
лент. 3. Лаки
-
растворы пленкообразующих веществ в
органических растворителях.4.
Клеи, композиции способные соединять
различные материалы вследствие
образования прочных связей между их
поверхностями клеевой прослойкой.5.
Пластмассы6. Композиты
(
композиционные материалы )
-
полимерная основа, армированная
наполнителем.
|
.
|


 38.Законы
Рауля.Особенность
растворов: давление пара растворителя
над раствором ниже, чем над чистым
растворителем. Первый
закон.Давление
пара растворителя над раствором
пропорционально мольной доле
растворителя в растворе.или Относительно
понижение давление пара растворителя
над раствором равно мольной доли
растворенного вещества.Введем
обозначения:
38.Законы
Рауля.Особенность
растворов: давление пара растворителя
над раствором ниже, чем над чистым
растворителем. Первый
закон.Давление
пара растворителя над раствором
пропорционально мольной доле
растворителя в растворе.или Относительно
понижение давление пара растворителя
над раствором равно мольной доли
растворенного вещества.Введем
обозначения: 46.Медно-цинковый
гальванический элемент Якоби-Даниэля.
Процессы на электродах. Понятие
ЭДС.Гальванический элемент
– любое устройство, дающее возможность
получать электрический ток за счет
проведения той или иной химической
реакции.Рассмотрим систему, в которой
медь и цинк в виде пластинок помещены
в растворы своих солей, разделенных
перегородкой – диафрагмой.
При разомкнутой цепи электроды
приобретают равновесные потенциалы,
которые отличаются по знаку и по
величине. При ее замыкании электроны
от цинкового электрода перемещаются
к медному. На электродах нарушается
равновесие:
46.Медно-цинковый
гальванический элемент Якоби-Даниэля.
Процессы на электродах. Понятие
ЭДС.Гальванический элемент
– любое устройство, дающее возможность
получать электрический ток за счет
проведения той или иной химической
реакции.Рассмотрим систему, в которой
медь и цинк в виде пластинок помещены
в растворы своих солей, разделенных
перегородкой – диафрагмой.
При разомкнутой цепи электроды
приобретают равновесные потенциалы,
которые отличаются по знаку и по
величине. При ее замыкании электроны
от цинкового электрода перемещаются
к медному. На электродах нарушается
равновесие:

 49.Типы
электродов. Окислительно-восстановительный
электроды.Электрод
– проводник 1 рода, погруженный в
раствор электролита в условиях
прохождения через него тока. Три
типа:
электроды первого, второго и третьего
рода.Электроды
1-го рода.Металлы,
погруженные в растворы своих солей.солей:
49.Типы
электродов. Окислительно-восстановительный
электроды.Электрод
– проводник 1 рода, погруженный в
раствор электролита в условиях
прохождения через него тока. Три
типа:
электроды первого, второго и третьего
рода.Электроды
1-го рода.Металлы,
погруженные в растворы своих солей.солей:

 52.Коррозия
металлов. Химическая и электрохимическая
коррозия.Коррозия – самопроизвольно
протекающий процесс поверхностного
окисления металла в результате его
химического или электрохимического
взаимодействия с окружающей средой.В
результате коррозии металл из свободного
состояния переходит в связанное.
Потери от коррозии велики: десятки
миллиардов долларов в индустриально-развитых
странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены).
52.Коррозия
металлов. Химическая и электрохимическая
коррозия.Коррозия – самопроизвольно
протекающий процесс поверхностного
окисления металла в результате его
химического или электрохимического
взаимодействия с окружающей средой.В
результате коррозии металл из свободного
состояния переходит в связанное.
Потери от коррозии велики: десятки
миллиардов долларов в индустриально-развитых
странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены).
 6.Сущность
термографического анализа. Кривые
нагревания и охлаждения.Термографический
анализ
– кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния)
строят исходя из кривых охлаждения,
которые изображаются в координатах:
температура(Оу), время(Ох). Рассмотрим
кривые
охлаждения
двух систем. Система I
в интервале t1-t2
не испытывает никаких фазовых
превращений, температура меняется
монотонно. Кривая II
отвечают охлаждению воды от 150
o
C
(пар при атмосферном давлении) до 0
o
C
и ниже. При 100
o
C
наблюдается горизонтальный участок,
отвечающий фазовому переходу –
процессу конденсации пара, температура
поддерживается низменной, пока не
исчезнет весь пар. Постоянство
температуры обеспечивается за счёт
выделения в процессе конденсации пара
теплоты испарения воды. От 100
o
C
до 0
o
C
наблюдается монотонный ход кривой
охлаждения – остывает жидкая вода.
При 0
o
C
наблюдается второй горизонтальный
участок, отвечающий фазовому переходу
– процессу кристаллизации. Температура
поддерживается постоянной за счет
выделения теплоты плавления.Рассмотрим
кривые
охлаждения
чистого металла (I)
и сплава с так называемой эвтектикой
(II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc,
отвечающая процессу кристаллизации
металла. При
tпл
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.Кривая II
отвечает охлаждению сплава А-В. От “а”
до “a’
“ температура меняется монотонно,
остывает жидкая фаза. При достижении
точки a’
из жидкой фазы начинают выпадать
кристаллы А – одного из компонентов
сплава, при этом жидкая фаза за счет
этого начнет обогащаться компонентом
В. Таким образом, в интервале a’-b
в равновесии находятся жидкая
и твердая фазы различного состава,
площадки на кривой охлаждения не
наблюдается. За счет выделения при
кристаллизации А теплоты плавления
этого компонента темп охлаждения
сплава замедляется, и на кривой
наблюдается перелом. Выпадение
кристаллов А продолжается до тех пор,
пока жидкая фаза не достигнет так
называемого “эвтектического состава”.
Основной особенностью эвтектического
сплава является то, что он кристаллизуется
подобно чистому компоненту – на кривой
охлаждения наблюдается площадка. Из
жидкой фазы одновременно выпадают
кристаллы А и В и, таким образом при
tЕ
(отрезок bc)
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Отрезок
cd
отвечают охлаждению твердого
сплава.Остановки в падении температуры
могут наблюдаться и на кривой охлаждения
уже твердого металла, указываю на
переходы металла из одной аллотропной
формы в другую.
6.Сущность
термографического анализа. Кривые
нагревания и охлаждения.Термографический
анализ
– кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния)
строят исходя из кривых охлаждения,
которые изображаются в координатах:
температура(Оу), время(Ох). Рассмотрим
кривые
охлаждения
двух систем. Система I
в интервале t1-t2
не испытывает никаких фазовых
превращений, температура меняется
монотонно. Кривая II
отвечают охлаждению воды от 150
o
C
(пар при атмосферном давлении) до 0
o
C
и ниже. При 100
o
C
наблюдается горизонтальный участок,
отвечающий фазовому переходу –
процессу конденсации пара, температура
поддерживается низменной, пока не
исчезнет весь пар. Постоянство
температуры обеспечивается за счёт
выделения в процессе конденсации пара
теплоты испарения воды. От 100
o
C
до 0
o
C
наблюдается монотонный ход кривой
охлаждения – остывает жидкая вода.
При 0
o
C
наблюдается второй горизонтальный
участок, отвечающий фазовому переходу
– процессу кристаллизации. Температура
поддерживается постоянной за счет
выделения теплоты плавления.Рассмотрим
кривые
охлаждения
чистого металла (I)
и сплава с так называемой эвтектикой
(II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc,
отвечающая процессу кристаллизации
металла. При
tпл
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.Кривая II
отвечает охлаждению сплава А-В. От “а”
до “a’
“ температура меняется монотонно,
остывает жидкая фаза. При достижении
точки a’
из жидкой фазы начинают выпадать
кристаллы А – одного из компонентов
сплава, при этом жидкая фаза за счет
этого начнет обогащаться компонентом
В. Таким образом, в интервале a’-b
в равновесии находятся жидкая
и твердая фазы различного состава,
площадки на кривой охлаждения не
наблюдается. За счет выделения при
кристаллизации А теплоты плавления
этого компонента темп охлаждения
сплава замедляется, и на кривой
наблюдается перелом. Выпадение
кристаллов А продолжается до тех пор,
пока жидкая фаза не достигнет так
называемого “эвтектического состава”.
Основной особенностью эвтектического
сплава является то, что он кристаллизуется
подобно чистому компоненту – на кривой
охлаждения наблюдается площадка. Из
жидкой фазы одновременно выпадают
кристаллы А и В и, таким образом при
tЕ
(отрезок bc)
в
равновесии находятся жидкая и твердая
фазы одинакового состава. Отрезок
cd
отвечают охлаждению твердого
сплава.Остановки в падении температуры
могут наблюдаться и на кривой охлаждения
уже твердого металла, указываю на
переходы металла из одной аллотропной
формы в другую.


 57.
Диаграмма плавкости бинарной системы
с ограниченными твердыми растворами.
Диаграмма состояния системы
- диаграмма, указывающая, в каких
фазовых состояниях находится система
в зависимости от условий: температура,
давление и состав. Диаграммы
плавкости
– частный вид диаграмм состояния.Для
данных систем характерны полная
взаимная растворимость компонентов
в жидком состоянии и ограниченная - в
твердом. Если твердые растворы образуют
эвтектику,
то точка нонвариантного равновесия
Е лежит ниже t
плавления чистых компонентов,если же
перитектику,то
нонвариантная точка P
лежит между t
плавления чистых компонентов.Пример.
Cu-Ag,Pb-Sn;
Hg-Cd.Рассмотрим
первый случай.Система А-В с
ограничен.тв.р-рами- с эвтектикой.
В системе имеется 2 твердых раствора:
α - р-р компонентов В в А и β- р-р компонента
А в В.Max
растворимость В в А при t
эвтектики tЕ
отвечает точке G,
а при комнат.t
– точке M.
Линия GM
характеризует уменьшение растворимости
В в А по мере понижения t
от эвтектич-й до комнат-й.Линия
FN-снижение
растворимости А в В при понижении t
от tЕ
до
комнат-й.Кривые охлаждения 4
сплавов:1,2,3,4.На кривой охлаждения
сплава
1
имееются 2 перегиба,отвечающих началу
и концу выделения кристаллов тв.р-ра
α.На кривой охлаждения сплава
2
дополнительно наблюдается слабо
выраженный перегиб при t”2,отвечающий
частичному распаду в тв.состоянии
кристаллов α с выделением кристаллов
тв.р-ра β. Кривая охлаждения сплава
3:
при t3
из жид.фазы выделяются кристаллы
тв.р-ра α,жид.фаза при понижении от t3
до
tЕ
меняет свой состав по линии
t3Е,т.е.обогащается
компонентом В.Как только жид.фаза
достигнет состава Е,начинается
кристаллизация эвтектики-мех.смеси
2 тв.фаз-тв.р-ра α состава G
и тв.р-ра β состава F,на
кривой охлаждения наблюдается
площадка.Сплав
4
точно отвечает эвтектич.составу,кривая
охлаждения его подобна кривой охлаждения
чистого компонента. Система А-В с
ограничен.тв.р-рами- с перитектикой(т.Р).
Перитектическое превращение-результат
химического взаимодействия ранее
выпавшей тв.фазы с жид.фазой определенного
(перитектического) состава.В результате
этого взаимодействия образуется новая
тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4.
Кривые охлаждения 1 и 2 полностью похожи
на эвтектические.Кривая
охлаждения 3:в
интервале t
от t
до t3
идет охлаждение жид.фазы,и t
изменяется монотонно.При t3
из жид.фазы выпадают кристаллы тв.р-ра
α, на кривой охлаждения-перегиб.В
интервале t3-tP
жид.фаза меняет свой состав по линии
t3Е,а
тв.фаза по линии LG.Как
только жид.фаза достигнет состава
P(перитектического),получает
развитие перитектическая реакция.В
результате этой реакции исчезает
жид.фаза и ниже tP
наблюдается смесь 2 тв.фаз-тв.р-ров α
и β.На кривой охлаждения наблюдается
площадка,т.к. имеет место нонвариантное
превращение:С=К-Ф+1=2-3+1=0.Для сплава
4
при tP
в результате перитектической реакции
исчезает тв.р-ра α.В интервале tP
–t’4
из жид.фазы выпадают кристаллы тв.р-ра
β. От t’4
до t”4
происходит охлпждение тв.фазы β, а при
t”4
тв.р-р β частично распадается-с
выделением кристаллов тв.р-ра α.
57.
Диаграмма плавкости бинарной системы
с ограниченными твердыми растворами.
Диаграмма состояния системы
- диаграмма, указывающая, в каких
фазовых состояниях находится система
в зависимости от условий: температура,
давление и состав. Диаграммы
плавкости
– частный вид диаграмм состояния.Для
данных систем характерны полная
взаимная растворимость компонентов
в жидком состоянии и ограниченная - в
твердом. Если твердые растворы образуют
эвтектику,
то точка нонвариантного равновесия
Е лежит ниже t
плавления чистых компонентов,если же
перитектику,то
нонвариантная точка P
лежит между t
плавления чистых компонентов.Пример.
Cu-Ag,Pb-Sn;
Hg-Cd.Рассмотрим
первый случай.Система А-В с
ограничен.тв.р-рами- с эвтектикой.
В системе имеется 2 твердых раствора:
α - р-р компонентов В в А и β- р-р компонента
А в В.Max
растворимость В в А при t
эвтектики tЕ
отвечает точке G,
а при комнат.t
– точке M.
Линия GM
характеризует уменьшение растворимости
В в А по мере понижения t
от эвтектич-й до комнат-й.Линия
FN-снижение
растворимости А в В при понижении t
от tЕ
до
комнат-й.Кривые охлаждения 4
сплавов:1,2,3,4.На кривой охлаждения
сплава
1
имееются 2 перегиба,отвечающих началу
и концу выделения кристаллов тв.р-ра
α.На кривой охлаждения сплава
2
дополнительно наблюдается слабо
выраженный перегиб при t”2,отвечающий
частичному распаду в тв.состоянии
кристаллов α с выделением кристаллов
тв.р-ра β. Кривая охлаждения сплава
3:
при t3
из жид.фазы выделяются кристаллы
тв.р-ра α,жид.фаза при понижении от t3
до
tЕ
меняет свой состав по линии
t3Е,т.е.обогащается
компонентом В.Как только жид.фаза
достигнет состава Е,начинается
кристаллизация эвтектики-мех.смеси
2 тв.фаз-тв.р-ра α состава G
и тв.р-ра β состава F,на
кривой охлаждения наблюдается
площадка.Сплав
4
точно отвечает эвтектич.составу,кривая
охлаждения его подобна кривой охлаждения
чистого компонента. Система А-В с
ограничен.тв.р-рами- с перитектикой(т.Р).
Перитектическое превращение-результат
химического взаимодействия ранее
выпавшей тв.фазы с жид.фазой определенного
(перитектического) состава.В результате
этого взаимодействия образуется новая
тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4.
Кривые охлаждения 1 и 2 полностью похожи
на эвтектические.Кривая
охлаждения 3:в
интервале t
от t
до t3
идет охлаждение жид.фазы,и t
изменяется монотонно.При t3
из жид.фазы выпадают кристаллы тв.р-ра
α, на кривой охлаждения-перегиб.В
интервале t3-tP
жид.фаза меняет свой состав по линии
t3Е,а
тв.фаза по линии LG.Как
только жид.фаза достигнет состава
P(перитектического),получает
развитие перитектическая реакция.В
результате этой реакции исчезает
жид.фаза и ниже tP
наблюдается смесь 2 тв.фаз-тв.р-ров α
и β.На кривой охлаждения наблюдается
площадка,т.к. имеет место нонвариантное
превращение:С=К-Ф+1=2-3+1=0.Для сплава
4
при tP
в результате перитектической реакции
исчезает тв.р-ра α.В интервале tP
–t’4
из жид.фазы выпадают кристаллы тв.р-ра
β. От t’4
до t”4
происходит охлпждение тв.фазы β, а при
t”4
тв.р-р β частично распадается-с
выделением кристаллов тв.р-ра α. 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
C
в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.
1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
C
в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности. 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции.
1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные
вещества (ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции. С
ростом давления увеличивается
количество адсорбируемого вещества.Лэнгмюр
при выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало.
3. адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения
адсорбента адсорбатом:
С
ростом давления увеличивается
количество адсорбируемого вещества.Лэнгмюр
при выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало.
3. адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения
адсорбента адсорбатом: