
Бёккер_Хроматография [2009]
.pdf
190
 Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
таким образом, что полярные группы молекулы направлены преимущественно к полярной стационарной фазе и взаимодействуют с ней.
В качестве элюентов используют гексан, гептан, метиленхлорид, уксусный эфир или их смеси. Из этого сразу вытекает ограничение для анализируемых проб: они должны быть не только растворимы в этих неполярных элюентах, но и нахо& диться уже растворенными в этих неполярных растворителях. В неполярных ра& створителях разделяются преимущественно неполярные органические вещества. Полярные соединения, даже если они растворимы в элюентах, могут сильно вза& имодействовать с поверхностью силикагеля, что приводит к пикам плохой фор& мы или элюирование вообще не происходит. Поэтому нормальнофазовая хрома& тография применяется для умереннополярных проб, растворимых в органичес& ких растворителях.
Типичным недостатком адсорбционной хроматографии является сильное вли& яние следов воды в элюентах. Вода адсорбируется на поверхности силикагеля и дезактивирует силанольные группы, вследствие чего удерживание уменьшается. Поэтому используемые колонки нужно часто регенерировать (сушить).
4.5.2. Химически привитые полярные фазы
Под понятием «полярные или гидрофильные привитые стационарной фазы» по& нимают, в общем случае, силикагель, поверхность которого модифицирована по& лярными функциональными группами. Так же, как немодифицированный сили& кагель, эти сорбенты могут использоваться в нормальнофазовом режиме, причем они показывают обычно разную селективность. Они менее чувствительны к сле& дам воды в подвижной фазе.
Это свойство делает их интересной альтернативой силикагелю. Они могут успешно применяться в адсорбционной хроматографии, в обращеннофазовой хроматографии и в ионообменной хроматографии [4.8]. В качестве функциональных групп для по& лярные привитых фаз предлагаются группы, представленные в табл. 4.1.
Таблица 4.1. Различные полярные привитые фазы
Обозначение |
Функциональные группы |
Применение |
NH2 |
–CH2–CH2–CH2–NH2 |
Адсорбционная хроматография, ионо- |
|
|
обменная хроматография, обращенно- |
|
|
фазовая хроматография |
|
|
|
CN |
–CH2–CH2–CH2–CN |
Адсорбционная хроматография, обращенно- |
|
|
фазовая хроматография |
ÄÈÎË |
–CH2–CH2–CH2–O–CHOH–CH2–OH |
Адсорбционная хроматография, |
|
|
эксклюзионная хроматография |
Гидрофильные привитые стационарные фазы предлагают интересную альтер& нативу для решения проблем ВЭЖХ. При использовании подходящих элюентов на этих модифицированных сорбентах могут действовать различные механизмы удерживания и, вследствие этого, проявляться особые эффекты разделения. Преж& де всего, эти носители могут успешно применяться для разделения заряженных и среднеполярных соединений.

4.5. Колонки для ВЭЖХ 191
4.5.2.1. Диольная фаза
Наряду с широко распространенным применением в гельпроникающей хроматогра& фии диольная фаза, прежде всего, используется при решении проблем разделения в адсорбционной хроматографии. Благодаря модификации эта фаза ведет себя подоб& но немодифицированному силикагелю, однако с отчетливо сниженной активнос& тью. Диольные группы образуют в основном активные центры для адсорбционной хроматографии. Основной тип взаимодействий с хроматографируемыми соединени& ями – это образование водородных связей и индуцированные диполь&дипольные вза& имодействия. Удерживание молекул пробы может варьироваться благодаря направ& ленному изменению полярности органической подвижной фазы. Подобно немоди& фицированному силикагелю величины k′ уменьшаются с ростом полярности элюен& тов. Это может быть объяснено тем, что с ростом содержания полярного компонента в подвижной фазе активные полярные молекулы растворителя занимают все больше активных мест на поверхности сорбента, предназначенных для хроматографии, и, тем самым, уменьшают взаимодействие с ними молекул пробы.
Если рассматривают последовательность удерживания сорбатов на диольной фазе в адсорбционной хроматографии, то всегда вещество с наименьшей поляр& ностью удерживается слабее всего, а с наивысшей полярностью – сильнее всего.
4.5.2.2.NH2 фаза
Уэтой стационарной фазы γ&аминопропильные группы ковалентно привязаны к поверхности силикагеля. Однако колонки с аминофазой на основе силикагеля лишь ограниченно устойчивы, так как, вероятно, происходит гидролиз частиц. Это проявляется в непрерывно уменьшающемся времени удерживания сорбатов в рутинной работе. В качестве носителей лучше подходят ПВА сополимеры, ко& торые очень устойчивы механически и химически. Благодаря химической моди& фикации эта стационарная фаза может взаимодействовать с молекулами пробы самыми разными способами. В нормальнофазовой хроматографии с гексаном, дихлорметаном и изопропанолом в качестве подвижной фазы разделяются по& лярные соединения, как, например, сложные эфиры, замещенные анилины и хло& рированные пестициды. Как на слабом анионообменнике, на аминофазе могут разделяться анионы и органические кислоты, для чего применяется обычно аце& татный или фосфатный буфер с добавлением органических растворителей.
Это означает, что при соответствующем выборе растворителей удерживание разделяемых соединений вызывается различными механизмами. Если применя& ются чисто органические элюенты, существует возможность адсорбционно&хро&
матографического разделения. В этом случае NH2 группа действует как незаря& женный, полярный, слабоосновный адсорбционный центр.
Намного чаще аминофазы используются в сочетании с водными элюентами. Примером тому являются разделение моно& и олигосахаридов с водно&ацетонит& рильными системами. Однако при использовании водных растворителей нужно учитывать, что аминогруппы существуют в протонированной форме. Это ведет к тому, что аминофаза действует в таких хроматографических условиях, как слабо& основный ионообменный сорбент. Поэтому ионообменная хроматография явля& ется основной областью применения аминофаз.

192
 Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Сорбаты удерживаются в этом варианте хроматографии из&за различия в элек& тростатических взаимодействиях и очень во многих случаях в соответствии с ве& личиной их заряда. На NH2 фазе, как в обычной ионообменной хроматографии, можно очень просто целенаправленно изменять удерживание компонентов про& бы, варьируя содержание соли в подвижной фазе. С ростом содержания соли в элюентах удерживание веществ пробы уменьшается. Это объясняется тем, что добавленные в элюент ионы конкурируют с ионами пробы за ионогенные группы стационарной фазы.
С ростом концентрации соли в элюенте функциональные группы ионообмен& ного сорбента все в большей стпени экранируются и в меньшей мере взаимодей& ствовуют с ионами пробы. Незаряженные соединения, в общем случае, удержи& ваются на аминофазе довольно слабо. Содержание соли в элюентах мало или вов& се не влияет на их удерживание.
4.5.2.3. CN фаза
Цианофаза представляет особенно интересную стационарную фазу в ВЭЖХ в рам& ках гидрофильно модифицированных сорбентов. Среднеполярная стационарная фаза образуется химической прививкой γ&цианопропильных групп на поверхности силикагеля. В соответствии с выбором подвижной фазы этот сорбент может успешно применяться как для нормальнофазовой, так и для обращеннофазовой хроматог& рафии. В нормальнофазовой хроматографии с относительно неполярными раство& рителями CN фаза разделяет многие соединения, которые могут разделяться также и на немодифицированном силикагеле. Преимущество этого сорбента – быстрое установление равновесия при градиентном элюировании.
При использовании неполярных элюентов (например, изооктана) сильнее всего удерживаются самые полярные вещества. С увеличением полярного харак& тера элюента при добавлении диоксана соединения удерживаются все меньше до полного прекращения удерживания. Только добавлением воды к растворителю (дальнейшее повышение полярности) разделение становится снова возможным. Разумеется, теперь ряд последовательности элюции обратится, и самые поляр& ные соединения удерживаются слабее всего. Повышение содержания воды в под& вижной фазе вызывает дальнейший рост величины k′. Это – известный феномен в обращеннофазовой хроматографии. CN фаза особенно подходит для разделе& ния среднеполярных соединений.
4.5.3. Обращеннофазовая хроматография
Как видно уже из названия, здесь работают с противоположным соотношением полярностей, т.е. стационарная фаза – неполярная, а подвижная фаза – полярная. В этом случае силикагель модифицируется химически. Обращенные фазы получают, если поверхность силикагеля покрывают гидрофобными функциональными груп& пами. Стабильнее всего соединения, в которых функциональная группа связана че& рез ковалентную связь Si–C, которая химически стабильна в области pH от 1 до 9. Наибольшое количество разделений в аналитике проводится в ВЭЖХ с модифици& рованными стационарными фазами. В зависимости от вида функциональной груп& пы для обозначения колонок используют сокращения, указанные в табл. 4.2.

4.5. Колонки для ВЭЖХ 193
Таблица 4.2. Доступные материалы для обращенной фазы
Модификация |
Функциональная группа |
Ñ2 |
Ýòèë |
Ñ4 |
Бутил |
Ñ8 |
Октил |
Ñ18 |
Октадецил |
Ñ6Í5 |
Фенил |
В качестве подвижной фазы используется вода, полярные органические ра& створители (метанол, ацетонитрил) или их смеси. Этим методом можно разде& лять широкий круг соединений, так как многие вещества растворимы в воде или подобных растворителях. Развитие техники обращеннофазовой хроматографии (ОФХ) с химически связанными обращенными фазами позволило значительно расширить область применения ВЭЖХ. Более 70% анализов методом ВЭЖХ про& водятся сегодня на химически связанных фазах.
Принцип ОФХ представлен на рис. 4.16. Химически модифицированный ал& кильными группами силикагель образует неполярную стационарную фазу, подвиж& ная фаза – полярная. Неполярные молекулы или соответственно неполярные груп& пы в молекулах предпочтительнее удерживаются на неполярной стационарной фазе.
Вода часто обозначается как самый сильный элюент в хроматографии. Однако это справедливо только для адсорбционной хроматографии (нормальнофазовая): вода может вступать в очень сильное взаимодействие с активными центрами сили& кагеля и оксида алюминия, так что молекулы пробы больше не могут адсорбиро&
Полярная |
Неполярная |
стационарная фаза |
подвижная фаза |
Неполярное Поляр>ное
Проба |
Элюент |
Колонка
Рис. 4.16. Обращеннофазовая хроматография

194
 Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
ваться и быстро элюируются. В ОФХ все с точностью до наоборот: вода не может смачивать аполярные (гидрофобные) алкильные группы и не вступает с ними во взаимодействие. Поэтому это самая слабая из всех мобильных фаз и медленнее все& го элюирует пробу. Чем больше содержание воды в элюенте, тем дольше время удер& жания. Поэтому разделение на ОФ можно легко оптимизировать, варьируя состав подвижной фазы: с возрастающим содержанием органического растворителя по& лярность подвижной фазы и, вместе с тем, время удерживания уменьшается.
ОФ матрицы, C2, C4, C8, C18 и фенил, отличаются временем удерживания ве& ществ. С ростом длины алкильных групп поверхность становится неполярной. Как показано на рис. 4.17, время удерживания в тех же самых хроматографических ус& ловиях (подвижная фаза, скорость потока) для C18 (ОФ&18, англ. RP&18) для мно& гих веществ примерно вдвое больше, чем для C8 (ОФ&8, англ. RP&8). Самое боль& шое время удерживания получают при использовании сорбента C18 как самой не& полярной стационарной фазы и воды как самой полярной подвижной фазы.
Механизмом разделения, который лежит в основе ОФХ, – это притяжение за счет Ван&дер&Ваальсовых сил между углеводородными фрагментами молекул про& бы и привитыми алкильными группами сорбента. Чем больше углеводородная часть в молекулах, тем сильней они притягиваются. Это различие в химической структу& ре молекул приводит к более сильной или более слабой их адсорбции на стацио& нарной фазе и, вместе с тем, к разделению. Вещества удерживаются ОФ поверхно& стью тем сильней, чем меньше они растворимы в воде, т.е. чем более они неполяр& ны. Полярные вещества элюируются раньше, чем неполярные.
Время, мин
Рис. 4.17. Влияние типа ОФ сорбента на время удерживания
4.5. Колонки для ВЭЖХ 195
Хотя привитые на поверхность силикагеля фазы представляют собой моно& мерный органический слой, они отличаются высокой поверхностной концентра& цией функциональных групп. Она составляет от 3 до 4 функциональных групп на 100 A2. Так как привитой фазой невозможно закрыть абсолютно все силанольные группы, то различные производители пытаются осуществлять в дополнительной стадии модификации так называемое дозакрытие (англ. «endcapping»), чтобы мо& дифицировать оставшиеся после первой обработки силанольные группы. Цель состоит в уменьшении активных центров на поверхности путем перевода актив& ных силанольных групп в индифферентные группы. Пожалуй, наиболее широко используемым реагентом для дозакрытия является триметилхлорсилан.
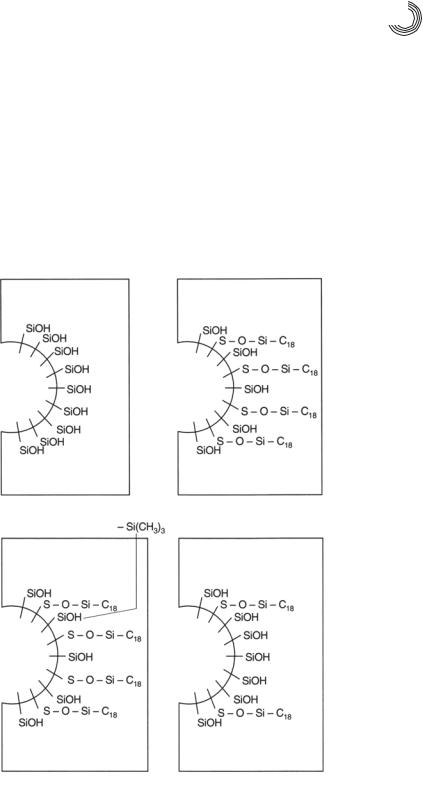
Различные стадии модификации силикагеля представлены на рис. 4.18. Часть а) показывает поверхность немодифицированного силикагеля. Поверхностные си&
a) |
б) |
в) |
г) |
Рис. 4.18. Типы модификации силикагеля

196
 Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
ланольные группы «активны» и вступают во взаимодействие с ионными и поляр& ными соединениями. Часть б) показывает модифицированный, привитой сили& кагель. Однако преобразование поверхностей никогда не может быть полным. На поверхности остается много активных силанольных групп. Часть в) показывает процесс дозакрытия. Маленькие нейтральные группы прививаются к большин& ству из оставшихся силанольных групп, чтобы уменьшить активность поверхнос& ти силикагеля. Часть г) показывает процесс «старения» колонок с обращенной фазой. В принципе, силикагельная основа, к которой привиты все фазы, неста& бильна. Силикагель растворяется при повышенных величинах pH (до кремние& вой кислоты) и подвергается разрушению также при нейтральных pH в водной среде. Из&за медленного, но непрерывного растворения кремниевой подложки свободные силанольные группы снова становятся все более и более доступными. Активность поверхности снова повышается. Это выражается в уменьшении вре& мени удерживания до тех пор, пока колонку, наконец, нужно будет заменить.
Поэтому в последнее время как носитель для химически привязанных фаз стал использоваться сополимер поливинилового спирта. Все же первоначально разде& ляющая способность колонок на полимерной основе была значительно хуже, чем разделительная способность колонок на основе силикагеля. Но дальнейшее раз& витие принесло свои поды. На сферических частицах сополимера поливинило& вого спирта была достигнута высокая плотность ковалентно привитых углеводо& родных цепей. Сегодня хроматографическое поведение этих фаз практически срав& нимо с обычными ОФ колонками. Гидрофильные частицы не имеют проблем со свободными силанольными группами и микропорами. Ковалентная связь между полимерными частицами и алкильными группами делает возможным использо& вание сильнощелочных буферов до величины pH примерно 13. Напротив, приви& тые фазы на основе силикагеля становятся нестабильными выше pH 7.
Колонки с обращенной фазой лучше подходят для решения широкого круга задач, чем колонки какого%либо другого типа. Для анализа неизвестного вещества сначала проводят пробное разделение на обращеннофазовой колонке.
4.5.4. Эксклюзионная хроматография
Эксклюзионная хроматография (англ.: Size exclusion chromatography, SEC) – это метод жидкостной хроматографии, который позволяет анализ молекул в области олигомеров и полимеров. При использовании органических элюентов метод ста& новится также гельфильтрационной хроматографией (ГФХ, англ.: GFC), а при вод& ных элюентах – упомянутой гельпроникающей хроматографией (англ. GPC). При этом большие молекулы пробы разделяются согласно эффективному размеру в ра& створе. Основное преимущество эксклюзионной хроматографии состоит в возмож& ности на основании предсказываемых времен удержания определять распределе& ние молекулярных масс в области примерно от 102 до 107 Da. Можно разделять сме& си компонентов, отличие молекулярных масс которых составляет около 10%.
Большинство полимеров представляет собой смесь из молекул с различными молекулярными массами и молекулярными размерами. Эта смесь характеризует&

4.5. Колонки для ВЭЖХ 197
ся молекулярно&массовым распределением полимера (ММР). ММР – это важная характеристика для предсказания физического и химического поведения поли& меров, так как ММР влияет на текучесть, активность, твердость и различные дру& гие механические свойства полимера. Анализ ММР применяется при контроле качества как исходных материалов, так и готовых продуктов.
Эксклюзионная хроматография разделяет молекулы пробы по их гидродинами& ческому объему или по эффективной величине молекулы в растворе. Она принципи& ально отличается от всех других методов хроматографии. Здесь разделение обуслов& лено не какими&то взаимодействиями сорбата со стационарной и подвижной фаза& ми, а является следствием простого процесса сортировки молекул по размерам. Для этого хроматографическая колонка заполняется частицами по возможности одина& кового зернения. Самым важным требованием для разделения молекул по размерам является то, что частицы должны быть очень пористы и поры должны иметь опреде& ленный размер. Эксклюзионная хроматография – это недеструктивный метод без какого&либо взаимодействмя между сорбатом и сорбентом, в котором разделение до& стигается за счет того, что молекулы пробы принудительно двигаются через твердый, высокопористый материал, который помещен в колонку из нержавеющей стали.
На рис. 4.19 представлено наглядное пояснение для пор конической формы. Маленькие молекулы пробы разделяемого полимера величины C проникают так& же в более тесные поры и вследствие этого дольше удерживаются до тех пор, пока они снова не диффундируют в подвижную фазу. Самые большие молекулы A не могут проникнуть в поры и непосредственно транспортируются подвижной фа& зой и, таким образом, покидают хроматографическую колонку первыми. Моле&
Материал Подвижная заполнения колонки
фаза
Поры
Время удерживания
Рис. 4.19. Механизм разделения в эксклюзионной хроматографии

198
 Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
Глава 4. Высокоэффективная жидкостная (колоночная) хроматография
кулы средней величины B могут только наполовину проникать в поры. Так как сорбционные взаимодействия со стационарной фазой в гельпроникающей хро& матографии при правильном выборе мобильной фазы исключаются, то компо& ненты элюируются в последовательности A, B и C, т.е. большие молекулы будут выходить вначале, а самые маленькие – в самом конце.
Чтобы достичь оптимального разделения олигомеров или, соответственно, полимеров, предлагаются сорбенты с различными размерами пор. Их различают либо по величине пор, либо по границе исключения. Граница исключения соот& ветствует молекулярному весу фракции полистирола или декстрана, который еще может проникать в гель и является при этом мерой пористости геля. Из вышеска& занного можно заключить, что:
•все введенные молекулы будут элюированы;
•хроматографирование закончено, когда из колонки элюируется неудержи& ваемый компонент (мертвое время). Таким образом, заранее известно, как долго будет проходить разделение;
•время элюирования зависит только от размера молекулы, но вместе с тем пусть даже косвенно – от ее молекулярной массы. Гельфильтрацию можно использовать для определения молекулярной массы;
•так как разделение заканчивается уже после прохождения небольшого объе& ма, пиковая емкость (т.е. количество пиков, которые могут быть разделены с определенным разрешением) ограничена;
•чтобы молекулы двух разных масс можно было разделить друг от друга, их молярные массы должны отличаться минимум на 10%;
•с ростом времени удерживания не происходит уширения пиков;
•поскольку в системе отсутствуют какие&либо равновесные взаимодействия, то колонку едва ли можно перегрузить. Можно разделять относительно боль& шие пробы.
На рис. 4.20 наглядно продемонстрирован механизм разделения.
Рис. 4.20. Схема трех этапов гельпроникающей хроматографии

4.5. Колонки для ВЭЖХ 199
У молекулы пробы, которые слишком велики, чтобы проникать в поры, есть только объем между отдельными шариками: они исключаются и должны искать себе путь между шариками в колонке. Так как шарики не входят с ними ни в какое взаимодействие, эти молекулы проходят колонку по наиболее короткому пути и элюируются из колонки вместе с подвижной фазой.
Напротив, если в пробе имеются молекулы, которые, благодаря своим малым размерам, могут проникать в поры, то в их распоряжении весь объем подвижной фазы. Так как подвижная фаза в порах неподвижна, то молекулы двигаются в по& рах только за счет диффузии и будут задерживаться по сравнению с исключенны& ми молекулами. Они последними появятся в детекторе, а именно с задержкой, точно равной мертвому времени системы, которое известно из других методов колоночной хроматографии. Сам растворитель не вступает во взаимодействие со стационарной фазой, но тем не менее проходит по всем порам. Поэтому в любом другом методе колоночной хроматографии молекулы растворителя первыми ока& жутся в детекторе. В эксклюзионной хроматографии такие маленькие молекулы как молекулы растворителя будут выходить последними. Они полностью прони& кают в стационарную фазу. Называют это «полным проникновением» (англ. totale penetration). Каждый компонент будет выходить из колонки самое позднее через мертвое время.
Молекулы средней величины не могут проникать в самые узкие поры. Они только частично проникают в стационарную фазу. Занимаемый ими объем нахо& дится между объемом «полного проникновения» и мертвым объемом. Они элюи& руются после «исключенных» молекул, но раньше «мертвого времени».
Если хотят знать, какому объему элюции следует отнести молекулы опреде& ленной величины, то колонку калибруют по тестовой смеси стандартных веществ с точно известными молекулярными массами. В результате получают примерно линейное соотношение между логарифмом молекулярной массы и объемом элю& ирования. Как стандарты при разделении полимеров, растворимых в органичес& ких растворителях, применяют преимущественно полистиролы, а для полимеров растворимых в воде – декстраны, которые имеют различные, но точно известные молекулярные массы. Рис. 4.21 показывает хроматограмму олигомеров стирола с n = от 1 до 14.
Крайний пик справа пренадлежит мономеру стирола. Это – самая маленькая молекула (наряду с молекулами подвижной фазы) и она будет элюироваться пос& ледней. Соответствующий объем элюирования – это мертвый объем V0, первый маленький пик слева принадлежит исключенным молекулам. Соответствующий объем – это межгранульный объем Vz, (жидкость, которая находится между от& дельными шариками стационарной фазы). Между Vz и V0 элюируются молекулы со степенью полимеризации n от 14 до 1. Объем V0–Vz соответствует объему пор стационарной фазы Vp (жидкость, которая находится в порах). Vp – это единствен& ный полезный для разделения объем и поэтому он должен быть как можно боль& ше, так как разрешение пиков зависит от Vp.
Если теперь хотят охарактеризовать неизвестную фракцию или определить молекулярно&массовое распределение полимера, то сравнивают хроматограмму пробы с калибровочной кривой. Так как объем элюирования соответствует раз&
