
- •Введение
- •1. Химическая термодинамика предмет и задачи термодинамики
- •1.1 Основные понятия и определения химической
- •1.2 Первый закон термодинамики
- •1.3 Применение первого закона термодинамики к процессам в любых системах
- •1.6 Теплоемкость. Связь теплоемкости с
- •1.7 Зависимость теплового эффекта oт температуры.
- •1.8 Второй закон термодинамики
- •1.9 Энтропия
- •1.10 Второй закон термодинамики для обратимых и
- •1.12 Постулат планка.Вычисление абсолютной энтропии
- •1.14 Энергия гельмгольца (изохорно-изотермический
- •1.15 Энергия гиббса (изобарно-изотермический
- •1.16 Уравнение гиббса-гельмгольца
- •1.17 Характеристические функции
- •1.18 Химический потенциал.Летучесть
- •1.20 Уравнение изотермы реакции
- •1.21 Зависимость константы равновесия от температуры
- •1.23 Тепловая теорема нернста
- •1.24 Расчет химического равновесия с помощью
- •2. Фазовые равновесия
- •2.1 Общие понятия
- •2.2 Условия фазового равновесия
- •2.3 Правило фаз гиббса
- •2.4 Уравнение клаузиуса-клапейрона
- •2.5 Однокомпонентная система воды
- •2.6 Диаграммы состояния двухкомпонентных
- •2.6.1 Система с неограниченной растворимостью
- •2.6.3 Система с ограниченной растворимостью
- •2.7 Трехкомпонентные системы
- •3. Растворы
- •3.1 Характеристика растворов
- •3.2 Закон рауля
- •3.5 Жидкие бинарные системы. Идеальные растворы
- •3.6 Растворы с положительными и отрицательными
- •3.7 Состав паровой фазы над растворами. Законы
- •3.7.1 Диаграммы состав – давление пара (температура
- •3.7.2 Перегонка. Ректификация
- •Ректификация
- •3.8 Термодинамика концентрированных
- •3.10 Растворимость твердых тел в жидкостях
- •3.12Распределение растворенного вещества между
- •4.2 Математическое описание волнового движения
- •4.3 Уравнение шредингера
- •4.4 Решение уравнения шредингера
- •4.7 Распространение волнового уравнения на
- •4.8 Атомные термы
- •5.1 Ионная связь.Энергия кристаллической решетки
- •5.2 Ковалентная связь
- •5.4 Расчет молекулярного иона водорода
- •5.7 Квантовохимические представления о координационных соединениях
- •5.9 Водородная связь
- •6.1 Дипольный момент молекул
- •Содержание
- •1.Химическая термодинамика
- •2.Фазовые равновесия
- •3.Растворы
- •4.Строение атомов
- •5.Химическая связь
- •6.Электрические и магнитные свойства молекул
4.2 Математическое описание волнового движения
Отвлечемся временно от описания строения атомов, чтобы познакомиться с математическим описанием волнового движения. Рассмотрим волну, изображенную на рисунке, которая с
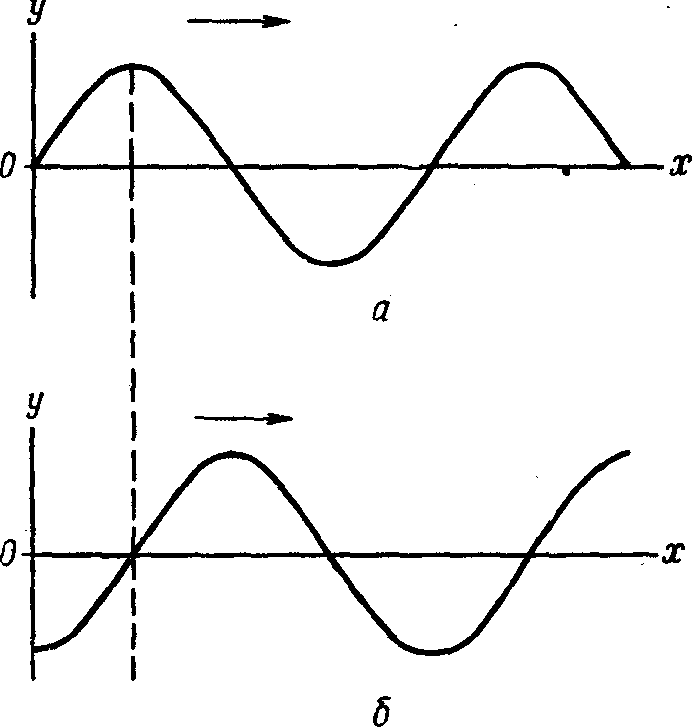
течением времени передвигается вдоль оси х в направлении, указанном стрелкой. Это волновое движение можно описать количественно с помощью дифференциального уравнения
![]() = (
= (![]() )
(
)
(![]() ),
),
где А — амплитуда, т. е. высота волны, измеряемая по оси у при данном расстоянии х; с — скорость, с которой передвигается волна, a — время. Решением этого дифференциального уравнения является функция
A==аsin2(х/—).
где — длина волны, —ee частота и а—постоянная. Из уравнения можно найти амплитуду А во время t в положении х.
Другой тип волнового движения — стоячая волна — возникает при колебаниях струны с закрепленными концами. Стоячей волне отвечает стационарная картина с фиксированным профилем (вместо перемещающегося вдоль оси х, как в случае волны, изображенной ранее). Эмпирическим .путем
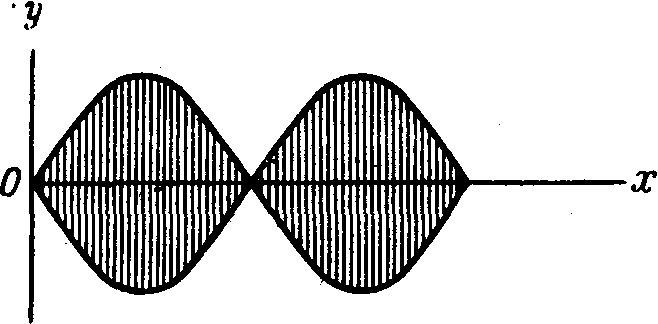
было найдено, что такая модель, обобщенная на случай трехмерной волны, лучше описывает поведение электрона, связанного с ядром. Дифференциальное уравнение, описывающее такую одномерную стоячую волну, имеет следующее решение:
A==2asin(2х/)cos2,
или более просто
A=f(x)cos2,
где f(x)—сокращенная запись для 2a sin(2x/)—функция только координаты х.
Вторая производная функция по времени, будучи подставленной в уравнение , позволяет исключить величину .
![]() = -2a
sin(2
= -2a
sin(2![]() )
sin2t2
)
sin2t2
![]() = -2a
sin(2
)
cos2t422
= -2a
sin(2
)
cos2t422
= -A422
=
![]()
= -A![]() = c2
= c2![]()
Получающееся уравнение для стоячей волны может быть обобщено для описания трехмерной волны:
![]() +
+
![]() +
+
![]() + 42/2
== 0,
+ 42/2
== 0,
где —трехмерный аналог величины А ). Введя сокращенное обозначение,
![]() +
+
![]() +
+
![]() =
2,
=
2,
получаем
2+42/2=0. )
Уравнения являются дифференциальными уравнениями, описывающими стационарную трехмерную волну, и не содержат переменной t. Целью исключения этой переменной было получение уравнения, решения которого не зависят от времени.
4.3 Уравнение шредингера
Шрёдингер выбрал математическое описание стоячей волны в качестве модели для строения атома. Он включил в выражение для стоячей волны предположение де Бройля =h/m и получил
2 + (42m22/h2) == 0.
Комбинируя уравнения с уравнением , связывающее полную энергию Е, потенциальную энергию V и кинетическую энергию m2/2 .
Е = V + m2/2 или 2 = 2 (Е — V)/m,
можно получить уравнение Шрёдингера в его обычной форме
2 +(82m/h2)(E-V)=0
Следует помнить, что уравнение Шредингера не выводится из более общих законов, а является следствием, во-первых, эмпирического выбора уравнения для стоячей волны в качестве модели для описания поведения -электрона в атоме и, во-вторых, включения в последнее гипотезы де Бройля. Обоснованием такого «вывода» является тот факт, что решение уравнения приводит к значениям энергии Е, точно соответствующим найденным экспериментально из атомных спектров
Остановимся на смысле символа в уравнении Шредингера. Поскольку является трехмерным аналогом А (амплитуды плоской волны), рассматривается как амплитудная функция. Самой функции нельзя приписать физический смысл, но такой смысл имеет величина *, которая, как можно показать, пропорциональна вероятности нахождения электрона в данном положении (* — это функция, комплексно сопряженная с ). Величина *d передает вероятность нахождения электрона в элементе объема d. Если является действительной функцией, * переходит в 2.
