
- •Лабораторные работы введение Величины
- •Измерения
- •Правила вывода единиц из формул:
- •Погрешности
- •Порядок вычисления погрешностей результатов измерения физической величины
- •Определение цены деления многопредельного прибора.
- •Лабораторная работа №1. Проверка объединенного газового закона. (уравнение газового состояния).
- •1. Теоретическое введение.
- •2. Ход работы.
- •Определение удельной теплоты парообразования.
- •I. Теоретическое введение.
- •2. Ход работы.
- •I. Теоретическое введение.
- •2. Ход работы.
- •Контрольные вопросы первого и второго уровня.
- •Определение коэффициента поверхностного натяжения методом капель.
- •1.Теоретическое введение.
- •Определение электроемкости конденсатора.
- •1. Теоретическое введение.
- •Определение удельного сопротивления проводника.
- •1.Теоретическое введение.
- •2. Ход работы.
- •Лабораторная работа № 7. Определение внутреннего сопротивления и эдс источника электрического тока.
- •1.Теоретическое введение.
- •2. Ход работы.
- •7.Измерительные приборы вольтметр и амперметр15.
- •Изучение зависимости сопротивления металлов от температуры
- •1. Теоретическое введение.
- •2. Ход работы.
- •Исследование зависимости мощности, потребляемой лампой накаливания от напряжения на ее зажимах.
- •1. Теоретическое введение.
- •2. Ход работы.
- •Контрольные вопросы
- •Определение электрохимического эквивалента меди.
- •1.Теоретическое введение.
- •2. Ход работы.
- •Изучение электрических свойств полупроводникового диода.
- •1. Теоретическое введение.
- •2. Ход работы.
- •Изучение устройства и работы трансформатора.
- •1. Теоретическое введение.
- •2. Ход работы.
- •Исследование цепи переменного тока, содержащей катушку индуктивности и конденсатор. Повышение коэффициента мощности.
- •1 .Теоретическое введение.
- •2.Ход работы.
- •Определение показателя преломления стекла.
- •1. Теоретическое введение.
- •2. Ход работы.
- •«Определение длины световой волны с помощью дифракционной решетки».
- •Теоретическое введение.
- •2.Ход работы:
- •Проверка законов освещенности.
- •Теоретическое введение.
- •Ход работы.
- •«Исследование линейчатых спектров испускания».35
- •1. Теоретическое введение и описание установки.
- •Лабораторная работа №18. Определение ускорения свободного падения с помощью математического маятника.
- •1. Теоретическое введение.
- •При малых углах отклонения математического маятника колебания будут
- •2. Ход работы.
- •Определение фокусного расстояния линзы.
- •1. Теоретическое введение.
- •2. Ход работы.
- •Изучение фотоэффекта.
- •1. Теоретическое введение.
- •2. Ход работы.
- •Определение показателя преломления с помощью дисперсионного рефрактометра.3
- •1. Теоретическое введение.
- •2 Среда
- •2. Ход работы.
Определение цены деления многопредельного прибора.
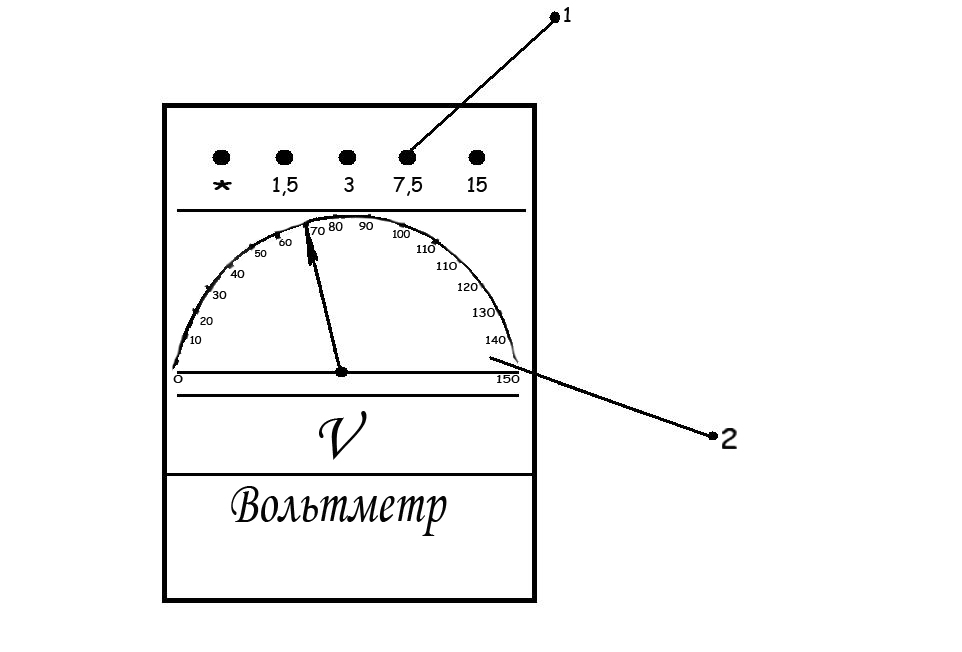
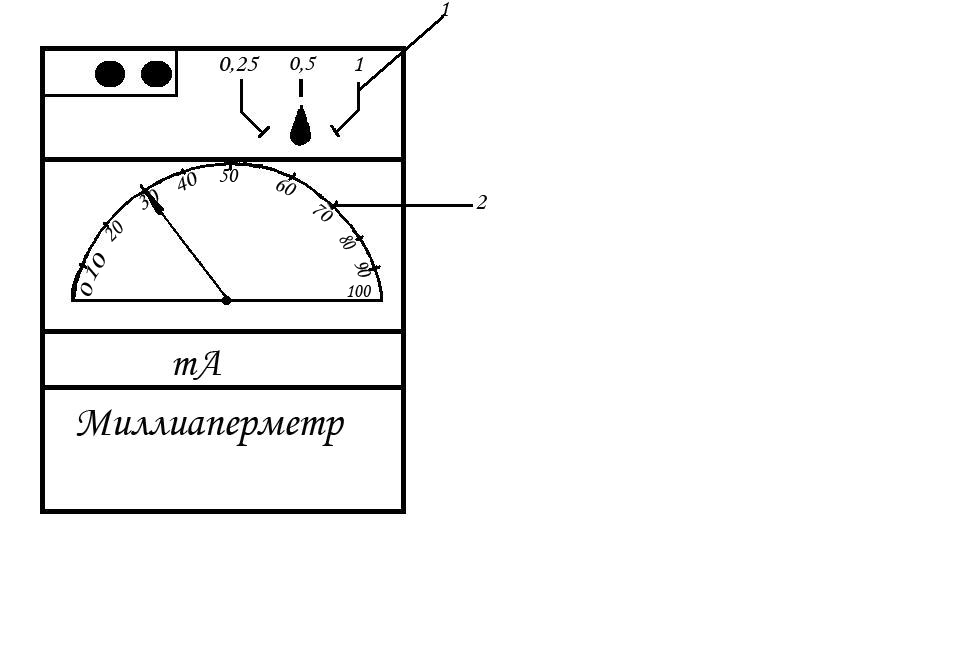
рис. 1а рис. 1б
а – цена одного деления.
а = предел измерения
число делений шкалы
Пример:
По рис. 1 а аВ = 7,5 В / 150 дел = 0,05 В/дел
U = 0,05 65 = 3,25 В.
По рис. 1 б амА = 0,5 А / 100 дел = 0,005 А/дел
I = 0,005 30 = 0,15 А.
Лабораторная работа №1. Проверка объединенного газового закона. (уравнение газового состояния).
Приборы и материалы используемые в работе:
Прибор для проверки газового состояния (укороченный манометр).
Химический стакан.
Термометр.
Барометр-анероид.
Электроплитка для нагревания воды.
Цель работы:
Целью работы является опытная проверка справедливости объединённого газового закона (1).
![]() ,
,
![]() ,
,
![]()
![]() ,
,
![]() ,
,
![]()
![]() ,
,
![]() ,
,
![]()
Если затем вычислить по формулам
![]()
![]()
![]()
значение
трёх величин:
![]() ,
,
![]() ,
,
![]() ,
то согласно уравнению (1) должно иметь
место равенство:
,
то согласно уравнению (1) должно иметь
место равенство:
![]()
1. Теоретическое введение.
Состояние данной массы газа т характеризуется тремя макроскопическими параметрами, которые ещё называются термодинамическими параметрами:
давление р,
объём V,
абсолютная температура Т.
Если параметры определённой массы газа р, V и Т остаются постоянными в течение определённого времени, то газ будет эта время находится в равновесном состоянии.
Если индексом 1 обозначить параметры, характеризующие массу газа в одном состоянии: , , , а индексом 2 - параметры, в другом состоянии , , , то в случае идеального газа параметры этих двух состояний связаны между собой следующим уравнением
![]() (1)
(1)
Это объединённый газовый закон или уравнение газовых состояний данной массы газа, который формируется так:
При постоянной массе газа произведение объёма на давление, делённое на абсолютную температуру газа, есть величина одинаковая для всех состояний этой массы газа.
2. Ход работы.
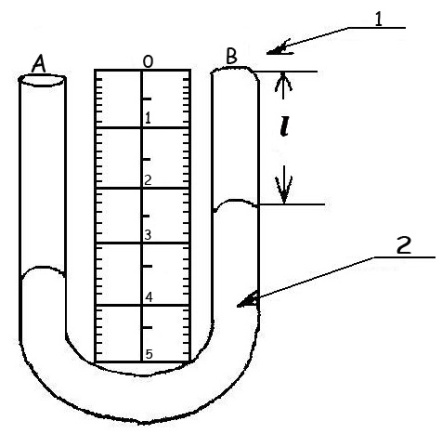
Рис. 1
Для проверки объединённого газового закона используется прибор (см. рис.1), состоящий из укороченного манометра 1, заполненного ртутью. Колено А манометра открытое, колено В - закрытое. В колене В находится столб воздуха высотой l. Манометр укреплён на металлической пластинке 2, имеющей шкалу с миллиметровыми делениями.
Исследуемая масса воздуха, находящаяся в закрытом колене В, остаётся в течение всех опытов неизменной, что требуется для проверки объединённого газового закона.
Реализация трёх различных состояний этой массы газа и измерение его параметров в этих состояниях производится следующим образом.
1. ПЕРВОЕ СОСТОЯНИЕ. Манометр помещают в химический стакан, туда же помещают термометр. Далее следует определить по шкале длину воздушного столба в закрытом колене.
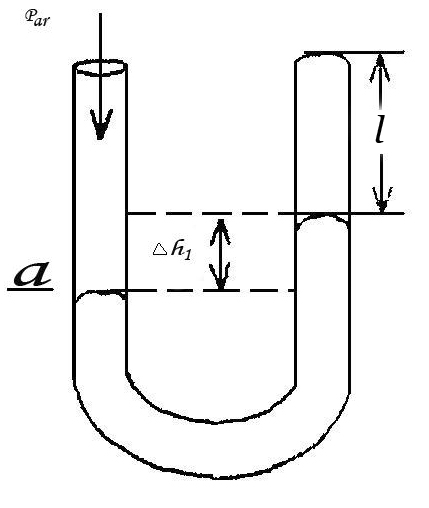
Рис.2
Если сечение трубки манометра принять за 1 условную единицу, то объём исследуемой массы газа в 1-м состоянии равен:
![]() (2)
(2)
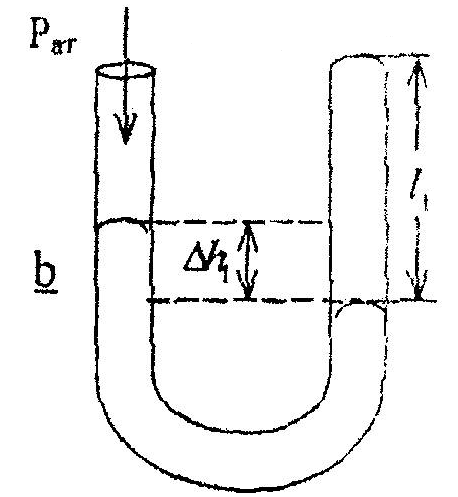
Рис.3
Определить
разность уровней ртути в коленах А и В
равную
![]() и вычислить давление воздуха в
закрытом колене в первом состоянии по
формуле
и вычислить давление воздуха в
закрытом колене в первом состоянии по
формуле
![]() ,(3)
,(3)
где
![]() - атмосферное давление, определяемое
барометром.
- атмосферное давление, определяемое
барометром.
Знак "-" берётся в том случае, когда уровень ртути в открытом колене ниже, чем в закрытом (случай (а) на рис.2).
Знак "+" берётся в том случае, когда уровень ртути в открытом колене выше, чем в закрытом (случай (в) на рис. 3)
Измерить температуру воздуха в стакане термометром и найти абсолютную температуру воздуха в закрытом колене:
![]() (4)
(4)
По формуле вычислить постоянную величину, характеризующую данную массу воздуха в 1-ом состоянии.
Полученные данные записать в таблицу.
2. ВТОРОЕ СОСТОЯНИЕ реализуется, когда в стакан наливается тёплая вода.
Воду надо наливать так, чтобы запаянный конец В был погружен в воду. Так же как в 1-ом состоянии определить три параметра состояния:
![]()
![]()
![]()
Вычислить
![]() 5)
5)
Полученные данные занести в таблицу.
3. ТРЕТЬЕ СОСТОЯНИЕ исследуемой массы воздуха реализуется когда в стакан наливается горячая вода и определяются три параметра третьего состояния:
![]()
![]()
![]()
Вычислить
![]() (6)
(6)
Полученные данные занести в таблицу.
4. Обработать полученные результаты1 и сделать вывод.
4.1
Вычислить
среднее значение постоянной
![]() :
:
![]() (7)
(7)
4.2. Вычислить абсолютные погрешности каждого опыта:
![]()
![]()
![]() (8)
(8)
4.3. Вычислить среднее значение абсолютной погрешности:
![]() (9)
(9)
4.4. Вычислить относительную погрешность опытов
![]() (10)
(10)
ТАБЛИЦА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ И ВЫЧИСЛЕНИЙ
№№ пп |
Атмосферное давление |
Разность уровней |
Параметры газа |
Газовая постоянная |
Погрешности опыта |
|||||
Давление |
Объем |
Абсолютная температура |
Текущее значение |
Среднее значение |
Абсолютная |
Среднее значение абсолютной |
Относительная |
|||
|
|
|
Рр |
V |
T |
C |
|
|
|
|
мм.рт.ст. |
мм.рт.ст. |
мм.рт.ст. |
усл.ед. |
К |
усл.ед. |
усл.ед. |
усл.ед. |
усл.ед. |
% |
|
1
|
|
|
|
|
|
|
|
|
|
|
2
|
|
|
|
|
|
|
|
|
|
|
3
|
|
|
|
|
|
|
|
|
|
|
КОНТРОЛЬНЫЕ ВОПРОСЫ ПЕРВОГО УРОВНЯ
1. Какие параметры при описании свойств газов называются макроскопическими, а какие микроскопическими? Какие параметры называются термодинамическими?
2. Какие параметры полностью описывают состояния определённой массы газа?
КОНТРОЛЬНЫЕ ВОПРОСЫ ВТОРОГО УРОВНЯ
3. Как формулируется объединённый газовый закон и его запись в виде формулы?
4. Почему давление исследуемой массы газа определяется по формулам?
КОНТРОЛЬНЫЕ ВОПРОСЫ ТРЕТЬЕГО УРОВНЯ
5. Как достигается в данной работе неизменность массы исследуемого газа и какой это газ?
6. В чём причина того, что полученные значения не имеют одинаковые значения? Можно ли на основании этого сделать вывод, что объединённый газовый закон несправедлив?
Лабораторная работа № 2.
