
- •Закон мозлі
- •9 Квантово-механічна модель атома корпускулярно-хвильовий дуалізм
- •Принцип невизначеності
- •Хвильове рівняння шредінгера
- •Хвильові функції та електронні орбіталі
- •Характеристика стану електрона за квантовими числами
- •Атомні ядра склад і будова атомних ядер
- •Властивості взаємодіючих атомів
- •Валентність
- •Метод валентних зв'язків умови утворення ковалентного зв'язку
- •Водневий зв'язок природа й енергія водневого зв'язку
- •Міжчастинкові взаємодії доказ існування міжчастинкових сил
- •Вандерваальсова взаємодія молекул
- •Іонно-молекулярна взаємодія
- •Будова твердого тіла загальна характеристика твердого стану речовини
- •Будова ідеальних кристалів 7.2.1. Основні положення
- •Кристалічна гратка
- •Типи кристалічних ґраток
- •Будова іонних кристалів основні типи кристалічних ґраток іонних сполук
- •Металічний стан і його особливості кристалічна структура металів
- •Хімічний зв'язок у металах
Характеристика стану електрона за квантовими числами
Дискретні квантові стани електрона в атомі виявляються у відмінності форм орбіталей і відсутності проміжних форм між ними, а також у певному розміщенні орбіталей у просторі. У станах, що відповідають певним дискретним значенням енергії, дискретні і фізичні величини, значення яких виражаються квантовими числами. Кожний енергетичний стан електрона описується набором із чотирьох квантових чисел. Три з них характеризують хвильові властивості електрона і виникають при розв'язанні рівняння Шредінгера. Четверте квантове число відображає корпускулярні властивості електрона. Розглянемо фізичний зміст і значення кожного з цих чисел.
Головне квантове число п визначає загальну енергію електрона в межах певної орбіталі та середню радіальну віддаль максимуму електронної густини від ядра або розмір електронної хмарки. Воно може мати будь-які додатні цілочислові значення п = 1, 2, 3, ...і дорівнює числу вузлових поверхонь орбіталі.
Енергія електрона в атомі Гідрогену залежить лише від значення п і згідно з (5.14) перебуває в оберненій залежності від квадрата головного квантового числа

Зі
збільшенням значення п
загальна
енергія електрона зростає (стає менш
негативною) і при п
=
![]() досягає
нуля, тобто електрон не притягується
до ядра. Різниця енергій Е1-
Е
досягає
нуля, тобто електрон не притягується
до ядра. Різниця енергій Е1-
Е![]() ,
— це енергія
іонізації атома. Позитивне
значення енергії відповідає електрону,
що рухається вільно поза атомом. У цьому
випадку його енергія не квантується.
,
— це енергія
іонізації атома. Позитивне
значення енергії відповідає електрону,
що рухається вільно поза атомом. У цьому
випадку його енергія не квантується.
Стан електрона, що характеризується певним значенням n, називають енергетичним рівнем електрона в атомі. Енергетичні рівні позначають великими латинськими літерами:
![]()
Орбітальне (азимутальне) квантове число l в межах енергетичного рівня характеризує енергію електрона на підрівні та форму електронної орбіталі. Енергетичні рівні складаються з певного числа підрівнів, які виявляються в тонкій структурі спектрів (мультиплетність).
Орбітальне квантове число відповідає абсолютному значенню орбітального моменту кількості руху електрона, який, подібно до енергії, може набувати лише квантованих значень залежно від l:
![]()
Число l показує, скільки вузлових поверхонь хвильової функції електрона проходить через ядро і може мати цілочислові значення
![]()
При п>l можливі декілька станів з однаковим значенням п, але різним значенням l. Кількість підрівнів у кожному рівні дорівнює його номеру. Наприклад, при n = 1 може бути лише один підрівень з l = 0, при п = 2 — два підрівні з l = 0; 1, при п = 3 — три підрівні з l — 0; 1; 2. Отже, кожному енергетичному рівню відповідає декілька станів. Стани з однаковою енергією називають виродженими відносно l. Зокрема, стан з п = 2 двічі вироджений, з п = З тричі вироджений і т. д. Число таких станів називають кратністю виродження.
Енергетичні підрівні позначають цифрами та малими латинськими літерами:
![]()
їх називають s-, p-, d-, f-станами, а електрони, що перебувають у цих станах, s-, p-, d-, f-електронами. При певному значенні п найменшу енергію мають s-електрони, потім р-, d- і f-електрони. Щоб записати енергетичний стан електрона, що відповідає певним значенням п і l, п позначають цифрою, після якої йде буквене позначення l, наприклад 2s (n = 2, l = 0).
Магнітне квантове число тl визначає орієнтацію електронної орбіталі у просторі та напрямок орбітального кутового моменту електрона, тобто електромагнітні властивості електрона. Орієнтація вектора l у просторі задається його проекцією на вибрану напрямленість магнітного поля (наприклад, на вісь X). Ця проекція lх пов'язана з магнітним квантовим числом залежністю
![]()
З рівняння Шредінгера випливає, що в будь-якому l-стані при l≠ 0 (тобто крім s-стану) електрон, що рухається в атомі, створює магнітне поле. Орбітальний магнітний момент цього поля спрямований у напрямку, протилежному до орбітального кутового моменту, і також квантується. Одиницею виміру магнітного моменту в атомній системі є магнетон Бора — стала величина . Значення магнітного моменту і його проекції обчислюють зі співвідношень, аналогічних (5.33) і (5.34) для кутового моменту
![]()
Квантова механіка дає змогу визначити значення проекції моменту тільки на одну з осей, знайти інші проекції неможливо через принцип невизначеності. З цієї ж причини значення проекції моменту кількості руху не може точно збігатися зі значенням самого моменту (він завжди розміщений під кутом до вибраної осі), бо тоді дві інші проекції точно дорівнювали б нулю і стали б відомі значення та напрямок вектора моменту кількості руху електрона, а отже, швидкість і положення електрона в просторі.
Магнітне квантове число може набувати будь-яких цілочислових значень від +l до -l, включаючи нуль
![]()
Воно не може бути більшим за орбітальне число, оскільки проекція не перевищує значення вектора.
Кожному значенню l відповідає (21 + 1) можливих значень тl, які визначають кількість орбіталей на даному підрівні.
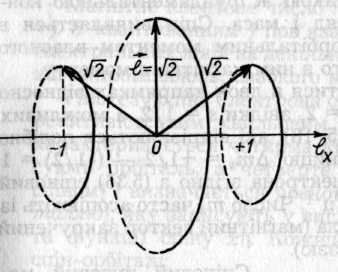
Рис. 5.17. Можливі проекції орбітальних моментів р-електрона в одиницях ħ
При відсутності зовнішнього поля у атома з даними n і l існує 21 + 1 стани з однаковою енергією, тобто ці стани вироджені. Під дією зовнішнього магнітного поля з напруженістю H в результаті взаємодії цього поля з магнітним полем електрона енергія електрона Е змінюється на ΔЕ відповідно до формули ΔЕ = ml μB Н.
У зв'язку з цим площина орбіталі електрона змінює своє положення в просторі — квантується. В межах одного підрівня енергетичні стани розщеплюються (підсилюється мультиплетність) з утворенням енергетичних комірок, віддаль між якими пропорційна напруженості поля. Тим самим у магнітному полі знімається виродження відносно тl На рис. 5.17 зображені можливі проекції орбітальних моментів електрона в р-стані lх довжиною 20.5 в одиницях ħ на напрямленість магнітного поля (вісь X) згідно з (5.34). Слід врахувати, що lу і lz при цьому продовжують залишатись невизначеними відповідно до принципу Гейзенберга.
Спінове квантове число ms визначає значення проекції спінового кутового моменту кількості руху електрона s на фіксовану вісь квантування
![]()
Значення спінового моменту знаходять зі співвідношення, аналогічного (5.33) для орбітального моменту
![]()
де s — квантове число (не плутати з s-станом електрона). Як і для орбітального руху, ms набуває всіх значень — від -s до +s, тобто всього 2s + 1 значень.
Магнітний орбітальний момент атома Гідрогену в основному стані (1s) при l = 0 дорівнює нулю, тому атом не повинен взаємодіяти з магнітним полем. Однак Штерн і Герлах (1922) виявили, що після проходження пучка атомів Гідрогену через магнітне поле він розщеплюється на два симетричні. Гаудсміт і Уленбек (1925) припустили, що електрон має додатковий ступінь вільності, який назвали спіном.
Поняття спіна відповідає класичному спрощеному уявленню про обертання електрона навколо власної осі, хоч воно й суперечить теорії відносності. Проте спін є такою ж фундаментальною константою електрона, як його заряд і маса. Спін виявляється в існуванні у електрона поряд з орбітальним моментом власного обертального моменту і пов'язаного з ним магнітного моменту.
Вектор спіна s може орієнтуватися в двох напрямках відносно поля, оскільки з досліду (2s + 1) = 2, звідки s = 1/2, а можливих значень ms два: +1/2 і -1/2 (рис. 5. 18), які відрізняються подібно до інших квантових чисел на одиницю: Δms = +1/2 — (-1/2) = 1 (крок квантування). Число ms часто асоціюють із циркуляційною поляризацією світла (магнітний вектор закручений за правою або лівою гвинтовою різзю).
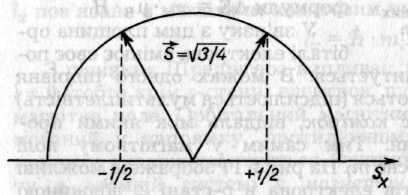
Рис. 5.18. Можливі проекції вектора спіна електрона в одиницях ħ
Спіновий кутовий момент пов'язаний зі спіновим магнітним моментом електрона, напрямленим протилежно першому. Значення його знаходять за співвідношенням
![]()
а проекція може мати тільки два значення
![]()
Тому атоми Гідрогену відхиляються в магнітному полі: їх магнітний момент не дорівнює нулю і орієнтований паралельно та ан-типаралельно полю — виродження зникає. Стани електрона з протилежними спінами дещо відрізняються за енергією (ΔЕ-0,0005 еВ), що й спричинює розщеплення ліній спектра атома Гідрогену.
Орієнтація спіна може змінюватися на протилежну, якщо електрон поглине випромінювання відповідної частоти. На цьому базується метод електронно-спінової резонансної спектроскопії (електронного парамагнітного резонансу).
