- •По структуре углеродного скелета антрацены подразделяются на мономерные, димерные и конденсированные соединения.
- •Физические и химические свойства
- •Распространение антраценпроизводных, локализация и динамика накопления в растениях
- •Анализ сырья, содержащего антраценпроизводные
- •Применение сырья, содержащего антрацены
Антраценпроизводные
Строение, классификация
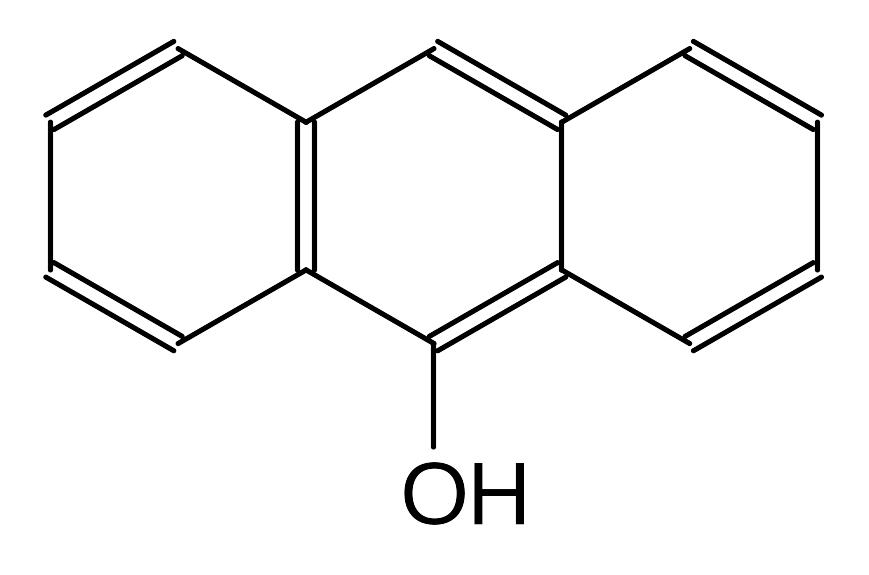
Антраценпроизводные – это группа природных соединений феенольной природы, в основе строения которых лежит ядро антрацена.
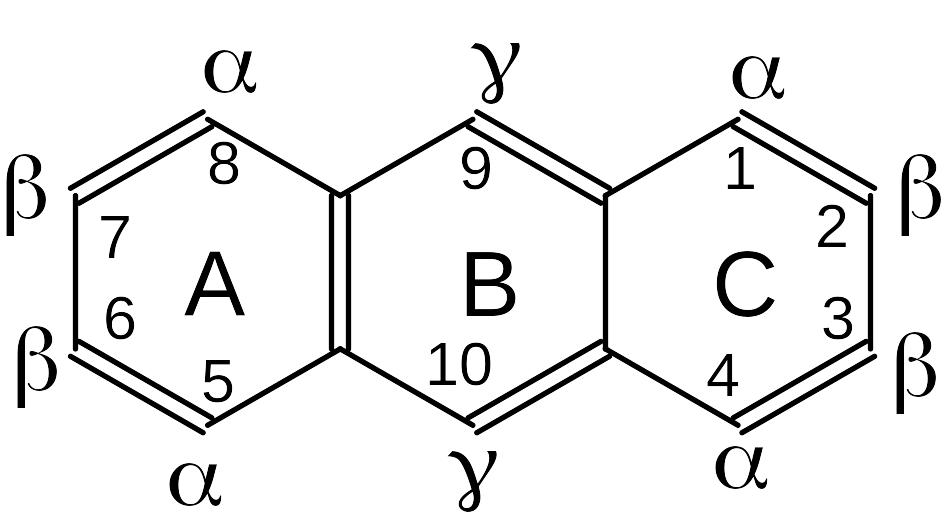
Все антраценпроизводные делятся на 2 подгруппы по степени окисленности кольца В:
окисленные формы– производные 9,10-антрахинона
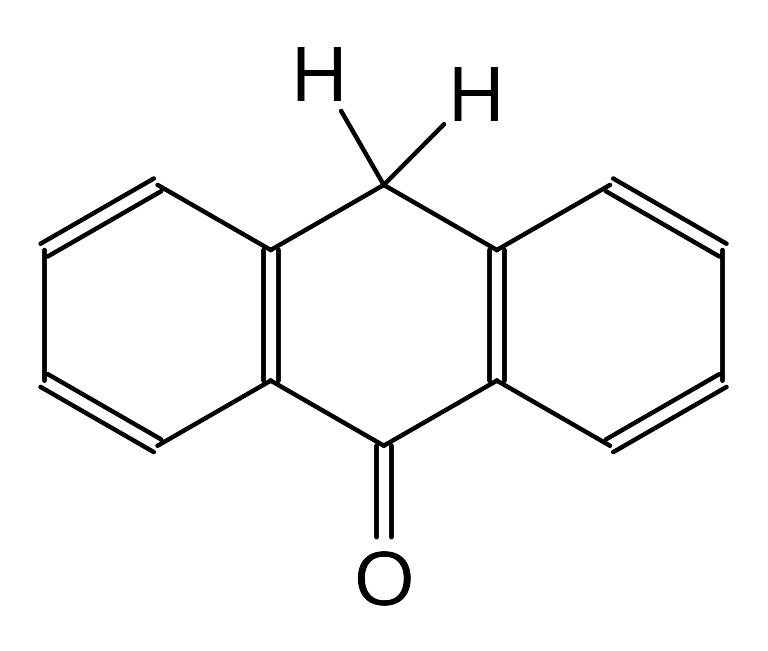
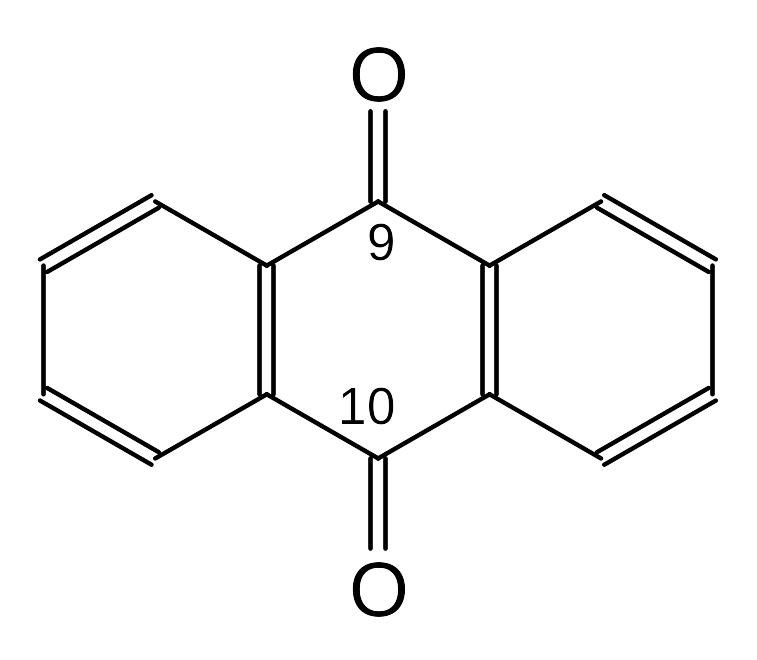 Антрахинон
Антрахинон
восстановленные формы – производные антранола и антрона
|
|
Антранол |
Антрон |
Природные соединения имеют в своем составе различные функциональные группы (фенольные гидроксилы, метильные, метоксильные, альдегидные, карбоксильные и карбинольные0. Встречаются производныые антрацена, содержащие несколько ОН-групп.
Все антраценпроизводные, имеющие гидроксилы в положениях 1,8 колец А и С (-положение), относят к производным хризацина. Это наиболее ценные соединения и они встречаются в растениях чаще.
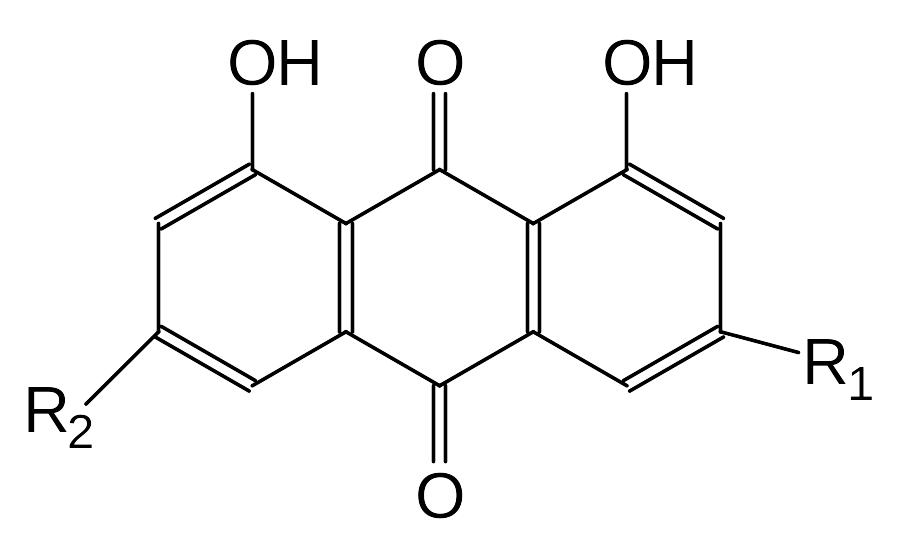
Примером могут служить следующие соединения:
|
R1=R2=Н – хризацин R1= СН3; R2=Н – хризофанол R1= СН2ОН; R2=Н – алоэ-эмодин R1=СООН; R2=Н – реин R1=СН3 ; R2=ОН – реум-эмодин |
Другие антраценпроизводные относятся к группе 1,2 дигидроксиантрахинонов, имеющих гидроксилы в - и -положениях (группа ализарина).
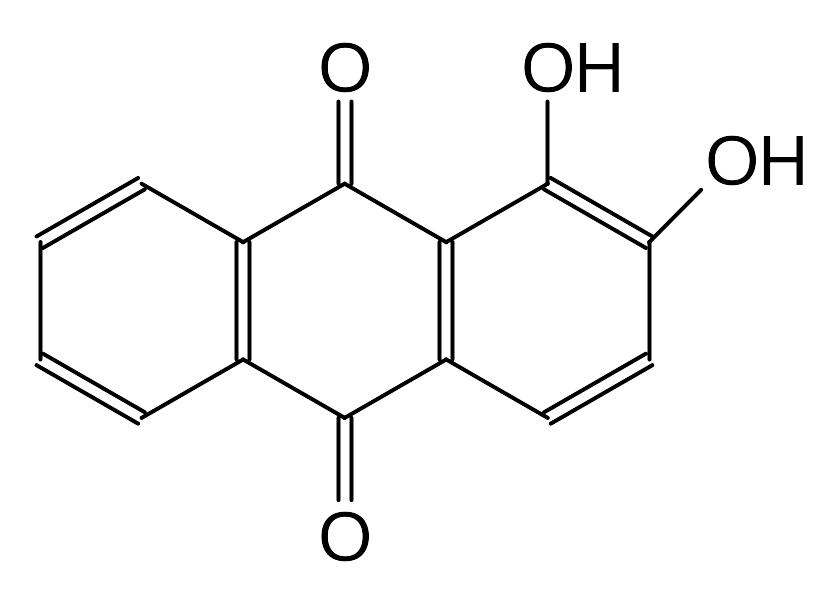
Ализарин
По структуре углеродного скелета антрацены подразделяются на мономерные, димерные и конденсированные соединения.
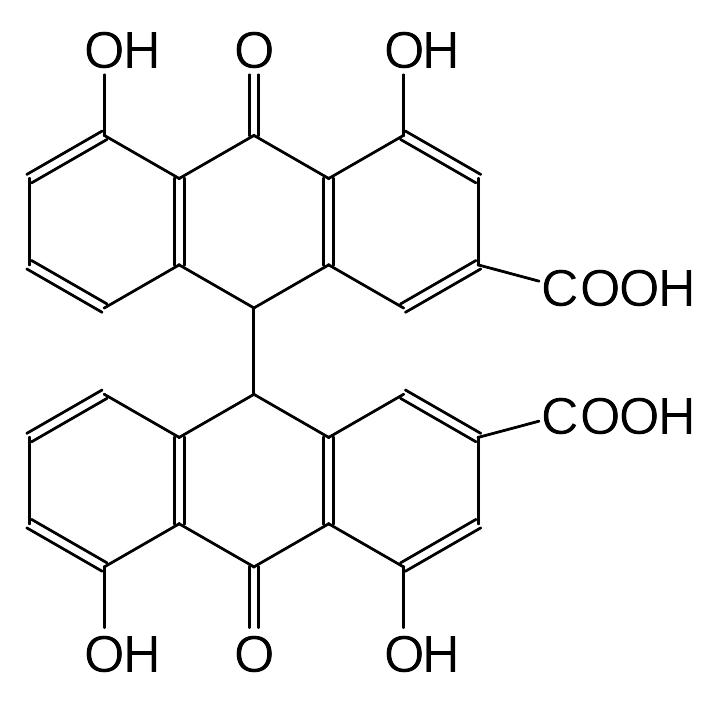
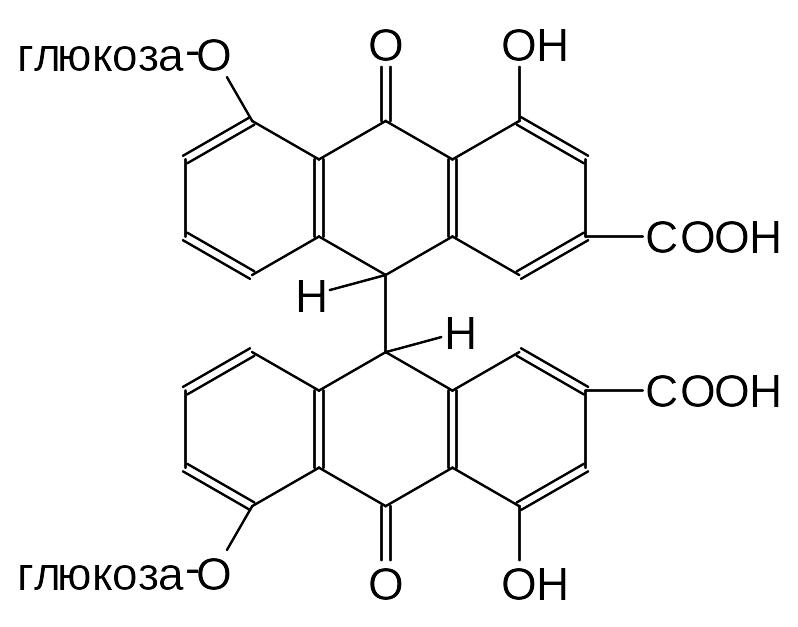
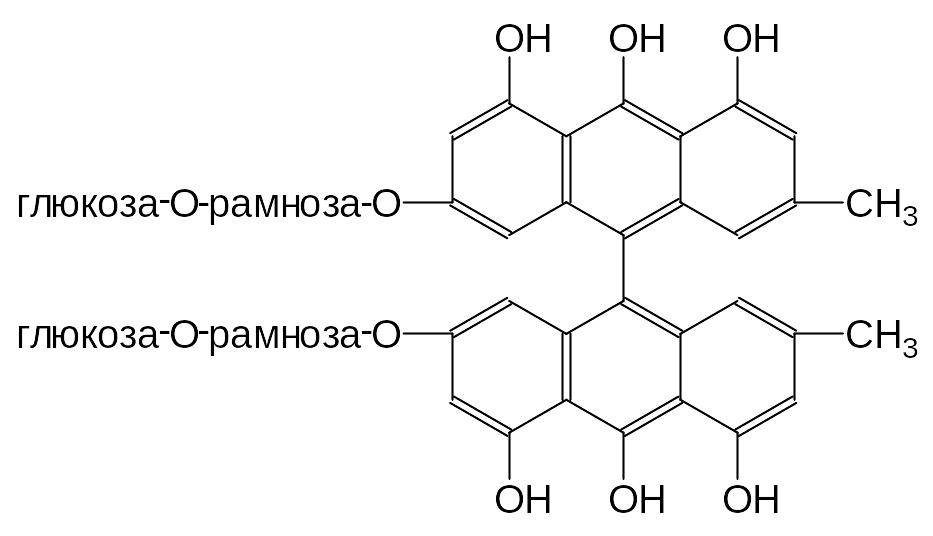
Димерные антраценпроизводные образуются при соединении двуз мономеров. Чаще всего конденсируются антронпроизводные по кольцу В в -положении. При соединении окисленых форм конденсация может иметь место по - и -положениям. При конденсации одинаковых мономеров образуется соединение, называемое диантроном, если разные – гетероантроном. Примером диантрона может быть сеннидин (диантрон реина), выделенный из листьев сенны, гетероантрона – пальмитин В из корней ревеня.
|
|
Сеннидин |
Пальмитин В (гетероантрон алоэ-эмодина и хризофанола) |
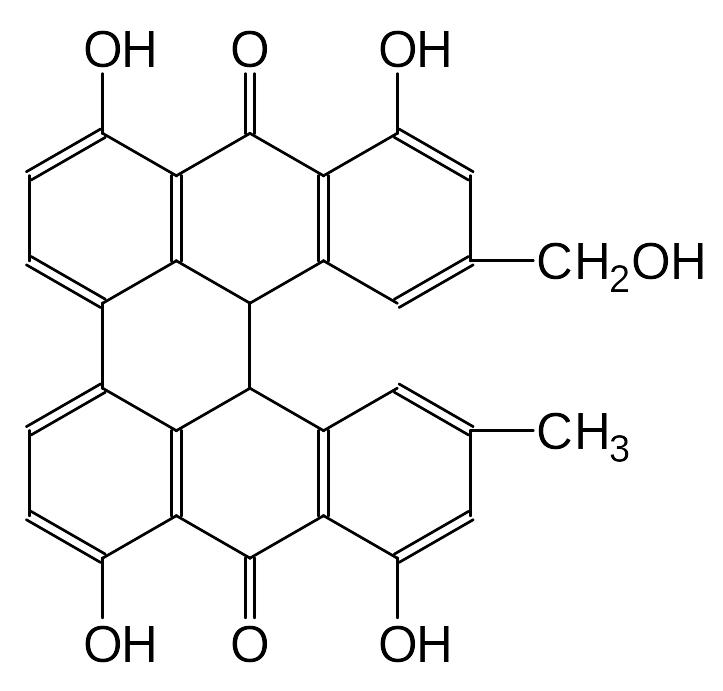
Конденсированные антраценпроизводные (нафтодиантроны) состоят из 2-х мономеров 1,8-дигидроксиантрахинонов, соединенных по - и -положениям. Примером может служить гиперицин, выделенный из разных видов зверобоя.
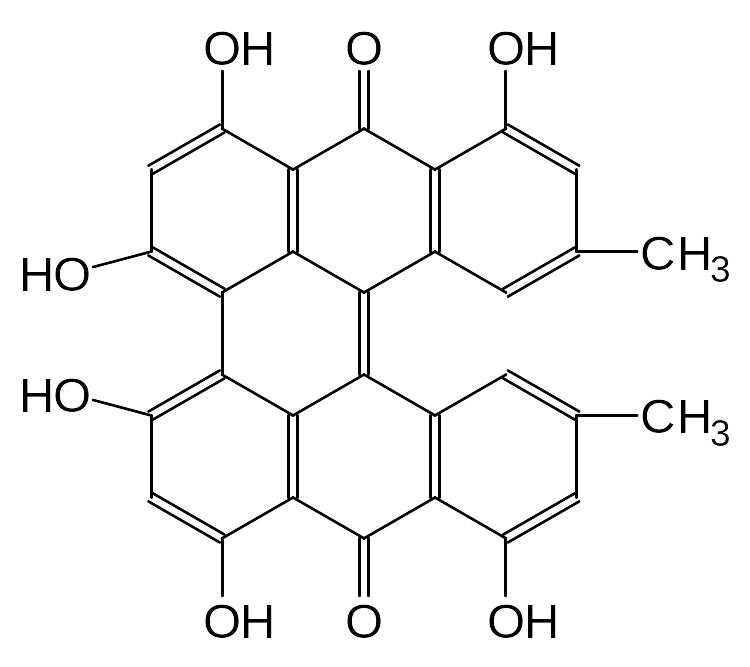
Гиперицин
В растениях антраценпроизводные могут находиться в свободном виде (агликоны) или в виде гликозидов. Антрагликозиды в качестве углеводного компонента чаще всего имеют глюкозу, рамнозу, иногда ксилозу и арабинозу. Сахара могут присоединяться в 1 и 8 положениях, реже в 3 и 6. Чаще встречаются О-гликозиды, но обнаружены также С-гликоизды в видах алоэ и сенны (например, в листьях алоэ содержится С-гликозид барбалоин).
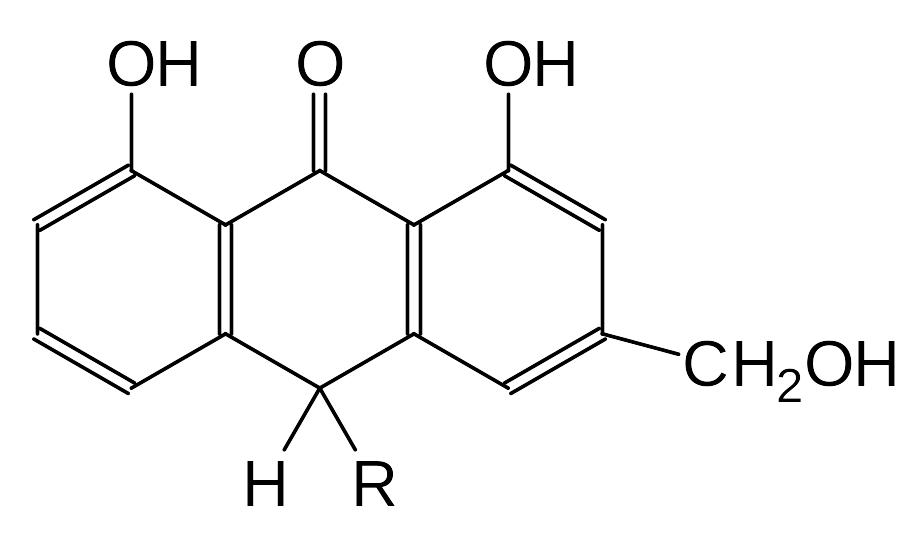
R = глюкоза - барбалоин
R = арабиноза – алоин
Гликозиды содержат один или два углеводных остатка (монозиды или биозиды) в одном положении (например, рубэритриновая кислота имеет глюкозу и ксилозу в положении 2), но могут быть и дигликозиды, когда сахара присоединяются в разных положениях.
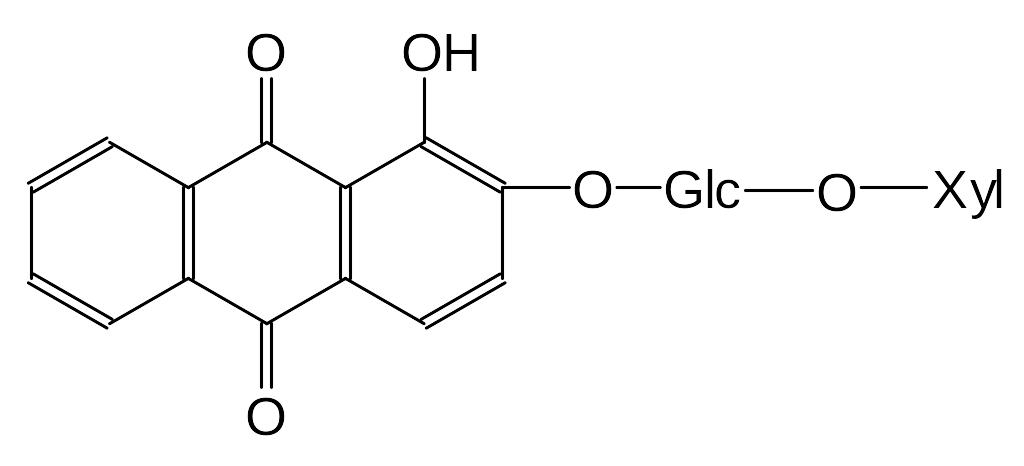
Рубэритриновая кислота
|
|
Сеннозид А |
Франгуларозид глюкозид (диантранол реум-эмодина) |
Физические и химические свойства
Антраценпроизводные – это твердые, кристаллические вещества, желтого, оранжевого или красно-оранжевого цвета. Гликозиды легко растворяются в воде, спиртах низкой концентрации и плохо или совсем не растворяются в органических растворителях.
Агликоны хорошо растворяются в эфире, хлороформе и других органических растворителях. Чрезвычайно легко они растворяются в щелочах, ледяной уксусной кислоте, как и гликозиды, но не растворяются в воде.
Гликозиды на вкус горькие, обладают оптической активностью и флюоресцируют в УФ-свете: антрахиноны – оранжевым, розовым или красным цветом; антроны и антранолы – желтым, голубым, фиолетовым.
Антраценпроизводные при нагревании до 2100 с возгоняются.
Характерным свойством всех антраценпроизводных является устойчивость их ядер. В присутствии щелочей и концентрированных кислот они дают окрашенные растворы с ионами щелочных металлов (Al, Cr, Sn) – очень устойчивые соли или комплексы – лаки.
Окисленные антраценпроизводные различно относятся к щелочам. Антрахиноны, имеющие гидроксилы в -положении, образуют феноляты только с гидроксидами щелочей, так как -гидроксилы образуют внутримолекулярную водородную связь с карбонильной группой, поэтому они менее реакционно способны, чем гидроксигруппа в -положении.
Антрахиноны, имеющие ОН-группу также в -положении, образуют феноляты с водными растворами карбонатов и гидроксидов щелочных металлов.