
8781
.pdf
191
частот. Этот результат парадоксальный, поскольку тело не имеет бесконечной энергии. Эта особенность классической теории теплового излучения была названа ультрафиолетовой катастрофой, поскольку подрывала все устои физики.
Формула планка*
Тупиковую ситуацию разрешил в 1890 г. немецкий физик-теоретик Макс Планк, предположивший, что электромагнитные колебания излучаются атомами не непрерывно, а дискретными порциями (квантами), энергия которых ε пропорциональна частоте ν
|
|
|
|
|
ε1 = hν , |
(8) |
|
где h = 6,63 ×10−34 Дж × с – постоянная Планка. |
|
||||||
Поэтому энергия осцилятора ε n |
= nε1 квантуется. |
|
|||||
Средняя энергия должна вычислятся с помощью распределения Больцмана: |
|||||||
|
∞ |
|
|
|
|
|
|
< ε (ν ) >= |
∑ nε1 exp[-nε1 |
/ kT ] |
|
hν |
|
||
n=0 |
|
|
= |
(9) |
|||
|
|
|
|
||||
∞ |
|
|
exp(hν / kT ) -1 |
||||
|
∑exp[-nε1 / kT ] |
|
|
||||
|
|
|
|
|
|||
n=0
Заметим что средняя энергия равна kT только для малых частот. Для больших частот эта величина экспоненциально уменьшается. Теперь, заменяя в формуле (7) kT выражение средней энергии, полученной в (9) для величины uν будем иметь :
u = kT × |
dN |
= |
8πhν 3 |
× |
1 |
(10) |
V × dν |
c3 |
|
||||
ν |
|
|
exp(hν / kT ) -1 |
|||
Это известная формула Планка, которая даёт корректный спектр теплового излучения. Для излучательной способности абсолютно чёрного тела получаются соотношения:
r |
= |
2πhν3 |
× |
1 |
|
или r |
= |
2πhc2 |
× |
1 |
|
exp[hνkT ]-1 |
|
exp[hc λkT ]-1 |
|||||||
ν,T |
|
c2 |
|
λ,T |
|
λ5 |
|
|||
|
|
|
|
|
|
|||||
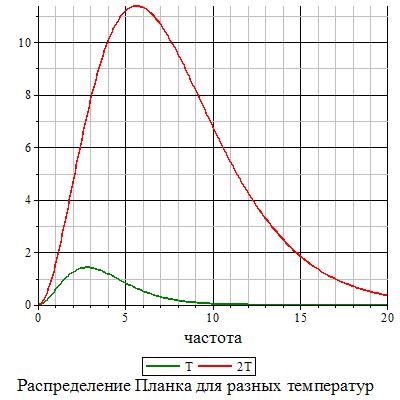
Графики первой из двух функций приведены на рисунке для двух температур, отличающихся в два раза (единицы измерения по осям условные).
192
Закон Стефана – Больцмана. Законы Вина.
Из рисунка видно, что спектр абсолютно черного тела всегда является сплошным, то есть в спектре представлен непрерывный ряд длин волн.
Поскольку энергетическая светимость АЧТ
Rэ = ∞∫ rλdλ, площадь под кривой Кирхгофа пропорциональна излучательной
0
способности АЧТ. С увеличением температуры излучательная способность АЧТ растет. Закон Стефана – Больцмана: энергетическая светимость абсолютно черного тела
пропорциональна четвертой степени его термодинамической температуры
R = σТ4 , |
(11) |
э
где σ = 5,67 ×10−8 Вт× м−2К−4 – постоянная Стефана-Больцмана.
Для реальных тепловых излучателей Rэ = kσТ4 , где k – коэффициент серости.
Закон (11) был получен экспериментально ранее формулы Планка.
Интегрированием распределения Планка, можно получить этот закон, а кроме того показать, что постоянная Стефана-Больцмана выражается через фундаментальные постоянные:

193
σ = 2π 5 k 4
15c 2 h3
Из рис. следует, что для каждой температуры кривые Планка имеют максимум что с ростом температуры максимум смещается в сторону более коротких длин волн, то есть
больших частот. Немецкий физик Вин установил, что длина волны λm , соответствующая максимальному значению спектральной плотности энергетической светимости АЧТ обратно пропорциональна его термодинамической температуре Т:
λm |
= |
C1 |
, |
(12) |
|
||||
|
|
T |
|
|
где C1 = 2,9 ×10−3 м× К .
Это первый закон Вина, или закон смещения Вина.
Второй закон Вина позволяет определить само значение максимальной спектральной плотности энергетической светимости rλm АЧТ при данной температуре Т:
r |
= C |
2 |
T 5 |
, |
(1.5) |
λm |
|
|
|
|
где C2 = 1,29 ×10−5 Втм−3К−5 .
Законы Вина также могут быть получены из формулы Планка. Для этого нужно выразить точку максимума распределения и найти зависимость максимальной излучательной способности от температуры.
Вычисляя производную получим
drλ |
= const ×[5(1 - exp(-x)) - x] = 0, где x = |
hc |
. |
dλ |
|
||
|
λkT |
||
Уравнение 5(1 - e− x ) = x может быть решено приближенно
(итерациями). Возьмём x0=0 и подставим его в левую часть, тогда в правая часть даст следующее приближение x1=5, подставляя его в левую часть получим x2=5(1-е-5)= 4,97. Видим, что второе приближение мало отличается от первого, следовательно можно его принять в качестве приближённого решения. В результате для первого закона Вина получим:
hc = 4,97
λkT
194
Что даёт коэфициенты, совпадающие с приведённой выше эмпирической формулой (12).
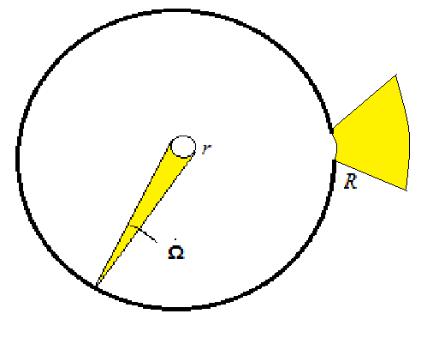
Приведем связь между интенсивностью I излучения абсолютно чёрного тела и равновесной плотностью энергии излучения u в окружающем пространстве. Для простоты вывода рассмотрим тело в виде сферической полости, радиусом R, а величину u вычислим в центре этой полости. По определению [ I ]=Дж/(c м2ср), то есть даёт мощность, выходящую из единичной площади тела в определённом направлении в расчёте на единичный телесный угол (в стерадианах ср).
Выделим в ценре полости небольшой шаровой объём, радиуса r. Этот объём виден из какой то точки полости под телесным углом U=πr2/R2. C с каждого квадратного сантиметра поверхности тела в 1 секунду на рассматриваемый объём падает энергия I U .
Поскольку энергия протекает через площадь πr2, вытекающая за секунду энергия равна должна иметь плотность u1: u1πr2c= I U или
u1 = |
I |
. |
|
cR 2 |
|||
|
|
Полная плотность энергии u складывается из излучения всей
поверхности полости, площадью 4πR2 в результате получим окончательную формулу:
u = |
4π I |
. |
(13) |
|
|||
|
c |
|
|
Заметим, что если в сферической полости проделать небольшое отверстие, то энергетическая светимость этого отверстия RЭ будет определятся формулой (11), а через плотность энергии внутри полости выразится следующим образом:
|
|
|
|
|
195 |
R |
|
= |
с × u |
. |
(14) |
Э |
|
||||
|
4 |
|
|
||
|
|
|
|
||
Подробности вычислений можно найти в учебниках.
Основы квантовой механики**
Спектр водорода. Постулаты Бора
Простейшим атомом является атом водорода, состоящий из одного протона в ядре и одного электрона, движущегося в кулоновском электрическом поле ядра.
Водородоподобными ионами (изоэлектронными водороду) называют ионы Не+, Li++, Be+++ и
т.д., имеющие ядро с зарядом Ze и один электрон.
Среди оптических свойств атома важнейшим является его спектр излучения. Частоты линий ν в дискретном линейчатом спектре атома водорода описываются формулой Бальмера – Ридберга
|
1 |
|
1 |
|
|
|
|
- |
|
(1) |
|||
ν = сR |
|
2 |
2 |
, |
||
n |
|
|
n1 |
|
|
|
где с – скорость света в вакууме; n и n1 – положительные целые числа, причем n1>n.
Величина R называется постоянной Ридберга ( R = 1,0973731×107 м−1 ). |
|
|||||||
Целые числа n |
и n1 называются главными |
квантовыми числами, причем |
||||||
n1 = n + 1,n + 2 и т.д. |
Группа линий с одинаковым числом n называется серией. |
Серии |
||||||
линий водородного спектра: n = 1 – серия Лаймана, |
|
n = 2 – |
серия Бальмера, n = 3 – |
серия |
||||
Пашена, n = 4 – серия Брэкета, n = 5 – серия Пфунда, n = 6 – серия Хэмфри. |
|
|||||||
Для водородоподобных ионов формула Бальмера-Ридберга имеет вид |
|
|||||||
|
|
1 |
|
1 |
|
|
||
|
ν = Z 2 R |
|
|
|
- |
|
, |
(2) |
|
|
|
2 |
2 |
||||
|
|
|
|
|
|
|||
|
n |
|
|
n1 |
|
|
||
где Z – порядковый номер элемента в периодической системе Менделеева.
Спектр и энергетические уровни атома водорода были объяснены впервые с помощью постулатов Бора.
Первый постулат Бора (постулат стационарных состояний): в атоме существует набор стационарных состояний, находясь в которых атом не излучает электромагнитные волны. Стационарным состояниям соответствуют стационарные орбиты, по которым электроны движутся с ускорением, но излучение света при этом не происходит.

196
Правило квантования орбит: в стационарном состоянии атома электрон, движущийся по круговой орбите, имеет квантованные значения момента импульса, удовлетворяющие условию:
|
Lk = mυr = kH |
( k = 1,2,3,...). |
(3) |
Здесь m – |
масса электрона, υ – его скорость, r – |
радиус k − й орбиты, H = h / 2π . |
|
Второй |
постулат Бора (правило частот): |
при переходе атома из |
одного |
стационарного состояния в другое испускается или поглощается один фотон. Излучение фотона происходит при переходе атома из состояния с большей энергией в состояние с меньшей энергией. При обратном переходе происходит поглощение фотона. Энергия hν фотона равна модулю разности энергий в двух состояниях атома:
|
Wn − Wm |
|
= hν. |
(4) |
|
|
|||
|
||||
При Wn > Wm происходит излучение фотона, при Wn < Wm – |
его поглощение. |
|||
2. Корпускулярно-волновая двойственность свойств частиц вещества. Волны де Бройля
Физика атомов, молекул и их комплексов, в частности кристаллов, а также атомных ядер и элементарных частиц изучается в квантовой механике. Объекты микромира, изучаемые квантовой механикой, имеют линейные размеры порядка 10-6 ÷ 10-12 см. Если частицы движутся со скоростями υ << c , где с – скорость света в вакууме, то применяется нерелятивистская квантовая механика.
Основополагающей в квантовой механике служит идея о том, что корпускулярноволновая двойственность свойств, установленная для света, имеет универсальный характер. Все движущиеся частицы обладают волновыми свойствами.
Формула де Бройля устанавливает зависимость длины волны, связанной с движущейся частицей вещества, от импульса р частицы
λ = |
h |
= |
h |
, |
(2.5) |
|
p |
mυ |
|||||
|
|
|
|
|||
где m – масса частицы, υ – ее скорость, h – |
постоянная Планка. Волны, о которых идет |
|||||
речь, называются волнами де Бройля. |
|
|
|
|
||
H = h = 1,05 ×10−34 Дж × с. 2π
Длина волны де Бройля для частицы с массой m , имеющей кинетическую энергию
Wk ,

197
λ = |
h |
(2.6) |
. |
 2mWk
2mWk
Формула де Бройля экспериментально подтверждается опытами по рассеянию электронов и других частиц на кристаллах и по прохождению частиц сквозь вещество. Признаком волнового процесса во всех таких опытах служит дифракционная картина распределения электронов (или других частиц) в приемниках частиц.
Волновые свойства не проявляются у макроскопических тел. Длины волн де Бройля для таких тел настолько малы, что обнаружение волновых свойств оказывается невозможным.
Соотношения неопределенностей Гейзенберга
Волновые свойства микрочастиц вносят ограничения в возможность применять к таким частицам понятия координаты и импульса в их классическом смысле.
В классической физике также существуют ограничения в применении некоторых понятий к определенным объектам. Так, понятие температуры не имеет смысла применять для одной молекулы, понятие о точной локализации (пребывание в одной точке) неприменимо к определению положения в пространстве волны и т.д. Однако в классической механике определенному значению координаты частицы соответствуют точные значения ее скорости и импульса. В квантовой механике существуют ограничения в возможности одновременного точного определения координаты частицы и величины ее импульса. Эти ограничения связаны с корпускулярно-волновой двойственностью свойств микрочастиц.
Соотношениями неопределенностей Гейзенберга называются неравенства |
|
|
Dx × Dp x ³ h, Dy × Dp y ³ h, Dz × Dpz |
³ h . |
(2.7) |
Здесь x , y и z означают интервалы координат, |
в которых может |
быть |
локализована частица, описываемая волной де Бройля, если проекции ее импульса по осям
координат заключены в интервалах px , p y |
и pz соответственно. |
Соотношения Гейзенберга показывают, |
что координаты частицы x, y, z и проекции |
px , p y , pz ее импульса на соответствующие оси не могут одновременно иметь значения в |
||
точности равные x и px , y и |
p y , z и pz . |
Эти физические величины могут иметь |
значения, заданные с точностью, |
определяемой |
соотношениями Гейзенберга. Чем более |
точно определено положение частицы, т.е. чем меньше x , |
y и |
z , тем менее точно |
определены значения проекций ее импульса (т.е. тем больше |
px , |
p y и pz ). Если |
198
положение частицы на оси ОХ определено точно и x = 0 , то px = ∞ и значение
проекции импульса px становится совершенно неопределенным.
Соотношения неопределенностей накладывают в квантовой механике определенные ограничения на возможности описания движения частицы по некоторой траектории.
В классической теории в каждой точке траектории частица имеет определенные координаты x, y,z и определенный импульс p с проекциями по осям px , p y , pz . В
квантовой механике это реализуется только в тех случаях, когда частица движется в макроскопической области пространства (например, оставляет след на фотопластинке или экране осциллографа). Если, например, положение электрона зафиксировано с точностью, определяемой линейными размерами зерна фотоэмульсии, испытывающего воздействие
электрона, |
то |
Dx ~ 10−6 м . |
Этому |
соответствует |
|
неопределенность |
импульса |
||||||||
Dpx |
³ |
h |
~ 10 |
−27 |
кг × м / с |
и |
скорости |
Dυx = |
px |
|
~ 10 |
3 |
м / с. |
Эта неопределенность |
|
Dx |
|
m |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
при |
скоростях |
электронов |
порядка (106 ¸107 )м / с |
позволяет |
считать, что |
электрон |
|||||||||
движется по определенной траектории с точно заданной в каждой точке скоростью.
Если частица движется в макроскопической области пространства, то соотношения неопределенностей существенно сказываются на характере движения частицы. Например, положение электрона, движущегося в атоме, может быть определено с точностью до
размеров атома, то есть Dx ~ 10−10 м . Неопределенность скорости υx оказывается при этом такого же порядка, что и сама скорость: Dυx » 106 м / с » υ. Траектория электрона в атоме с точно заданной в каждой точке скоростью не имеет смысла. Это вовсе не означает, что соотношения неопределенностей свидетельствуют о принципиальной ограниченности наших знаний о микромире. Эти соотношения лишь отражают ограниченную применимость понятий классической физики в области микромира.
Соотношения неопределенностей не вносят ограничений в возможность использовать в классическом смысле понятия координаты и импульса для макроскопических тел. Волновые свойства у таких тел не проявляются и поэтому для макроскопических тел соотношения
неопределенностей не играют никакой роли. |
|
Соотношение неопределенностей для энергии W и времени t : |
|
DW × Dt ³ h , |
(2.8) |
где DW – неопределенность энергии частицы, которая находится в течение времени Dt в
состоянии с энергией W . Энергия частицы в данном состоянии может быть определена тем точнее, чем дольше частица находится в этом состоянии.

199
Уравнение Шредингера**
Положение частицы в пространстве в данный момент времени определяется в
квантовой механике заданием волновой функции (пси-функции) Ψ(x, y,z,t ). |
Вероятность |
||||||||||||||||
dω того, что частица находится в момент времени t в малом объеме dV |
вблизи точки |
||||||||||||||||
M (x, y,z), равна |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
dω = |
|
Ψ |
|
2 dV , |
(2.9) |
|
|
||||||||||||||||
где |
|
Ψ |
|
2 – квадрат модуля Ψ -функции: |
|
Ψ |
|
2 = ΨΨ * . Здесь Ψ * – функция, комплексно |
|||||||||
|
|
|
|
||||||||||||||
сопряженная с Ψ . Величина |
|
Ψ |
|
2 есть плотность вероятности пребывания частицы в |
|||||||||||||
|
|
||||||||||||||||
данной точке пространства: Ψ 2 = dω = ρ . Интенсивность волны де Бройля определяется
dV
величиной Ψ 2 .
Волновая функция Ψ(x, y,z,t ) является основной характеристикой состояния
микрообъектов (атомов, молекул, элементарных частиц). С ее помощью вычисляется среднее
значение физической величины L , характеризующей объект, находящийся в состоянии,
описываемом волновой функцией Ψ ,
+∞ |
2 |
|||
(L) = ∫ ∫ ∫ L |
|
Ψ |
|
dxdydz , |
|
|
|||
−∞ |
|
|
|
|
|
|
|
|
|
где (L) – среднее значение величины L . |
|
|
|
|
Какому уравнению должна подчинятся волновая функция для состояния, когда энергия системы фиксирована (стационарное уравнение шредингера).
Волновое уравнение может быть записано в виде:
∂2 S − |
1 |
∂2 S = 0 |
|
||
∂2 x V 2 |
∂2t |
|
Для гармонической волны зависимость от времени определяется формулой
S (t, x) = A ×sin(ωt M kx) тогда заменяя вторую производную по времени соотношением
&& |
= −ω |
2 |
Asin(ωt M kx) = −ω |
2 |
S , |
запишем уравнение в виде: |
||||||||||
S |
|
|
|
|||||||||||||
∂2 S |
|
ω |
2 |
|
ω 2 |
|
2π 2 |
∂2 S |
|
2π 2 |
||||||
∂ |
|
− |
|
|
|
S = 0; |
|
= |
|
|
; |
∂2 x |
− |
|
S = 0 |
|
2 x |
V |
|
V 2 |
λ |
|
|
||||||||||
|
2 |
|
|
|
|
|
λ |
|||||||||

