
- •Правила техники безопасности. Знакомство с техникой выполнения лабораторных работ. Основные свойства важнейших классов неорганических веществ.
- •Лабораторная работа № 1 Основные классы неорганических соединений
- •Порядок выполнения работы
- •Лабораторная работа №2 Химическая кинетика .Химическое равновесие.
- •Лабораторная работа №3 Электролитическая диссоциация
- •Лабораторная работа №4 Способы выражения концентрации растворов
- •Формулы перехода от одних выражений концентраций растворов к другим
- •100 Г раствора - 1 г NaCl
- •201,315 Г раствора - х г NaCl
- •1. Что такое раствор? Какими способами можно выразить содержание растворенного вещества в растворе?
- •Лабораторная работа №5 Приготовление растворов заданной концентрации
- •Лабораторная работа №6 Окислительно-восстановительные реакции
- •Лабораторная работа №7
- •Пример 6.
- •Пример7.
- •Лакмус содержит так называемую азометиновую кислоту, недиссоциированные молекулы которой красного цвета, а анионы – синего цвета.
Пример 6.
Составьте молекулярное и ионно-молекулярное уравнение реакции гидролиза соли CuCl2 .
Решение:
Хлорид меди – соль слабого многокислотного основания Cu(OH)2 и сильной кислоты HCl . В данном случае катионы Cu2+ связывают гидроксильные ионы воды, образуя катионы основной соли CuOH+. Образование молекул Сu(OH)2 не происходит, так как ионыCuOH+ диссоциируют гораздо треднее, чем молекулы Cu(OH)2.
В обычных условиях гидролиз идет по первой ступени.
Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
Cu2+ + H2O ⇄ CuOH+ + H+
или в молекулярной форме:
CuCl2 + H2O ⇄CuOHCl + HCl
В растворе появляется избыток ионов водорода, поэтому раствор ZnCl2 имеет кислую реакцию (рН > 7) .
Пример7.
Составьте молекулярное и ионно-молекулярное уравнение реакции гидролиза соли Pb(CH3COO)2 .
Решение:
Ацетат свинца – соль слабого многокислотного основания Pb(OH)2 и слабой одноосновной кислоты CH3COOH. В данном случае параллельно протекают два процесса:
Pb+2 + H2O⇄PbOH+ + H+
СН3СОО- + Н2О⇄СН3СОО + ОН-
Ионно - молекулярное уравнение:
Pb2+ + СН3СОО- + Н2О ⇄ PbOH+ + СН3СООН
или в молекулярной форме:
Pb(СН3СОО)2 + Н2О ⇄ PbOHСН3СОО + СН3СООН
Реакция раствора при этом зависит от относительной силы кислоты и основания, образующих соль. Если Ккисл. = Косн., то катион и анион гидролизуются в равной степени и реакция раствора будет нейтральной (рН = 7). Если Ккисл. > Косн., то катион солигидролизуется в большей степени, чем анион, и концентрации ОН- - ионов. В данном случае реакция раствора слабокислая. Наконец, если Ккисл. < Косн., то гидролизу преимущественно подвергается анион соли, и реакция раствора будет слабощелочной.
Пример 8.
Какие продукты образуются при смешивании растворов солей Fe(NO3)3 и Na2CO3? Составьте ионно-молекулярное и молекулярное уравнение реакции.
Решение: Соль Fe(NO3)3 гидролизуется по катиону, а Na2CO3 – по аниону.
Fe3+ + Н2О ⇄ FeОН2+ + Н+
CO32־ + Н2О ⇄ НСО־3- + ОН
Гидролиз этих солей обычно ограничивается первой ступенью. При смешивании растворов этих солей ионы Н+ и ОН־взаимодействуют, образуя молекулы слабого электролита. Это приводит к тому, что усиливается гидролиз каждой из солей до образования осадка и газа: Fe(ОН)3 и СО2
Ионно-молекулярное уравнение
2 Fe+3 + 3CO32- + 3Н2О = 2Fe(ОН)2¯ + СО2
Молекулярное уравнение
2Fe(NO3)3 + 3Na2CO3 + 3Н2О = 2Fe(ОН)2¯ + 3СО2 + 6Na NO3
Для воды и ее растворов произведение концентрации ионов Н+ и ОН- величина постоянная при данной температуре и называется ионным произведением воды Кв. При 25оС Кв = [H+] · [OH-] = 1·10-14. Постоянство ионного произведения воды дает возможность вычислить концентрацию одного вида ионов, если известна концентрация другого вида ионов, а именно:
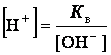
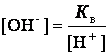
В
чистой воде [H+]
= [OH-]
= ![]() =
10-7 моль/л
=
10-7 моль/л
Концентрация ионов водорода указывает на характер среды:
[H+] = [OH-] = 10-7 моль/л, нейтральная среда;
[H+] > 10-7 моль/л, кислая среда;
[H+] < 10-7 моль/л, щелочная среда.
Для удобства оценки кислотности и щелочности среды пользуются не концентрацией водородных ионов, а величиной водородного показателя рН, он равен отрицательному десятичному логарифму концентрации водородных ионов рН = -lg[H+], следовательно, в щелочной среде рН > 7; в нейтральной среде рН = 7, в кислой среде рН < 7.
Пример 10. Вычислить рН раствора, если [H+] = 0,0001 = 10-4 моль/л.
Решение: [H+]= 0,0001 = 10-4 моль/л.
рН = -lg10-4 = 4; рН = 4
Порядок выполнения работы
Опыт 1. Определение реакции среды в растворах различных солей.
В пять пробирок до 1/3 их объема налить нейтральный раствор лакмуса. Одну пробирку оставить в качестве контрольной, а в остальные добавить по одному микрошпателю кристаллов следующих солей: в первую – хлорида алюминия, во вторую – карбоната натрия, в третью – хлорида калия, в четвертую – ацетата аммония.
По изменению окраски лакмуса сделать вывод о реакции среды в растворе каждой соли. Полученные результаты внести в таблицу.
Таблица 1.
Реакция среды в растворах солей
№ пробирки |
Формула соли |
Окраска лакмуса |
Реакция среды |
РН раствора рН<7 рН=7 рН>7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Какие из исследованных солей подвергаются гидролизу? Написать ионные и молекулярные уравнения реакций их гидролиза и указать вид гидролиза каждой соли (простой или ступенчатый).
В случае ступенчатого гидролиза написать уравнение реакции только для первой ступени, так как практически в достаточно концентрированных растворах последующие ступени протекают очень слабо.
Опыт 2. Случаи полнлго(необратимого)гидролиза солей.
.
В две пробирки внести по 6-8 капель раствора хлорида алюминия. В одну пробирку добавить такой же объем раствора сульфида натрия, в другую - раствора карбоната натрия. Отметить выделение сероводорода в первой пробирке (по запаху) и пузырьков диоксида углерода во второй. В обоих случаях в осадок выпадает гидроксид алюминия.
Написать уравнения реакций, которые привели к образованию гидроксида алюминия. Почему не получилось сульфида и карбоната алюминия.
Опыт 3. Влияние температуры на степень гидролиза соли.
В два стакана налить 1 М раствор ацетата натрия. Один стакан нагреть почти до кипения раствора. Затем в оба стакана капнуть по 3-5 капель фенолфталеина. Окраска появляется в стакане с горячим раствором, это указывает на усиление гидролиза при нагревании.
Опыт 4. Определение реакции среды.
Для определения реакции среды пользуются индикаторами – веществами, которые изменяют окраску в зависимости от концентрации в растворе ионов Н+.
Индикаторы – слабодиссоциирующие органические кислоты или основания, у которых недиссоциированные молекулы и ионы благодаря разному строению имеют различную окраску.
