
- •Методичні вказівки
- •Розрахункова робота №1
- •Теоретична частина
- •Порядок виконання роботи:
- •Контрольні запитання:
- •Приклад:
- •Розрахункова робота № 2
- •Теоретична частина
- •Порядок виконання роботи:
- •Контрольні запитання:
- •Розрахункова робота № 3
- •Теоретична частина
- •Порядок виконання роботи:
- •Контрольні запитання:
- •Приклад:
- •Теоретична частина
- •Порядок виконання роботи:
- •Приклад:
- •Розрахункова робота №5
- •Теоретична частина
- •Порядок виконання роботи:
- •Контрольні запитання:
- •Приклад:
- •Практична робота №6
- •Мета: Навчитися розраховувати сумарний коефіцієнт тепловіддачі Теоретична частина
- •Порядок виконання роботи:
- •Контрольні запитання:
- •Приклад:
- •Розрахункова робота №7
- •Мета: Навчитися розраховувати час нагрівання тонкого та масивного тіла. Теоретична частина
- •Порядок виконання роботи:
- •Вихідні дані для розрахунків приведені в таблиці 8
- •Визначити приведену ступінь чорноти системи піч-заготовка:
- •Контрольні запитання:
- •Приклад:
- •Вихідні дані для розрахунків приведені в таблиці 8
- •Визначити приведену ступінь чорноти системи піч-заготовка:
- •Визначити приведену ступінь чорноти системи піч-заготовка:
- •Визначити приведену ступінь чорноти системи піч-заготовка:
- •Розрахункова робота № 8
- •Теоретична частина
- •Порядок виконання роботи:
- •Кінцеву температуру диму знайти з рівняння теплового балансу рекуператора :
- •Контрольні запитання:
- •Приклад:
- •Кінцеву температуру диму знайти з рівняння теплового балансу рекуператора :
- •Розрахункова робота №9
- •Теоретична частина
- •Рекомендована література
Контрольні запитання:
Класифікація палива.
Хімічний склад палива.
Що називається теплотою згоряння палива?
Найвища та найнижча теплота згоряння палива.
Особливості горіння рідкого палива.
Особливості горіння газоподібного палива.
Приклад:
1. Визначити найнижчу теплоту згоряння мазута.
Склад мазута приведений в таблиці 1.
Таблиця 1 - Хімічний склад мазута
№ |
Хімічний склад мазута, % |
||||||
Ср |
Нр |
Sр |
Ор |
Nр |
Н2Ор |
Ар |
|
31 |
84,0 |
9,8 |
4,1 |
0,7 |
0,2 |
1,0 |
0,2 |
Найнижчу теплоту згоряння мазута визначаємо за формулою Д.І. Менделєєва:
![]()
![]()
![]()
Визначити найнижчу теплоту згоряння природного газу.
Склад природного газу приведений в таблиці 2.
Таблиця 2 - Хімічний склад природного газу
№ |
Хімічний склад природного газу, % |
|||||||
СН4 |
С2Н6 |
С3Н8 |
С4Н10 |
С5Н12 |
Н2S |
СО2 |
N2 |
|
31 |
83,4 |
2,5 |
1,7 |
0,8 |
- |
- |
7,4 |
4,2 |
Визначаємо склад вологого газу:
Приймаємо
вологість природного газу
![]() :
:
![]()
![]()
![]()
Тоді склад вологого природного газу:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
де К - кількість вологого компоненту газу.
Визначити найнижчу теплоту згоряння природного газу за формулою:
![]()
![]()
![]()
Після проведення розрахунків зробити висновок.
Розрахункова робота № 2
Тема: Розрахунок горіння газоподібного палива.
Мета: Навчитися визначати витрати повітря, кількість і склад продуктів горіння, температуру горіння.
Теоретична частина
Горінням називається процес взаємодії палива з окислювачем, що супроводжується виділенням тепла, а іноді і світла. Роль окислювача в більшості випадків виконує кисень повітря. Всяке горіння припускає перш за все тісний контакт між молекулами палива і окислювача. Щоб відбувалося горіння, необхідно забезпечити цей контакт, тобто необхідно змішати паливо з повітрям. Отже, процес горіння складається з двох стадій: змішення палива з повітрям і займання і горіння палива.
При горінні палива як окислювач використовують кисень повітря. В результаті утворюються продукти згорання і розвивається певна температура горіння. Тому розрахунки горіння палива виконуються з метою визначення:
а) кількості необхідного для горіння повітря;
б) кількості і складу продуктів згорання;
в) температури горіння.
Витрати повітря можна визначати як в об'ємних, так і в масових одиницях.
Найменша кількість повітря (кисню), яка необхідна для повного окислення одиниці горючої речовини, називається теоретичною кількістю. На практиці спалювання палива здійснюється при витратах повітря, що дещо перевищують теоретичну кількість - дійсні витрати повітря. Величина, що показує відношення дійсної витрати повітря (Vд) до теоретичної кількості (Vт), називається коефіцієнтом надлишку повітря :
![]() ,
,
і грає на практиці дуже важливу роль.
Коефіцієнт надлишку повітря придатний тільки для повного згорання палива в повітрі.
При неповному ж згоранні, коли кількість кисню, що подається, менше теоретичного, застосуємо тільки коефіцієнт витрати кисню, який стає менше одиниці.
Під температурою горіння розуміють ту температуру, якої набувають продукти згорання в результаті повідомлення їм тепла, виділеного при спалюванні. Розрізняють теоретичну, калориметричну та практичну температуру горіння палива.
Продукти згоряння палива нагріваються до високих температур, при яких можлива дисоціація С02 і Н2О, що досягає іноді 10 %. В результаті дисоціації відбувається зміна об'єму і зменшується кількість тепла, що виділяється, оскільки в процесі дисоціації поглинається тепло.
Теоретична температура горіння визначається з урахуванням дисоціації в продуктах згорання, тобто
 ,
,
де
![]() -
теплота згорання палива, Дж/м3
або Дж/кг;
-
теплота згорання палива, Дж/м3
або Дж/кг;
qдис - тепло, що пішло на процес дисоціації, Дж;
Vпр - об'єм продуктів згорання, що утворюються при згоранні одиниці палива, м3;
C - питома теплоємність продуктів згорання, кДж/(м3-К).
Практичною температурою називають дійсну теппературу в топці печі з урахуванням втрат на дисоціацію і теплопередачу в навколишнє середовище; є усередненою величиною.
tпр = ŋ · tк ,
де ŋ - пірометричний коефіцієнт, який залежить від колнструкции печі (ŋ = 0,62 - 0,82)
Калориметрична температура визначається з умови, що все тепло. Яке виділилося при горінні, витрачається тільки на підвищення температури продуктів згоряння. Іншими словами, калориметрична температура горіння визначається для адиабатных умов, коли відсутній теплообмін із зовнішнім середовищем. Отже
![]()
За наявності підігрітого повітря (або палива) калориметричну температуру можна визначити з виразу:
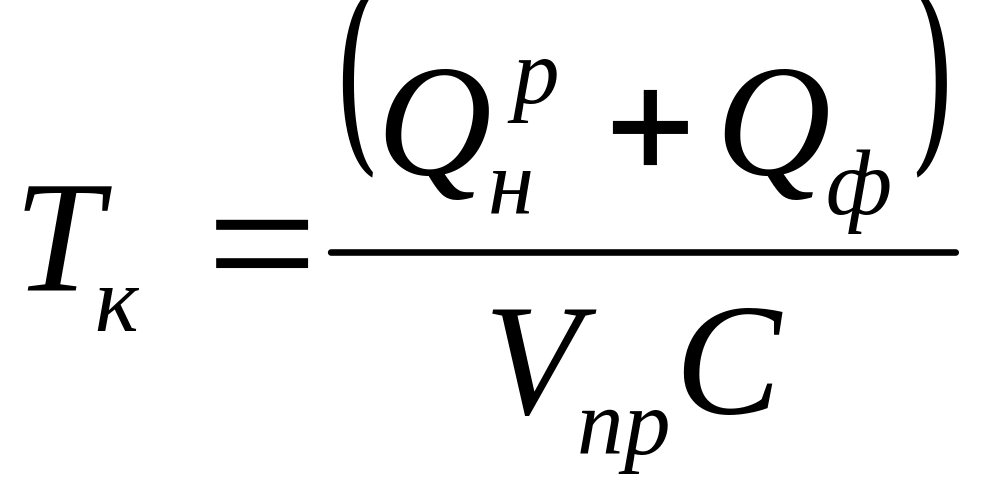 ,
,
де Qф - фізичне тепло підігріву повітря і палива.
На практиці звичайно визначають калориметричну температуру горіння, яка є однією з характеристик палива.
Розрахунок калориметричної температури виконують з умов повного згорання палива таким чином. Продукти згорання будь-якого палива є сумішшю різних газоподібних складових СО2, H2O, N2, O2, SО2. Кожній з цих складових при тій або іншій температурі властива цілком певна величина теплоємності. Це дає можливість визначити теплоємність продуктів згорання в цілому для відповідної температури.
Ентальпія продуктів згорання, як суміші газів, визначають аналогічно визначенню теплоємності продуктів згорання.
