
- •Некоторые сведения из курсов физики и
- •1.1 Основные свойства газа
- •1.2. Основные сведения из термодинамики
- •2. Основные законы сжимаемой среды
- •2.1. Вводные замечания
- •2.2. Закон сохранения массы
- •2.3. Закон изменения количества движения
- •2.4. Закон изменения момента количества движения
- •2.5. Закон сохранения энергии
- •2.6. Уравнение Бернулли - Сен Венана. Параметры заторможенного газа
- •3. Число маха. Режимы течения газа
- •4. Связь между площадью сечения и скоростью потока газа. Сопло лаваля
- •5. Истечение газа из резервуара через сходящуюся насадку
- •6. Режимы работы сопла лаваля
- •7. Критерии подобия. Газодинамические функции
- •8. Скачки уплотнения
- •8.1. Скорость распространения волн сжатия
- •8.2. Прямой скачок уплотнения
- •8.3. Косой скачок уплотнения
- •9. Основные задачи установившегося движения газа в трубах
- •9.1. Изотермическое движение идеального газа в горизонтальном трубопроводе
- •9.2. Установившееся изотермическое движение реального газа в горизонтальном трубопроводе
- •1.1. Основные свойства газа 4
1.2. Основные сведения из термодинамики
Первое
начало термодинамики представляет
собой частную форму применительно к
тепловым процессам всеобщего закона
природы - закона превращения и сохранения
энергии. Для квазистатических
процессов он формулируется следующим
образом: подведенное к единице массы
газа бесконечно малое количество
тепла
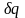 расходуется на повышение внутренней
энергии газа
расходуется на повышение внутренней
энергии газа
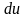 и
на выполнение термодинамической работы
и
на выполнение термодинамической работы
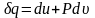 (1.8)
(1.8)
где - удельный объем, определяемый по формуле (1.2).
Формальное интегрирование выражения (1.8) позволяет найти полное количество тепла, которое подведено к газу в процессе изменения его состояния от начального 1 до конечного 2.
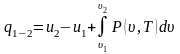 (1.9)
(1.9)
Интеграл,
стоящий в правой части равенства (1.9),
представляет работу термодинамического
процесса расширения и зависит от
характера процесса, т.е. вида кривой,
соединяющей точки 1 и 2 на поверхности
.
Это
указывает на то, что
,
входящее в равенство (1.8), не является
полным дифференциалом. Однако, если обе
части равенства (1.8) умножить на
интегрирующий множитель
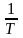 ,
то выражение
,
то выражение
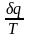 становится полным дифференциалом
некоторой функции состояния
становится полным дифференциалом
некоторой функции состояния
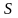 ,
называемой энтропией, т.е.
,
называемой энтропией, т.е.
 (1.10)
(1.10)
При
переходе газа из состояния 1 в состояние
2 изменение
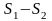 не
зависит от характера процесса перехода,
а целиком и полностью определяется
начальным и конечным состояниями.
не
зависит от характера процесса перехода,
а целиком и полностью определяется
начальным и конечным состояниями.
Следует обратить внимание, что равенство (1.10) справедливо для обратимых процессов. Обратимым называется процесс изменения состояния, который, будучи переведен в обратном направлении, возвращает систему в первоначальное состояние через те же промежуточные состояния без каких- либо изменений в окружающей среде.
Необратимые процессы изменения состояния определяются условием
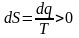 (1.11)
(1.11)
Неравенство (1.11) является математическим выражением второго начала термодинамики, которое характеризует направление протекающих в природе макроскопических процессов. Второе начало термодинамики позволяет установить количественное соотношение между работой, которая могла бы быть совершена системой при обратимом процессе, и действительной работой.
При изучении закономерностей движения газа необходимо учитывать термодинамический процесс изменения состояния газа. При этом различают изотермический, адиабатный, изоэнтропийный, изоэнтальпийный процессы.
Процесс,
происходящий без теплообмена системы
с окружающей средой, называется
адиабатным. Процесс в системе, при
котором сохраняется неизменной энтропия
системы, называется изоэнтропийным.
Изоэнтропийный процесс - это не что иное
как обратимый адиабатный процесс. Он
возможен в энергетически изолированной
системе при отсутствии трения между
частицами газа. При наличии трения между
частицами газа адиабатный процесс будет
неизоэнтропийным. Выделяющееся внутри
системы тепло, обусловленное работой
сил трения приводит к возрастанию
энтропии
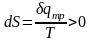 и, конечно, процесс при этом будет
необратимым.
и, конечно, процесс при этом будет
необратимым.
Процесс в системе, характеризуемый постоянством энтальпии, называется изоэнтальпийным.
Энтальпией (теплосодержанием), отнесенной к единице массы, называется функция
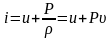 (1.12)
(1.12)
которая определяется только состоянием газа, например, температурой и давлением.
Рассмотрим основные соотношения термодинамических параметров для идеального газа, которые будут использоваться в дальнейшем при изложении курса.
Подведенное
к системе тепло
приведет
к новому состоянию газа с параметрами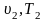 .
Количество подведенного тепла
можно выразить через удельную теплоемкость
газа при постоянном давлении
.
Количество подведенного тепла
можно выразить через удельную теплоемкость
газа при постоянном давлении
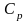

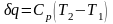 (1.13)
(1.13)
С
другой стороны, согласно первому началу
термодинамики подведенное тепло
идет на изменение внутренней энергии
газа, которое в соответствии с (1.5) равно
 ,
и на выполнение работы расширения газа
,
и на выполнение работы расширения газа
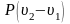 .
Следовательно,
.
Следовательно,
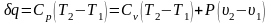 (1.14)
(1.14)
Второе слагаемое в правой части равенства (1.14) можно преобразовать, используя уравнение состояния (1.3), к виду
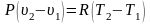 (1.15)
(1.15)
Если
теперь заменить второе слагаемое в
(1.14) по формуле (1.15), то после сокращения
на величину
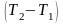 получим
известное в термодинамике выражение
Майера
получим
известное в термодинамике выражение
Майера
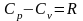 (1.16)
(1.16)
Используя
соотношения (1.3), (1.5) и (1.16), можно получить
иные выражения для энтальпии
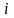 .
В самом деле, из (1.12) имеем
.
В самом деле, из (1.12) имеем
 (1.17)
(1.17)
Последнее выражение предстанет в ином виде, если в нем заменить по формуле (1.3)
 (1.18)
(1.18)
где
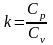 (1.19)
(1.19)
Изменение
энтропии
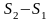 при
переходе идеального газа из состояния
1 в состояние 2 определится интегрированием
(1.10), которое с учетом выражений (1.5) и
(1.3) дает
при
переходе идеального газа из состояния
1 в состояние 2 определится интегрированием
(1.10), которое с учетом выражений (1.5) и
(1.3) дает
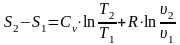
или, если использовать формулу Майера (1.16)
 (1.20)
(1.20)
Используя
(1.20), получается уравнение адиабаты
Пуассона, описывающее изоэнтропийный
(обратимый адиабатный) процесс
изменения состояния газа

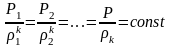 (1.21)
(1.21)
Показатель
степени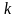 ,
входящий в (1.21) и определяемый формулой
(1.19), называется показателем адиабаты
Пуассона.
,
входящий в (1.21) и определяемый формулой
(1.19), называется показателем адиабаты
Пуассона.
