
- •Визначення залежності швидкості хімічних реакцій від різних умов
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •4.1. Вплив температури на швидкість реакції.
- •4.2. Вплив поверхні зіткнення на швидкість хімічної реакції.
- •4.3. Вплив каталізатора на швидкість хімічної реакції,
- •4.4. Вплив інгібітору на швидкість хімічної реакції.
- •5. Вимоги до звіту
- •6. Техніка безпеки
- •7. Контрольні питання
- •8. Література
- •Вивчення моделі проточного трубчастого реактора
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади і посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Вивчення моделі реактору ідеального змішування
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •2.Хімічні реактиви, прилади, посуд
- •3.Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •Одержання нафтопродуктів прямою перегонкою нафти
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •Визначення густини пікнометром
- •Визначення в 'язкості
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи.
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Дослідження корозії металів
- •1. Теоретичні основи
- •Показники корозії металів
- •2. Хімічні реактиви та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •Отримання їдкого натрію (NаOh) і хлору електрохімічним методом
- •1.Теоретичні основи
- •2.Хімічні реактиви, прилади та посуд
- •3.Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •Одержання сульфату амонію
- •1.Теоретичні основи
- •2.Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •2. Хімічні реактиви, прилади та посуд
- •3. Послідовність виконання роботи
- •3.1 Визначення твердості води
- •3.2 Визначення хлоридів
- •3.3 Визначення масової концентрації двовалентного і тривалентного заліза
- •3.4 Визначення масової концентрації міді
- •3.5 Визначення масової концентрації хрому
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Одержання і дослідження конденсаційних смол (новолочна смола)
- •Теоретичні основи
- •2. Хімічні реактиви та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Очищення хімічних реагентів ( реактивів) методом прямої перегонки
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
2. Хімічні реактиви, прилади та посуд
Реактиви:
сірка - 50 г;
гідроксид натрію NaOH - 20 г;
вата гігроскопічна -10г;
оксид магнію -10 г;
діхлоретан -10г;
соляна кислота - 20 мл;
бензол - 20 мл;
вуглець чотирихлористий - 20 мл;
сірчана кислота - 20 мл;
ацетон - 20 мл;
оцтова кислота -20 мл.
Прилади та посуд:
тришийкова колба;
зворотний холодильник;
мішалка;
реостат;
електричний мотор;
водяна баня;
електроплита;
штатив - 1 шт.;
фарфорова чашка - 3 шт.;
краплинна лійка - 1 шт.;
лійка з коротким носиком - 2 шт.;
колби V = 100 мл - 10 шт.;
термометр - 2 шт.;
ваги технічні.
3. Опис лабораторної установки
На рисунку 11.1 зображено лабораторну установку, яка складається з круглодонної колби 1, водяної бані 2, мотора з мішалкою 3, краплинної лійки 4, зворотного холодильника 5, термометра 6.
Розчин тетрасульфіду заливають у колбу 1, маса підігрівається на водяній бані 2 до температури 70°С. При діючій мішалці з краплинної лійки 4 доливають діхлоретан у присутності диспергатора - оксиду магнію. Одержується тіокол.
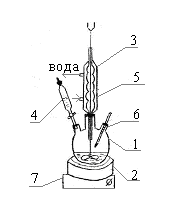
– круглодонна тришийкова колба; 2-водяна баня ; 3- мішалка;
4 - краплинна лійка; 5 - зворотний холодильник; 6 – термометр; 7 - електрична плита
Рисунок 11.1 - Лабораторна установка
4. Послідовність виконання роботи
Перший етап роботи полягає в приготуванні розчину тетрасульфіду натрію Na2S4. Він утворюється при нагріванні сірки з концентрованим розчином їдкого натру
6 NaOH + 10 S 2 Na2S4 + З Н2О + Na2S2O3 (11.5)
Для цього приблизно 48-52 см заздалегідь підігрітої води швидко доводять до кипіння в фарфоровій чашці і потім обережно додають 15,5 г їдкого натру. В одержаний розчин порціями додають раніше розраховану кількість сірки, помішуючи вміст чашки до повного розчинення. Утворений прозорий розчин бурого кольору після охолодження до 30-40°С фільтрують через гігроскопічну вату, поміщену в лійку з коротким носиком. Профільтрований розчин заливають в тришийкову крутлодонну колбу 1 і на водяній бані нагрівають до 70°С.
Після досягнення вказаної температури в колбу через один з отворів вводять як диспергатор оксид магнію (2% від усієї реагуючої маси, їдкий натр + сірка) і далі при ретельному перемішуванні мішалкою 3 додають
10 см3 дихлоретан ( температура його кипіння - 82-84°С). Подачу здійснюють з швидкістю 8-10 крапель на хвилину при температурі близько 70°С (якщо потрібно, в водяну баню додають холодну воду, але потім, в кінці реакції, її знову підігрівають).
Після закінчення процесу весь вміст колби виливають у чисту фарфорову чашку, промивають теплою водою (температура 40-50°С), 2-3% розчином соляної кислоти об'ємом 20 см3 (до нейтральної реакції за лакмусом) і потім знову (3-4 рази) теплою водою. Тіокол висушують при температурі 18-20°С і за зваженою масою визначають його вихід.
Далі одержаний тіокол випробовують на стійкість різними розчинниками.
Для цього під тягою до пробірки з 1-2 cmj розчинника вносять 0,2 г тіоколу і спостерігають його стійкість,відмічаючи через 15-20 хв. в таблиці "++" - якщо розчиняється, "+" - якщо набухає, "-" - якщо не змінюється. Для досліду беруть такі розчинники:
чотирихлористий вуглець;
ацетон;
оцтову кислоту;
розчин сірчаної кислоти 5, 10, 20%;
розчин соляної кислоти 5,10, 20%;
розчин їдкого натру 5%. Одержані дані заносять в таблицю.
