
- •Глава 14 патофизиология сердечно-сосудистой системы
- •Глава 14 / патофизиология сердечно-сосудистой системы
- •Часть III. Патофизиология органов и систем
- •Глава 14 / патофизиология сердечно-сосудистой системы
- •Часть III. Патофизиология органов и систем
- •Глава 14 / патофизиология сердечно-сосудистой системы
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 15 патофизиология дыхания
- •15.1. Патофизиология внешнего дыхания
- •15.1.1. Недостаточность внешнего дыхания
- •Часть III. Патофизиология органов и систем
- •15.1.6. Изменение газового состава окружающего воздуха
- •15.2. Нарушение внутреннего
- •15.2.1. Транспорт кислорода и его нарушения
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 15 / патофизиология дыхания
Глава 15 патофизиология дыхания
Дыхание - это совокупность процессов, обеспечивающих аэробное окисление в организме, в результате которого освобождается энергия, необходимая для жизни. Оно поддерживается функционированием нескольких систем: 1) аппарата внешнего дыхания; 2) системы транспорта газов; 3) тканевого дыхания. Система транспорта газов, в свою очередь, подразделяется на две подсистемы: сердечно-сосудистую и систему крови. Деятельность этих систем тесно связана сложными регуляторными механизмами. Поэтому патологический процесс в любом из звеньев указанной системы может быть причиной общего или регионарного нарушения дыхания. Например, при патологии сердечно-сосудистой системы говорят о сердечной или сосудистой недостаточности, в описание которой входят и изменения аппарата внешнего дыхания, и нарушения тканевого дыхания (гипоксии). Другой пример - гипоксия мозга самого различного происхождения может привести к нарушениям регуляции дыхания, в том числе и к фатальным.
Собственно термин «дыхательная недостаточность» принято использовать при характеристике нарушений функции аппарата внешнего дыхания, хотя это некорректно с позиции системного анализа патологических явлений в целом организме. Поэтому нарушения функции аппарата внешнего дыхания правильнее называть недостаточностью внешнего дыхания.
15.1. Патофизиология внешнего дыхания
Внешнее дыхание - это совокупность процессов, совершающихся в легких и обеспечивающих нормальный газовый состав артериальной крови. Следует подчеркнуть, что в данном случае речь идет только об артериальной крови, так как газовый состав венозной крови зависит от состояния тканевого дыхания и транспорта газов в организме. Внешнее дыхание обеспечивается аппаратом внешнего дыхания, т.е. системой легкие - грудная клетка с дыхательной мускулатурой и системой регуляции дыхания.
Нормальный газовый состав артериальной крови поддерживается следующими взаимно связанными процессами: 1) вентиляцией легких; 2) диффузией газов через альвеолярно-капилляр-ные мембраны; 3) кровотоком в легких; 4) регуляторными механизмами. При нарушении любого из этих процессов развивается недостаточность внешнего дыхания.
15.1.1. Недостаточность внешнего дыхания
Недостаточность внешнего дыхания - патологическое состояние, развивающееся вследствие нарушения внешнего дыхания, при котором не обеспечивается нормальный газовый состав артериальной крови или он достигается в результате компенсаторных механизмов, приводящих к ограничению резервных возможностей организма. Недостаточность внешнего дыхания может возникнуть и у практически здорового человека при изменении газового состава вдыхаемого воздуха.
Существует много классификаций недостаточности внешнего дыхания. Большинство классификаций создано для диагностики функциональных нарушений при заболеваниях системы дыхания. Однако недостаточность внешнего дыхания может развиваться при заболеваниях не только системы дыхания, но и системы кровообращения, пищеварения, гепатобилиарной системы, центральной нервной системы и т.д. Поэтому требуется классификация, учитывающая возможность патологических изменений внешнего дыхания при любой форме патологии.
При классифицировании недостаточности внешнего дыхания нужно прежде всего учитывать темпы ее развития. Для этого применяется термин «форма недостаточности внешнего дыхания»: острая, подострая и хроническая. Далее целесообразно классифицировать поражение основных функциональных звеньев аппарата внешнего дыхания. Здесь удобно использовать термин «вид недостаточности внешнего дыхания». Наконец, недостаточность внешнего дыхания необходимо классифицировать по глубине функциональных нарушений и выделять со-
503
ответственно стадии, или функциональные классы.
Формы недостаточности внешнего дыхания.
Острая недостаточность внешнего дыхания развивается в течение минут, часов. Примером острой недостаточности внешнего дыхания может быть быстро развивающийся приступ удушья при бронхиальной астме, сердечной астме, при острой пневмонии.
Подострая недостаточность внешнего дыхания развивается в течение суток, недели и может быть рассмотрена на примере гидроторакса, накопления различной природы жидкости в плевральной полости (недели).
Хроническая недостаточность внешнего дыхания развивается месяцы и годы, например при хронической обструктивной эмфиземе легких, диссеминированных легочных фиброзах. Следует отметить, что патологические изменения при хронической недостаточности внешнего дыхания, как правило, необратимы. Однако практически всегда под влиянием лечения происходит существенное улучшение функциональных параметров. При острой и подострой недостаточности внешнего дыхания возможно полное восстановление нарушенных функций.
Виды недостаточности внешнего дыхания определяются по основным функциональным звеньям аппарата внешнего дыхания, где выявляются патологические изменения:
нарушения вентиляции легких;
нарушения диффузии газов через альвео-лярно-капиллярные мембраны;
нарушения легочного кровотока;
нарушения регуляции дыхания;
изменения газового состава окружающего воздуха.
Виды недостаточности внешнего дыхания можно диагностировать, используя клинические методы обследования (опрос, осмотр, физические методы исследования), а также параклинические методы обследования (газы артериальной крови, показатели вентиляционной функции, диффузионная емкость легких, соотношения вентиляция - кровоток и др.). 1-4-й виды недостаточности внешнего дыхания редко бывают относительно изолированными. Чаще всего имеются изменения, характерные для всех видов, однако диагноз ставится по преобладанию одного из них. Например, при хронической обструктивной эмфиземе легких преобладает 1-й вид, но име-
ются и нарушения диффузионной способности мембран, и нарушения кровотока в легких, и нарушения регуляции дыхания.
Глубина функциональных нарушений внешнего дыхания
Острую недостаточность внешнего дыхания обычно называют острой дыхательной недостаточностью и по выраженности гипоксемии различают три степени ее тяжести: 1-я степень (умеренная) - ра02 > 70 мм рт. ст.; 2-я степень (средняя) - ра02 = 70-50 мм рт. ст.; 3-я степень (тяжелая) - ра0г < 50 мм рт. ст. В то же время необходимо учитывать, что хотя степень выраженности недостаточности внешнего дыхания определяется гипоксемией, гипервентиляция или гиповентиляция альвеол может вносить существенные коррективы в лечебную тактику. Например, при тяжелой пневмонии возможна ги-поксемия 3-й степени. Если при этом Р„С02 нормальное, показано лечение вдыханием чистого кислорода. При понижении РаС02 назначается газовая смесь кислорода и углекислого газа. Другой пример - астматический статус, картина «немого легкого» в результате тотальной обструкции бронхов, гиперкапния (раС02 более 70 мм рт.ст.). Патогенетически обоснованная тактика в данной ситуации - лаваж бронхов (промывание с помощью специального фибробронхоско-па).
Если при острой недостаточности внешнего дыхания для определения глубины функциональных нарушений достаточно исследовать газы крови, то при подострой и хронической формах недостаточности внешнего дыхания необходимо исследовать по крайней мере функциональные показатели, отражающие состояние вентиляционной функции легких и газовый состав артериальной крови.
Стадии, или функциональные классы, недостаточности внешнего дыхания определяются только по степени отклонения функциональных параметров от нормы. Выделяют:
компенсированную недостаточность, когда нет гипоксемии, но определяются различные варианты и степени обструктивных, рестриктив-ных и смешанных нарушений вентиляционной функции легких;
субкомпенсированную недостаточность, когда имеет место гипоксемия (НЬО, менее 93%).
504
При этом функциональном классе она может быть умеренная (92-86%) и выраженная (85-75%). Показатели вентиляционной функции легких могут быть нормальными, если гипоксе-мия обусловлена нарушениями диффузии или кровотока в легких. При заболеваниях бронхо-легочной системы могут определяться различные степени обструктивных, рестриктивных и смешанных нарушений вентиляционной функции. При этом могут быть также нарушения диффузионной способности легких и легочного кровотока (в зависимости от вида недостаточности внешнего дыхания);
3) декомпенсированную недостаточность, когда определяется тяжелая гипоксемия (НЬ02 менее 75%), гипоксемия с гиперкапнией или тяжелая гипоксемия с гипокапнией.
Нарушение функции внешнего дыхания клинически выявляется симптомами одышки (см. разд. 15.1.5) и цианозом.
15.1.2. Нарушение вентиляции легких
Различают обструктивные, рестриктивные и смешанные нарушения вентиляционной функции легких.
Обструктивные (от лат. obstructio - препятствие) нарушения вентиляции легких. В основе обструктивных нарушений вентиляции легких лежит сужение суммарного просвета бронхов в результате: 1) повышения тонуса гладкой мускулатуры бронхов (бронхоспазм); 2) отека слизистой бронхов (он может быть воспалительным, аллергическим, застойным); 3) гиперсекреции слизи бронхиальными железами. При этом имеет значение не только гиперкри-ния, но в большей степени дискриния, повышение вязкости секрета, который может закупоривать бронхи и обусловливать синдром тотальной бронхиальной обструкции; 4) рубцовой деформации бронхов (сужения и расширения просвета бронхов, увеличивающих аэродинамическое сопротивление); 5) клапанной обструкции бронхов. Сюда же нужно отнести трахеобронхиаль-ную дискинезию, т.е. экспираторный коллапс трахеи и главных бронхов, связанный с неполноценностью структур дыхательных путей, в особенности мембранозной части.
Обструктивные нарушения вентиляции легких характерны для бронхообструктивного син-
дрома, который является основным при бронхиальной астме и при обструктивном бронхите. Кроме того, он может быть у больных с системными заболеваниями соединительной ткани (дис-семинированная красная волчанка, узелковый периартериит), при аллергических заболеваниях, гриппе. Застойное набухание слизистой бронхов возникает при недостаточности левых отделов сердца (острой и хронической) и создает обструкцию бронхов. Раздражение слизистой бронхов при этом может дополнительно вызвать бронхоспазм и усилить выраженность обструк-тивного компонента, что значительно затрудняет дифференциальную диагностику между бронхиальной и сердечной астмой. Рубцовая деформация бронхов характерна для хронического бронхита и приводит к фиксированному нарушению бронхиальной проходимости. Значение сужения просвета бронхов в нарушении механики дыхания доказывается физическим законом Пуазейля, согласно которому бронхиальное сопротивление возрастает пропорционально квадрату скорости воздушной струи и четвертой степени уменьшения радиуса.
Клапанная обструкция бронхов характерна для хронической обструктивной эмфиземы лёгких. Сущность ее заключается в следующем. На вдохе отрицательное внутригрудное давление передается к поверхности легких, к альвеолярным структурам и к внелегочным дыхательным путям (главные бронхи и часть трахеи, расположенная в грудной полости). При вдохе давление в бронхе ниже атмосферного. В альвеолах давление еще меньше, чем в бронхе, что обеспечивает движение воздуха по направлению к альвеолам. В структурах легких, окружающих бронх, давление ниже, поэтому оно способствует расширению бронхов. При выдохе соотношение давлений меняется. Внутригрудное давление повышается, а в альвеолах оно становится положительным в результате ретракции легких. Давление в бронхах ниже, чем в альвеолах, и оно уменьшается по направлению к трахее. Это связано с увеличением скорости потока воздуха в крупных бронхах по сравнению с мелкими, так как с увеличением скорости потока воздуха уменьшается статическое и увеличивается динамическое давление в бронхе. Увеличение же скорости потока воздуха объясняется тем, что суммарный просвет мелких бронхов много больше, чем крупных. Падение статического дав-
505
ления в бронхах способствует их компрессии окружающими структурами легочной паренхимы, где давление выше.
Расширение бронхов на вдохе и сжатие на выдохе действуют подобно клапану и в нормальных условиях, однако значительному сужению бронхов противодействует эластическое напряжение легких.
При хронической обструктивной эмфиземе легких эластическое напряжение последних резко снижено, поэтому даже мелкие бронхи на выдохе подвержены значительному экспираторному сужению, что называют воздушной ловушкой.
Считается, что клапанная обструкция является основным механизмом развития и острой эмфиземы легких, возникающей при бронхоспа-стическом синдроме. Клапанная обструкция при этом усиливается в результате сужения просвета бронхов и увеличения амплитуды дыхательных колебаний внутригрудного давления. При хроническом бронхите происходит деформация бронхов. Места их регионарных сужений также становятся предрасположенными к проявлению клапанной обструкции, что в конечном счете приводит к неравномерности вентиляции различных участков легких и к различной степени выраженности эмфиземы легких.
Значение регионарного сужения бронхов в механизме клапанной обструкции можно пояснить с помощью физических закономерностей. Допустим, что по трубке, имеющей регионарное сужение просвета, протекает жидкость с определенной объемной скоростью. В широком отрезке трубки поток жидкости оказывает определенное статическое давление на стенки трубки и динамическое давление, обеспечивающее ее поток. В узкой части трубки увеличивается скорость потока, возрастает динамическое давление за счет снижения статического (уравнение Берну лл и). При переходе жидкости в участок трубки с прежним диаметром просвета скорость ее восстанавливается, снижается динамическое давление и повышается до прежних значений статическое давление. Таким же образом в суженном участке бронха снижается статическое давление, и он в большей степени подвергается сжатию во время фазы выдоха.
Рестриктивные (от лат. restrictio - ограничение) нарушения вентиляции легких. В основе рестриктивных нарушений вентиляции легких лежит ограничение их расправления в резуль-
тате действия внутрилегочных и внелегочных причин.
Внутрилегочными причинами рестриктивных нарушений вентиляции легких являются: 1) диффузные фиброзы различного происхождения (альвеолиты, грануломатозы, гематогенно-диссеминированный туберкулез легких, пневмо-кониозы, коллагенозы и др.); 2) отек легких различного генеза (воспалительный, застойный, токсический; в свою очередь, отек может быть альвеолярный и интерстициальный); 3) повышение давления в сосудах малого круга кровообращения; 4) очаговые изменения в легких (доброкачественные и злокачественные опухоли, ателектазы различного происхождения, кисты, инфильтраты различной природы).
К внелегочным причинам рестриктивных нарушений вентиляции легких относятся: 1) изменения в плевре и средостении (экссудативные плевриты, пневмоторакс, плевральные нашвар-тования, опухоли плевры и средостения, увеличение сердца); 2) изменения грудной клетки и дыхательной мускулатуры (деформация грудной клетки, окостенение реберных хрящей, ограничение подвижности позвоночника, реберных суставов, поражение диафрагмы и других дыхательных мышц, в том числе при поражении нервной системы, ожирение, истощение и др.); 3) изменения органов брюшной полости (увеличение печени, метеоризм, асцит, воспалительные заболевания органов брюшной полости и др.).
Смешанные нарушения вентиляции легких. Чисто обструктивные и рестриктивные нарушения вентиляции легких возможны лишь теоретически. Практически всегда имеется определенная комбинация обоих видов нарушения вентиляции.
Поражение плевры
Поражения плевры приводят к развитию рестриктивных нарушений вентиляции легких вследствие следующих причин: 1) болей в грудной клетке; 2) гидроторакса; 3) гемоторакса; 4) пневмоторакса; 5) плевральных шварт.
Под влиянием боли происходит ограничение дыхательной экскурсии грудной клетки. Боли возникают при воспалении плевры (плеврит), опухолях, ранениях, травмах, при межреберной невралгии и др.
Гидроторакс - жидкость в плевральной полости, вызывающая компрессию легкого, ограничение его расправления (компрессионный ате-
506
лектаз). При экссудативном плеврите в плевральной полости определяется экссудат, при легочных нагноениях, пневмониях экссудат может быть гнойным; при недостаточности правых отделов сердца в плевральной полости накапливается транссудат. Транссудат в плевральной полости может обнаруживаться также при отечном синдроме различной природы.
Гемоторакс - кровь в плевральной полости. Это может быть при ранениях грудной клетки, опухолях плевры (первичных и метастатических). При поражениях грудного протока в плевральной полости определяется хилез-ная жидкость (содержит липоидные вещества и по внешнему виду напоминает молоко). В ряде случаев в плевре может накапливаться так называемая псевдохилезная жидкость - мутная белесоватая жидкость, не содержащая липоид-ных веществ. Природа этой жидкости неизвестна.
Пневмоторакс - газ в плевральной области. Различают спонтанный, травматический и лечебный пневмоторакс. Спонтанный пневмоторакс возникает внезапно. Первичный спонтанный пневмоторакс может развиваться у практически здорового человека при физическом напряжении или в покое. Причины этого вида пневмоторакса не всегда ясны. Чаще всего он обусловлен разрывом мелких субплевральных кист. Вторичный спонтанный пневмоторакс развивается тоже внезапно у больных на фоне обструктивных и необструктивных заболеваний легких и связан с распадом легочной ткани (туберкулез, рак легких, саркоидоз, инфаркт легких, кистозная гипоплазия легких и др.). Травматический пневмоторакс связан с нарушением целостности грудной стенки и плевры, ранением легкого. Лечебный пневмоторакс в последние годы используется редко. При попадании воздуха в плевральную полость развивается ателектаз легких, выраженный тем больше, чем больше газа находится в плевральной полости.
Пневмоторакс может быть ограниченным, если в плевральной полости имеются сращения висцерального и париетального листков плевры в результате перенесенного воспалительного процесса. Если воздух в плевральную полость поступает без ограничения, происходит полный коллапс легкого. Двухсторонний пневмоторакс имеет очень неблагоприятный прогноз. Если доступ воздуха в полости ничем не ограничен, возникает полный коллапс левого и право-
го легкого, что является, безусловно, смертельным патологическим состоянием. Однако и частичный пневмоторакс имеет серьезный прогноз, так как при этом нарушается не только дыхательная функция легких, но также функция сердца и сосудов. Пневмоторакс может быть клапанным, когда на вдохе воздух попадает в плевральную полость, а во время выдоха патологическое отверстие закрывается. Давление в плевральной полости становится положительным, и оно нарастает, сдавливая функционирующее легкое и нарушая более значительно функцию сердца и сосудов. В таких случаях нарушения вентиляции легких и кровообращения быстро нарастают и могут привести к гибели пациента, если ему не будет оказана квалифицированная помощь.
Состояние, когда в плевральной полости находятся и жидкость и газ, называют гидропневмотораксом. Это бывает при прорыве абсцесса легких в бронх и плевральную полость.
Плевральные шварты являются следствием воспалительного поражения плевры. Выраженность нашвартований может быть различной: от умеренной до так называемого панцирного легкого.
Показатели, характеризующие состояние вентиляции легких
Функциональные показатели, с помощью которых оценивается состояние вентиляционной функции легких, можно разделить на три группы: 1) статические легочные объемы и емкости; 2) показатели, отражающие изменение объема легких в единицу времени, т.е. воздушный поток; 3) показатели механики дыхания, когда рассматриваются не только легочные объемы, емкости и показатели воздушного потока, но и давление, обеспечивающее соответствующий объем легких или поток воздуха. Показатели первой и второй групп рассматриваются в системе BTPS (газ при температуре тела (37"С), окружающем давлении и насыщении водяными парами). Фактические величины соответствующих показателей необходимо сравнивать с должными величинами (табл. 73).
В настоящее время разработаны нормативы для этих показателей, они унифицированы и заложены в программы современных приборов, снабженных компьютерной обработкой результатов измерений. Снижение показателей на 15%
507
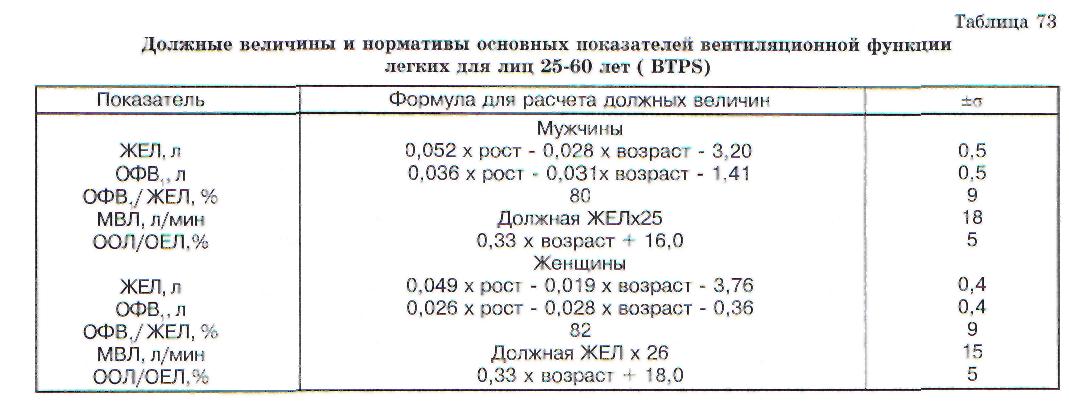
Изменения статических объемов и емкостей легких при патологии. Дыхательный объем (ДО) обычно составляет 0,5 л. Он уменьшается при рестриктивных формах патологии и может увеличиваться при обструктивных нарушениях вентиляции легких. На начальных стадиях об-структивной эмфиземы легких ДО смещается в сторону резервного объема вдоха (РОвд), который уменьшается, а резервный объем выдоха (РОвыд) - увеличивается. Это происходит в результате снижения эластического напряжения легких и преобладания эластического напряжения грудной клетки. В инспираторном положении устанавливается равновесие между силами эластического напряжения легких и грудной
клетки. Остаточный объем легких (UUJi) и жизненная емкость легких (ЖЕЛ) первое время остаются нормальными.
Таким образом, увеличение функциональной остаточной емкости легких (ФОЕ), состоящей из нормального ООЛ и увеличенного РО,1Ь|Д, является ранним признаком эмфиземы легких. Снижение эластического напряжения легких способствует дальнейшему смещению ДО в сторону РОвд и увеличению ООЛ. При этом происходит увеличение общей емкости легких (ОЕЛ) за счет увеличения ООЛ. По мере присоединения рестриктивных нарушений (окостенение реберных хрящей, пневмофиброз) ЖЕЛ снижается, а ООЛ увеличивается еще больше. Особенно отчетливо повышается отношение ООЛ/ОЕЛ (%). Увеличение ООЛ обусловлено снижением силы ретракции легких, экспираторным коллапсом дыхательных путей и ригидностью грудной клетки, а также повышением инспираторного тонуса дыхательной мускулатуры.
Таким образом, при резко выраженной об-структивной эмфиземе легких имеют место и рестриктивные изменения (рис. 149). Считается, что при острой эмфиземе легких, которая развивается при бронхообструктивном синдроме, происходит улавливание воздуха на выдохе в связи с действием клапанного механизма обструкции. Однако механизм острого, обратимого вздутия легких гораздо сложнее, поскольку при нем возможно обратимое и понижение, и повышение эластической способности легких.
При рестриктивных нарушениях вентиляции легких уменьшаются ОЕЛ и ЖЕЛ. Снижение ООЛ наблюдается редко. Даже при выраженном
508
з астое
в легких при острой пневмонии,
пневмо-фиброзе ООЛ остается либо
нормальным, либо немного повышенным.
При этом, как правило, повышается
отношение ООЛ/ОЕЛ за счет снижения
ОЕЛ. Поддержание относительно нормального
ООЛ при патологии рассматривается как
защитная реакция в системе аппарата
внешнего дыхания, направленная на
поддержание постоянного состава
газа в респираторной зоне. При снижении
ООЛ усиливаются изменения напряжения
кислорода в респираторной зоне от вдоха
к выдоху. Снижение ЖЕ Л и ОЕЛ характерно
для рестриктивных изменений вентиляции
легких.
астое
в легких при острой пневмонии,
пневмо-фиброзе ООЛ остается либо
нормальным, либо немного повышенным.
При этом, как правило, повышается
отношение ООЛ/ОЕЛ за счет снижения
ОЕЛ. Поддержание относительно нормального
ООЛ при патологии рассматривается как
защитная реакция в системе аппарата
внешнего дыхания, направленная на
поддержание постоянного состава
газа в респираторной зоне. При снижении
ООЛ усиливаются изменения напряжения
кислорода в респираторной зоне от вдоха
к выдоху. Снижение ЖЕ Л и ОЕЛ характерно
для рестриктивных изменений вентиляции
легких.
Изменение показателей, характеризующих воздушный поток при патологии. Минутный объем дыхания (МОД) в нормальных условиях варьирует от 6 до 10 л/мин. Сравнение с должной величиной МОД можно проводить лишь в тех случаях, когда он определяется в условиях основного обмена (исследование проводится утром и натощак в клиностатическом положении пациента). Должная величина МОД равна должному поглощению кислорода, деленному на 40 (40 мл кислорода поглощается из 1 л вдыхаемого воздуха). МОД повышается при тиреотоксикозе, анемии, сердечной недостаточности, об-структивных нарушениях вентиляции легких, лихорадке. Повышение МОД направлено на обеспечение увеличения затраты кислорода. При тиреотоксикозе и лихорадке основной обмен повышен в целом организме, при сердечной недостаточности увеличивается затрата кислорода на работу сердечной мышцы и дыхательных мышц. При затруднении вентиляции легких повышается затрата кислорода на работу дыхательных мышц.
Принцип использования показателей бронхиальной проходимости для диагностики ее нарушения основан на том, что воздушный поток через суженные бронхи резко уменьшается и требуется больше времени, чтобы обеспечить такой же объем вентиляции, как и при нормальном просвете бронхов. Максимальная вентиляция легких (МВЛ) - это объем воздуха, который можно провентилировать в легких при максимальном произвольном усилении работы дыхательной мускулатуры. Исследуемому предлагается подышать в регистрирующий прибор (спирограф, пневмотахограф) как можно чаще и глубже 5-6 раз. Полученный при этом объем перерассчитывается на 1 мин. Чем меньше просвет
бронхов, тем меньше будет величина МВЛ по сравнению с должной.
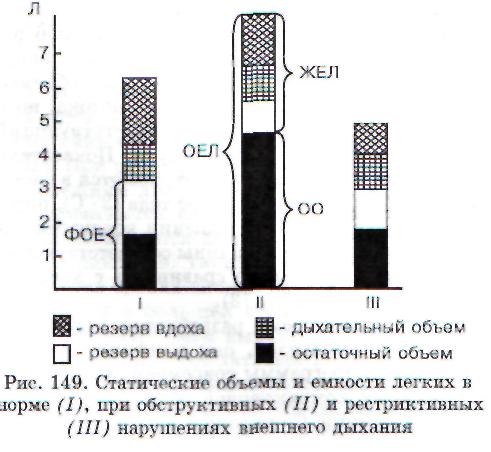
В практике функциональной диагностики чаще всего используются показатели форсированного выдоха. Исследуемому предлагают сделать глубокий вдох, задержать дыхание на некоторое время и далее сделать как можно более полный и быстрый выдох. Через суженные бронхи поток воздуха будет снижен. При этом рассчитываются следующие показатели: объем форсированного выдоха за первую секунду (ОФВ^, отношение ОФВ( к ЖЕЛ в процентах, или ФЖЕЛ,, или тест Тиффно (ТТ), а также петля поток/объем. Этот показатель получают при регистрации на взаимно перпендикуляторных осях изменения потока воздуха в литрах за 1 с (л/с) и объема выдыхаемого воздуха (ЖЕЛ) при форсированном выдохе (рис. 150). Пик объемной скорости (ПОС) достигается в первом объеме выдыхаемого воздуха (5-10%). Далее измеряют максимальную объемную скорость (МОС) потока на уровне 25% ЖЕЛ от начала выдоха (МОС25), на уровне 50% ЖЕЛ (МОС50) и на уровне 75% ЖЕЛ (МОС75) . Начальные отделы петли поток/объем отражают усилие исследуемого, которое он развивает при форсированном выдохе. ПОС и МОС25 снижаются при обструкции крупных дыхательных путей, МОС50 и МОС75 - при обструкции мелких бронхов.
Изменения показателей механики дыхания при патологии. Для измерения показателей механики дыхания необходимо одновременно регистрировать дыхательные колебания транспуль-монального давления и объема легких. Транс-
509
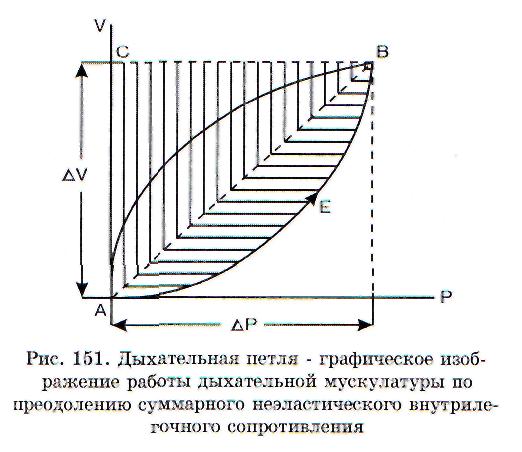
Вторая часть петли соответствует работе по преодолению неэластического сопротивления на выдохе. Неэластическое сопротивление включает три вида сопротивления: 1) аэродинамическое (бронхиальное); 2) тканевое трение; 3) инерцию газа и тканей. Последними двумя видами неэластического сопротивления обычно пренебрегают как малыми, и неэластическое сопротив-
ление рассматривают как аэродинамическое. Площадь треугольника ABC соответствует работе по преодолению эластического сопротивления легких, а площадь всей фигуры АЕВС составляет общую работу дыхания, т.е. затрату работы дыхательной мускулатуры по преодолению суммарного внутрилегочного сопротивления. На вдохе дыхательная мускулатура преодолевает неэластическое сопротивление легких (АЕВ) и эластическое сопротивление (ABC). Выдох происходит за счет запаса потенциальной энергии, полученной на вдохе благодаря напряжению эластической структуры легких. Таким образом, выдох происходит пассивно. Запас эластического напряжения легких частично тратится на преодоление неэластического сопротивления легких на выдохе (часть дыхательной петли внутри треугольника ABC). Остальная часть эластического запаса нейтрализуется постепенным снижением инспираторного тонуса дыхательной мускулатуры. Термины «работа дыхания», «неэластическая», «эластическая фракции работы дыхания» являются общепринятыми.
Отношение объема легких (АС) к величине давления Р называют динамической растяжимостью легких. Она показывает, насколько изменится объем легких, если транспульмональ-ное давление понизится на 1 см вод. ст. Растяжимость легких измеряется в литрах на 1 см водного столба (л/см вод. ст.).
Общая работа дыхания у здоровых людей составляет 0,23+0,06 кгм/мин. При обструктивных нарушениях вентиляции легких она увеличивается до 1 кгм/мин и более за счет увеличения неэластической фракции. Увеличивается площадь дыхательной петли и часть ее, которая располагается выше линии АС и соответствует активной работе дыхательной мускулатуры на выдохе по преодолению повышенного неэластического сопротивления. Отношение эластической фракции работы дыхания к общей работе дыхания уменьшается с 60 до 30%. При рестриктив-ных нарушениях вентиляции легких увеличение общей работы дыхания выражено меньше и происходит оно за счет увеличения эластической фракции работы дыхания. Растяжимость легких снижается и становится менее 0,175 л/см вод. ст., а отношение эластической фракции работы к общей работе дыхания возрастает до 80-95%.
Бронхиальное сопротивление (RaJ определяется по величине альвеолярного давления
510
(см вод. ст.), необходимого для обеспечения потока воздуха, равного 1 л/с. Нормальная величина Дцц| составляет 1,5-2,5 см вод. ст./л/с. При обструктивных нарушениях вентиляции легких бронхиальное сопротивление увеличивается в 10 раз и более, при рестриктивных нарушениях оно увеличивается в меньшей степени и обычно связывается с сопутствующими явлениями обструкции бронхов.
Эластические свойства легких оценивают по статической растяжимости, которая определяется по изменению объема легких и транспульмональ-ного давления на медленном глубоком вдохе. При рестриктивных формах патологии легких она снижается и составляет менее 0,1 л/см вод. ст. Однако это наблюдается не всегда.
Коэффициент эластичности легких (CR) представляет собой отношение величины статического транспульмонального давления, измеренного на высоте резервного вдоха, к ОЕЛ. У здоровых людей этот показатель варьирует в очень широких пределах (от 2 до 8 см вод. ст./л), поэтому значение эластического сопротивления легких в механике дыхательных движений в нормальных условиях и при патологии остается во многом неясным.
Диагностика обструктивных и рестриктивных нарушений вентиляции легких. Значение диагностики обструктивного, рестриктивного и смешанного типов нарушения вентиляции легких не следует преувеличивать, так как это диагностика всего лишь типов нарушения вентиляции, и не всегда можно с достоверностью судить о механизмах соответствующих нарушений без специальных исследований механики дыхания, проведения фармакологических проб, с помощью которых можно судить еще и об обратимости функциональных нарушений. Следует, наконец, помнить, что функциональная диагностика невозможна без учета клинической картины.
Обструктивные нарушения вентиляции легких характеризуются снижением МВЛ и родственных показателей при нормальной ЖЕ Л. По степени снижения МВЛ можно различать умеренные (на 16-35%), выраженные (на 36-55%) и резко выраженные (более чем на 55%) нарушения вентиляции обструктивного типа. Другие показатели обструктивных нарушений вентиляции легких изменяются аналогично, но разграничить их по степеням затруднительно. Показатели петли поток/объем являются весьма чув-
ствительными в отношении раннего выявления обструктивных нарушений вентиляции легких, при этом они позволяют дифференцировать уровень бронхиального дерева с более выраженной обструкцией: крупные бронхи - преимущественное снижение ПОС и МОС,5; мелкие бронхи -преимущественное снижение MOCw и МОС?5.
К признакам рестриктивных нарушений относится снижение ЖЕЛ, ОЕЛ, растяжимости легких. ЖЕЛ - показатель, наиболее доступный для исследования и лучше других характеризующий пределы расправления и спадения легких. Показатели проходимости бронхов при рестриктивных нарушениях вентиляции легких могут оставаться нормальными, но практически они всегда снижаются параллельно снижению ЖЕЛ. Это можно пояснить на примере уменьшения ЖЕЛ и МВЛ. Напомним, что МВЛ - это объем воздуха, который можно провентилировать в легких при максимальном усилении дыхательных движений. Наиболее эффективная частота дыхания при этом составляет 60 в 1 мин, наиболее эффективным является объем, равный половине ЖЕЛ. У здоровых, хорошо тренированных людей дыхательный объем при выполнении МВЛ может приближаться к ЖЕЛ. При исследовании из 5-6 зарегистрированных дыхательных движений устанавливают наиболее эффективный дыхательный цикл и по нему рассчитывают объем вентиляции легких за минуту (МВЛ), который будет отражать потенциальные возможности вентиляционной функции легких. Например, при ЖЕЛ, равной 4 л, составляющей 100% к должной величине, обследуемый здоровый субъект для МВД использует 2 л и при частоте 60 дыхательных движений в 1 мин получит минутный объем, равный 120 л/мин. Это соответствует нормальной величине МВЛ (100% для условного субъекта). Если же у субъекта ЖЕЛ будет составлять всего 2 л, или 50% от должной величины ЖЕЛ, то при тех же условиях проходимости бронхов для получения МВЛ обследуемый будет использовать половину ЖЕЛ, т.е. 1 л, и МВЛ будет составлять 60 л/мин - 50% от должной величины МВЛ. Таким образом, можно сформулировать принцип диагностики рестриктивных нарушений вентиляции легких: это либо изолированное снижение ЖЕЛ, либо параллельное снижение ЖЕЛ и МВЛ на 16-35% (1-я степень), на 36-55% (2-я степень) и более чем на 55% (3-я степень).
Нарушения вентиляции легких можно назы-
511
вать смешанными в тех случаях, когда снижение показателей, характеризующих проходимость бронхов, выражено в большей степени, чем снижение ЖЕЛ. Например, при снижении ЖЕЛ 1-й степени МВЛ снижена до 2-й или 3-й степени; при снижении ЖЕЛ 2-й степени снижение МВЛ соответствует 3-й степени.
Альвеолярная вентиляция
Минутный объем дыхания, в нормальных условиях составляющий 6-8 л/мин, при патологии может увеличиваться и уменьшаться, способствуя развитию альвеолярной гипервентиляции либо гиповентиляции, которые определяют соответствующие клинические синдромы. Однако по величине МОД нельзя судить о состоянии альвеолярной вентиляции без исследования газового состава альвеолярного воздуха. Тем не менее показатели глубины дыхания - ДО и частота дыхания - могут давать важные сведения об условиях вентиляции альвеол. Например, при поверхностном и частом дыхании увеличивается вентиляция мертвого пространства, которое в нормальных условиях составляет в среднем 150 мл. Так, одинаковый МОД, равный 8 л/мин, может быть у пациента при глубине дыхания 500 мл с частотой 16 дыхательных движений в 1 мин и у пациента при глубине дыхания 250 мл с частотой дыхательных движений 32 в 1 мин. Вентиляция мертвого пространства в первом случае составляет 150 мл • 16 = 2,4 л/мин, а альвеолярная вентиляция - 5,6 л/мин. Во втором случае вентиляция мертвого пространства возрастает до 4,8 л/мин, а альвеолярная вентиляция уменьшается до 3,2 л/мин. Такая ситуация характерна для рестриктивных нарушений вентиляции легких, например при острой пневмонии, отеке легких.
В рассмотренном примере учитывалась величина анатомического мертвого пространства, которое включает в себя объем дыхательных путей, где не происходит газообмена между воздухом и кровью (кондуктивная зона дыхательного тракта, включающая рот, нос, глотку, гортань, трахею, бронхи и бронхиолы). Кроме анатомического, существует и физиологическое мертвое пространство (ФМП), которое дополнительно к анатомическому включает часть респираторной зоны, где нет достаточного кровотока. У здоровых людей анатомическое и физиологическое мертвые пространства практически
одинаковы. При патологии физиологическое мертвое пространство увеличивается, иногда значительно. Оно исследуется по формуле Бора:
р„со2 - Ресо2
фмп = довыл ,
расо2
где ДОвыд - объем воздуха за один цикл; р„С02 -парциальное давление С02 в артериальной крови, которое принимается за альвеолярное; РЕС02 - парциальное давление С02 в выдыхаемом воздухе. При эмфиземе легких, когда происходит резкое снижение эластического сопротивления легких, вентиляция мертвого пространства увеличивается за счет значительного расширения мелких бронхов на вдохе и сужения их на выдохе.
Данные морфометрии легких [Вейбель Е., 1963] позволили установить: из 23 порядков ветвления бронхов респираторная зона начинается с 17-го, когда суммарный просвет трубок настолько велик, что движения воздуха в этой зоне практически нет. Обмен газов происходит здесь преимущественно путем диффузии, и объем респираторной зоны равен примерно 3000 мл. Расстояние от конечных бронхиол до самых ди-стальных альвеол составляет до 5 мм. Скорость диффузии газов достаточно велика, чтобы концентрация их в пределах ацинуса выравнивалась за 1 с. При эмфиземе легких резко увеличивается ООЛ за счет расширения бронхиол, что увеличивает расстояние диффузии.
Избыточная вентиляция легких способствует вымыванию С02 из альвеолярного воздуха, приводит к возникновению гипервентиляционного синдрома, который развивается при многих заболеваниях (лихорадка различного происхождения, острая пневмония, приступ бронхиальной астмы средней степени тяжести, поражения нервной системы, психические расстройства и др.) и диагностируется по снижению Р„С02 артериальной крови. Альвеолярная гиповентиляция характерна для тяжелой степени недостаточности внешнего дыхания при резко выраженных об-структивных и рестриктивных нарушениях внешнего дыхания и определяется по повышению р„С02 артериальной крови.
Неравномерность альвеолярной вентиляции. Регионарное распределение вентиляции легких в нормальных условиях не является идеальным не только в связи с особенностями анатомического строения легких и функциони-
512
р ования
дыхательной мускулатуры. При изучении
градиента плеврального давления было
установлено, что над верхушками
легких плевральное давление более
отрицательное (примерно на 2 см вод.
ст.), в связи с чем верхние отделы легких
были растянуты. Нижние же отделы легких
менее растянуты и больше, чем верхние,
податливы инспираторному расширению,
а следовательно, лучше вентилируются.
В конце глубокого выдоха бронхи
нижних отделов легких закрываются, а
бронхи верхних отделов продолжают
оставаться открытыми. Считается, что
это обусловлено массой легких.
ования
дыхательной мускулатуры. При изучении
градиента плеврального давления было
установлено, что над верхушками
легких плевральное давление более
отрицательное (примерно на 2 см вод.
ст.), в связи с чем верхние отделы легких
были растянуты. Нижние же отделы легких
менее растянуты и больше, чем верхние,
податливы инспираторному расширению,
а следовательно, лучше вентилируются.
В конце глубокого выдоха бронхи
нижних отделов легких закрываются, а
бронхи верхних отделов продолжают
оставаться открытыми. Считается, что
это обусловлено массой легких.
Неравномерность альвеолярной вентиляции -одно из важнейших патологических проявлений нарушения функции вентиляции легких, которое оценивается с помощью нового информативного метода - определения объема закрытия дыхательных путей. Исследование проводится с помощью азотографа или капнографа, позволяющих регистрировать концентрацию азота или углекислого газа в выдыхаемом воздухе безынерционно. Этот метод используется для определения физиологического мертвого пространства. Обследуемый делает глубокий вдох чистым кислородом и выдыхает в газоанализатор, снабженный двухкоординатным самописцем. По оси абсцисс регистрируется ЖЕ Л, а по оси ординат - концентрация азота или углекислого газа. На графике вычерчивается кривая, отражающая изменение концентрации исследуемого газа в выдыхаемом воздухе в зависимости от структуры ЖЕЛ.
В начальном отрезке ЖЕЛ (уровень РО ) азота нет, так как выдыхается воздух из мертвого пространства, где находится чистый кислород (1-я фаза). Далее в газоанализатор поступает газ из мелких бронхов, где к чистому кислороду примешивается альвеолярный воздух, содержащий азот. Концентрация азота при этом быстро нарастает (2-я фаза), достигает определенного уровня и выходит на плато (это 3-я фаза, которая расценивается как альвеолярное плато). Концентрация азота в этой фазе сравнительно постоянна, что обусловлено поступлением в газоанализатор воздуха из респираторной зоны. С выдыханием последних порций газа РО. кон-
Ьыд
центрация азота вновь повышается. Это 4-я фаза, которая обусловлена тем, что бронхи в нижних отделах легких закрываются и изгнание газа из них прекращается. Последние порции газа вы-
дыхаются из верхних отделов легких, где бронхи еще открыты, а концентрация азота в верхних отделах легких выше, так как они вентилируются хуже, чем нижние отделы. Объем газа, который выдыхается от начала 4-й фазы, называют объемом закрытия легких (ОЗЛ). В норме он составляет 14% ЖЕЛ и нарастает при нарушении бронхиальной проходимости. Считается, что ОЗЛ является наиболее чувствительным тестом нарушения вентиляционной функции легких. Он увеличивается с возрастом у здоровых людей, у курильщиков.
15.1.3. Нарушение диффузионной способности легких
Диффузионная способность легких - скорость диффузии газов через альвеолярно-капил-лярный барьер, выражается в миллилитрах в 1 мин (мл/мин) при разнице парциальных давлений газа по обе стороны барьера 1 мм рт. ст. В данном случае исключаются изменения вентиляции альвеол, соотношений между вентиляцией и кровотоком, а подразумевается мембранное сопротивление диффузии газа.
Диффузия газа через альвеолярно-капилляр-ный барьер согласно закону Фика прямо пропорциональна площади диффузионной поверхности, разнице парциального давления по обе стороны мембраны и обратно пропорциональна ее толщине. Это может быть проиллюстрировано следующей формулой:
S V= — D(Pl -PJ, d
где V - количество диффундируемого газа; S - площадь диффузионной поверхности; D - константа диффузии; (Р1 - Р2) - разница парциального давления газа по обе стороны барьера; d - толщина слоя. Константа диффузии пропорциональна растворимости газа (а) и обратно пропорциональна квадратному корню из величины его молекулярной массы:
а D~ -== . д/ м.м.
Диффузионная поверхность легких огромна и достигает в нормальных условиях 50-100 м2. Толщина альвеолярно-капиллярного барьера составляет в норме менее 0,5 мкм. Молекулы кислорода проходят через альвеолярную мембрану,
513
межклеточную жидкость, мембрану капилляра, слой плазмы, эритроцит.
Определение так называемого мембранного компонента диффузии газов через альвеоляр-но-капиллярный барьер представляет собой основную и наиболее трудную задачу при исследовании диффузионной способности легких, поскольку перенос газов зависит и от свойств мембран, и от перфузии. Оценка значения неравномерности вентиляции легких также достаточно сложна.
Для определения диффузионной способности легких (ДЛСО) используются 3 метода, которые основаны на определении концентрации СО: 1) метод устойчивого состояния (ДЛус); 2) метод с задержкой дыхания, или метод одиночного вдоха (ДЛзд); 3) метод возвратного дыхания. Наиболее часто используют второй метод. Исследуемый вдыхает газовую смесь с низким содержанием СО и гелия. В конце вдоха исследуемый задерживает дыхание на 10 с. На выдохе определяют концентрацию СО и гелия в выдыхаемом воздухе. По разнице концентраций гелия во вдыхаемом и выдыхаемом воздухе определяют остаточный объем легких, по разнице концентрации СО - количество газа, прошедшего через мембраны. ДЛСО увеличивается с увеличением размеров тела (масса, рост, площадь поверхности), увеличивается к 20 годам, затем уменьшается с возрастом в среднем на 2% ежегодно. У женщин ДЛСО в среднем на 10% меньше, чем у мужчин. При физической нагрузке ДЛСО увеличивается, что связано с раскрытием резервных капилляров. В клиностатическом положении ДЛСО больше, чем в положении сидя, и еще больше по сравнению с положением стоя. Это объясняется разницей объема капиллярной крови в легких при разных положениях тела.
Уменьшение ДЛСО происходит при рестрик-тивных нарушениях вентиляции легких, что обусловливается уменьшением объема функционирующей паренхимы легких. При хронической обструктивной эмфиземе легких также снижается ДЛСО, но это главным образом связано с редукцией сосудистого русла. В таких случаях на первое место выступают вентиляционные нарушения легких и нарушения ДЛСО рассматриваются как сопутствующие изменения.
Диффузионный вид нарушения функции внешнего дыхания является ведущим при: 1) отеке легких (альвеолярном, интерстициальном)
различного происхождения (кардиогенный, токсический, при аллергическом, иммунном, бактериальном воспалении различной этиологии); 2) при развитии фиброзных изменений в легких, в частности при поражении пространства между альвеолярными и капиллярными мембранами (склеродермия, саркоидоз легких, берил-лиоз, асбестоз, аллергические заболевания с поражением легких, альвеолярный рак и другие заболевания).
При отеке легких увеличивается расстояние диффузии, что объясняет снижение ДЛСО. Особое место в рассматриваемой группе болезней занимает острая пневмония. Проникая в респираторную зону, бактерии взаимодействуют с сур-фактантом и нарушают его структуру. Это ведет к снижению его способности уменьшать поверхностное натяжение в альвеолах, а также способствует развитию отека. Кроме того, нормальная структура монослоя сурфактанта обеспечивает высокую растворимость кислорода и способствует его диффузии в кровь. При нарушении структуры сурфактанта растворимость кислорода уменьшается, снижается диффузионная емкость легких. Важно отметить, что патологическое изменение сурфактанта характерно не только для зоны воспаления, но и для всей или по крайней мере большей части диффузионной поверхности легких. Восстановление свойств сурфактанта после перенесенной пневмонии происходит в течение 3-12 мес.
Фиброзные и грануломатозные изменения в легких затрудняют диффузию кислорода, обусловливая умеренную степень гипоксемии. Ги-перкапния для диффузионного вида недостаточности внешнего дыхания не типична, так как диффузия С02 через мембраны проходит в 20 раз легче, и для снижения диффузии С02 требуется очень высокая степень поражения мембран. Так, например, при очень тяжелой пневмонии возможна III степень гипоксемии, а избыточная вентиляция в связи с лихорадкой может привести к гипокапнии.
С гиперкапнией, тяжелой гипоксемией, дыхательным и метаболическим ацидозом протекает дистресс-синдром у новорожденных, который нужно отнести к диффузионному виду нарушения внешнего дыхания. В патогенезе его имеет большое значение анатомическая и функциональная незрелость легких, заключающаяся в том, что к моменту рождения в легких в недо-
статочной мере вырабатывается сурфактант. В связи с этим при первом вдохе раскрываются не все отделы легких, возникают участки ателектаза. В них повышена проницаемость сосудов, которая способствует развитию кровоизлияний. Гиалиноподобное вещество на внутренней поверхности альвеол и альвеолярных ходов способствует нарушению диффузии газов. Прогноз тяжелый, зависит от степени и протяженности патологических изменений в легких.
Если раньше респираторный дистресс-синдром описывали только у новорожденных детей, го позднее такое название синдрома стало применяться для описания тяжелых нарушений легочных функций и у взрослых. Это неспецифический синдром, развивающийся как крайняя степень острого нарушения внешнего дыхания. Повреждение легких приводит к обширным двухсторонним инфильтратам, очень плохо поддающейся коррекции гипоксемии, резкому снижению растяжимости легких. Синдром наблюдается при сепсисе, аспирации содержимым желудка, вдыхании токсических газов, лекарственной болезни, наркомании, высотном отеке легких, жировой эмболии, реимплантации легких и др. Прогноз тяжелый: до 50% больных с такими нарушениями в легких погибают.
15.1.4. Нарушение кровообращения в легких
В легких имеется два сосудистых русла: малый круг кровообращения и система бронхиальных сосудов большого круга кровообращения. Кровоснабжение легких осуществляется, таким образом, из двух систем.
Малый круг кровообращения имеет ряд особенностей, связанных с физиологией аппарата внешнего дыхания, которые определяют характер патологических отклонений функции кровообращения в легких, приводящих к развитию гипоксемии. Давление в легочных сосудах низкое по сравнению с большим кругом кровообращения. В легочной артерии оно в среднем составляет 15 мм рт. ст. (систолическое - 25, диа-столическое - 8 мм рт. ст.). Давление в левом предсердии достигает 5 мм рт. ст. Таким образом, перфузия легких обеспечивается давлением, в среднем равным 10 мм рт. ст. Этого достаточно для достижения перфузии против сил гравитации в верхних отделах легких. Тем не ме-
нее силы гравитации считаются важнейшей причиной неравномерности перфузии легких. В вертикальном положении тела легочный кровоток почти линейно убывает в направлении снизу вверх и является минимальным в верхних отделах легких. В горизонтальном положении тела (лежа на спине) кровоток в верхних отделах легких увеличивается, но остается все-таки меньше, чем в нижних отделах. При этом возникает дополнительный вертикальный градиент кровотока - он убывает от дорзальных отделов по направлению к вентральным. Следует заметить, что при изменении положения тела человека так называемый весовой градиент кровотока, впрочем как и вентиляции легких, и плеврального давления, полностью не исчезает и не извращается. Последнее дает основание осторожнее относиться к сугубо механистическим построениям учения о весовом градиенте различных функций легких.
Вполне удовлетворительная функция аппарата внешнего дыхания в условиях невесомости указывает на существование развитых систем регуляции различных механических функций легких. Однако при патологии гравитационные влияния на функциональные параметры легких нарастают. Примером этому может служить клиническая картина ортопноэ, особенно ярко выраженная при острой недостаточности левых отделов сердца (сердечная астма). В клиноста-тическом положении приток крови к левому предсердию затрудняется, а в ортостатическом -облегчается.
Особенностью малого круга кровообращения является еще то, что все крупные и средние артерии его относятся к сосудам эластического типа. К артериям мышечного типа относятся артерии диаметром 0,1-1 мм. В более мелких артериях и артериолах мышечные волокна почти отсутствуют. Таким образом, вазомоторные реакции реализуются не в артериолах малого круга, а в артериях мышечного типа. В нормальных условиях минутный объем правого желудочка сердца несколько меньше, чем левого, за счет сброса крови из системы большого круга кровообращения через анастомозы бронхиальных артерий, капилляров и вен с сосудами малого круга, так как давление в сосудах большого круга выше, чем в сосудах малого круга.
При значительном увеличении давления в малом круге, например при митральном стенозе, сброс крови может быть в противоположном
направлении, и тогда минутный объем правого желудочка сердца превышает таковой левого желудочка.
В нормальных условиях в легких находится в среднем 500 мл крови: по 25% ее объема в артериальном русле и в легочных калиллярах, 50% - в венозном русле. Время прохождения крови через малый круг кровообращения составляет в среднем 4-5 с. Гиперволемия малого круга кровообращения характерна для врожденных пороков сердца (открытый артериальный проток, дефект межжелудочковой и межпредсердной перегородок), когда в легочную артерию постоянно поступает повышенный объем крови в результате патологического сброса ее слева направо. В таких случаях оксигенация крови остается нормальной. При высокой легочной артериальной гипертензии сброс крови может быть в противоположном направлении. В таких случаях развивается гипоксемия.
Уменьшению перфузии легких способствуют: 1) снижение сократительной функции правого желудочка; 2) недостаточность левых отделов сердца, когда снижение перфузии легких происходит на фоне застойных изменений в легких; 3) некоторые врожденные и приобретенные пороки сердца (стеноз устья легочной артерии, стеноз правого атриовентрикулярного отверстия);
сосудистая недостаточность (шок, коллапс);
тромбоз или эмболия в системе легочной артерии. При данных патологических состояниях нет гипоксемии, поскольку вентиляция легких существенно преобладает над кровотоком, тогда как содержание углекислоты в крови может быть сниженным. При резком падении минутного объема крови содержание углекислоты в крови повышается в связи с замедлением кровотока в тканях.
Бронхиальное сосудистое русло представляет собой разветвление бронхиальных артерий большого круга кровообращения, через которые осуществляется кровоснабжение легких. Через эту систему сосудов проходит от 1 до 2% крови минутного объема сердца. Около 30% крови, проходящей по бронхиальным артериям, поступает в бронхиальные вены и затем в правое предсердие. Большая часть крови попадает в левое предсердие через прекапиллярные, капиллярные и венозные шунты. Кровоток по бронхиальным артериям усиливается при патологии (острые и хронические воспалительные заболевания, пнев-мофиброз, тромбоэмболия в системе легочной
артерии и др.). Значительное повышение кровотока по бронхиальным артериям способствует повышению нагрузки на левый желудочек сердца. Разрывы расширенных бронхиальных артерий являются основной причиной легочных кровотечений при различных формах патологии легких.
Механизмы развития гипоксемии
Альвеолярная гиповентиляция. Давление кислорода в альвеолярном воздухе меньше атмосферного в среднем на l/З, что обусловлено поглощением О, кровью и восстановлением его напряжения в результате вентиляции легких. Соответственно поддерживается нормальная величина напряжения СО.,. Это равновесие динамическое. При уменьшении вентиляции легких преобладает процесс поглощения кислорода, а вымывание углекислого газа снижается. В результате развиваются гипоксемия и гиперкап-ния, что наблюдается при различных формах патологии - при обструктивных и рестриктив-ных нарушениях вентиляции легких, нарушениях регуляции дыхания, поражении дыхательной мускулатуры.
Неполная диффузия кислорода из альвеол. Она имеет место и в нормальных условиях. При повышении сопротивления диффузии (величина, обратная диффузионной способности легких) развивается гипоксемия. Причины нарушения диффузионной способности легких рассмотрены выше.
Увеличение скорости потока крови по легочным капиллярам. Оно приводит к уменьшению времени контакта крови с альвеолярным воздухом, что наблюдается при рестриктивных нарушениях вентиляции легких, когда уменьшается емкость сосудистого русла и увеличивается минутный объем кровотока, в частности при физической нагрузке. Это характерно и для хронической обструктивной эмфиземы легких, при которой имеет место уменьшение сосудистого русла (структурные изменения).
4.Шунты. В нормальных условиях около 5% потока крови идет мимо альвеолярных капилляров и неоксигенированная кровь снижает среднее напряжение кислорода в венозном русле малого круга кровообращения. Насыщение артериальной крови кислородом составляет 96-98%. Шунтирование крови может увеличиваться при повышении давления в системе легочной
516
артерии, возникающем при недостаточности левых отделов сердца, при хронической обструк-тивной патологии легких, при патологии печени, что связывается с влиянием биологически активных веществ, которые не инактивируются в печени в достаточной мере. Шунтирование венозной крови в легочные вены может осуществляться из системы вен пищевода при портальной гипертонии через так называемые порто-пульмональные анастомозы. Особенностью ги-поксемии, связанной с шунтированием крови, является отсутствие лечебного эффекта от вдыхания чистого кислорода.
5. Вентиляционно-перфузионные расстройства. Неравномерность вентиляционно-перфу-зионных отношений свойственна нормальным легким и обусловлена, как уже было отмечено, силами гравитации. В верхних отделах легких кровоток минимальный. Вентиляция в этих отделах тоже снижена, но в меньшей степени. Поэтому от верхушек легких кровь оттекает с нормальным или даже повышенным напряжением Ог, однако в связи с небольшим общим количеством крови это мало влияет на степень ок-сигенации артериальной крови. В нижних отделах легких, напротив, кровоток значительно повышен (в большей степени, чем вентиляция легких). Небольшое снижение напряжения кислорода в оттекающей крови при этом способствует развитию гипоксемии, так как увеличивается общий объем крови с недостаточным насыщением кислородом. Такой механизм гипоксемии характерен для застоя в легких, отека легких различной природы (кардиогенный, воспалительный, токсический).
Легочная артериальная гипертензия
Повышение давления в системе легочной артерии могут вызывать следующие факторы:
1. Рефлекс Эйлера - Лильестранда. Уменьшение напряжения кислорода в альвеолярном воздухе сопровождается повышением тонуса артерий малого круга. Этот рефлекс имеет физиологическое назначение - коррекция кровотока в связи с изменяющейся вентиляцией легких. Если в определенном участке легкого вентиляция альвеол уменьшается, соответственно, должен уменьшиться кровоток, так как в противном случае отсутствие должной оксигенации крови приводит к снижению насыщения ее кислородом. Повышение тонуса артерий в данном учас-
тке легкого уменьшает кровоток, и отношение вентиляция/кровоток выравнивается. При хронической обструктивной эмфиземе легких альвеолярная гиповентиляция охватывает основную массу альвеол. Следовательно, тонус артерий малого круга, ограничивающих кровоток, повышается в основной массе структур респираторной зоны, что приводит к увеличению сопротивления и повышению давления в легочной артерии.
Редукция сосудистого русла. В нормальных условиях при физической нагрузке в легочный кровоток включаются резервные сосудистые русла и повышенный кровоток не встречает повышенного сопротивления. При редуцировании сосудистого русла увеличение кровотока при физической нагрузке приводит к увеличению сопротивления и повышению давления в легочной артерии. При значительном сокращении сосудистого русла сопротивление может быть повышенным и в покое.
Повышение альвеолярного давления. Повышение давления на выдохе при обструктивной патологии способствует ограничению кровотока. Экспираторное повышение альвеолярного давления более продолжительное, чем падение его на вдохе, ибо выдох, как правило, затянут. Поэтому повышение альвеолярного давления способствует повышению сопротивления в малом круге и повышению давления в легочной артерии.
Повышение вязкости крови. Оно обусловлено симптоматическим эритроцитозом, который характерен для хронической экзогенной и дыхательной гипоксии.
Увеличение минутного объема сердца.
6.Биологически активные вещества. Они вырабатываются под влиянием гипоксии в тканях легких и способствуют развитию легочной артериальной гипертензии. Серотонин, например, способствует нарушению микроциркуляции. При гипоксии снижается разрушение в легких ангиотензина-Н и норадреналина, которые способствуют сужению артериол.
Легочная артериальная гипертензия может быть и другой природы, которая во многом остается недостаточно изученной: 1) постэмболическая легочная гипертензия; 2) иммуноаллерги-ческий васкулит с преимущественным поражением легких и 3) первичная легочная артериальная гипертензия, природа которой неясна и чаще всего объясняется теми же причинами, что и артериальная гипертония.
517
Особого внимания заслуживает изучение так называемой северной гипертензии малого круга кровообращения, которая связана с влиянием холода, вызывающего перестройку органов дыхания и кровообращения. Реакция системы дыхания и кровообращения при этом может носить как адаптивный, так и дезадаптивный характер, способствуя развитию хронических заболеваний бронхолегочной системы.
Актуальной является еще одна причина развития легочной артериальной гипертензии: лекарственная болезнь, прием гормональных противозачаточных препаратов и др. Описанные механизмы легочной артериальной гипертензии способствуют развитию легочного сердца.
При пороках левых отделов сердца, гипертонической болезни, ишемической болезни сердца развитие легочной артериальной гипертензии обусловлено недостаточностью левых отделов сердца. Недостаточность систолической и диас-толической функции левого желудочка приводит к повышению в нем конечного диастоличес-кого давления (более 5 мм рт.ст.), что затрудняет переход крови из левого предсердия в левый желудочек. Антеградный кровоток в этих условиях поддерживается в результате повышения давления в левом предсердии. Чтобы поддержать кровоток по системе малого круга, включается рефлекс Китаева. Барорецепторы находятся в устье легочных вен, а результатом раздражения этих рецепторов является повышение давления в артериях малого круга. Таким образом, увеличивается нагрузка на правый желудочек, повышается давление в легочной артерии и восстанавливается каскад давлений от легочной артерии к левому предсердию. Это так называемая пассивная легочная артериальная гипертен-зия.
Легочная артериальная гипертензия приводит к рестриктивным нарушениям вентиляции легких: инспираторной одышке, снижению растяжимости легких, ЖЕЛ, ОЕЛ. Снижение растяжимости легких определяет инспираторную одышку. Объяснение этому явлению можно дать на примере шланга, по которому протекает вода под разным давлением. При большом давлении шланг согнуть труднее. При легочной артериальной гипертензии могут развиваться фиброзные изменения в легочной ткани, что усиливает рестриктивные нарушения вентиляции легких. Легочная артериальная гипертензия способствует также усилению шунтирования крови
в легочные вены, минуя капилляры, и возникновению артериальной гипоксемии.
Отек легких
В зависимости от причин, вызвавших развитие отека легких, различают следующие его виды: 1) кардиогенный (болезни сердца и сосудов); 2) обусловленный парентеральным введением большого количества кровезаменителей; 3) воспалительный (бактериальные, вирусные поражения легких); 4) вызванный эндогенными токсическими воздействиями (уремия, печеночная недостаточность) и экзогенными поражениями легких (вдыхание паров кислоты, отравляющих веществ); 5) аллергический (например, сывороточная болезнь); 6) вызванный воздействием вазоактивных веществ и препаратов (гиста-мин, простагландины, катехоламины).
Кардиогенный отек легких развивается при острой недостаточности левых отделов сердца (см. гл. 14). Ослабление сократительной и диастолической функций левого желудочка возникает при миокардитах, кардиосклерозе, инфаркте миокарда, гипертонической болезни, недостаточности митрального клапана, недостаточности аортальных клапанов и стенозе устья аорты. Недостаточность левого предсердия развивается при митральном стенозе. Исходным моментом недостаточности левого желудочка является повышение в нем конечного диастоли-ческого давления, что затрудняет переход крови из левого предсердия. Повышение давления в левом предсердии препятствует переходу в него крови из легочных вен. Повышение давления в устье легочных вен приводит к рефлекторному повышению тонуса артерий мышечного типа малого круга кровообращения (рефлекс Китаева), что и вызывает легочную артериальную ги-пертензию. Давление в легочной артерии возрастает до 35-50 и даже до 150 мм рт.ст. Особенно высокой легочная артериальная гипертензия бывает при митральном стенозе. Фильтрация жидкой части плазмы из легочных капилляров в ткани легких начинается, если гидростатическое давление в капиллярах превышает 25-30 мм рт. ст., т.е. величину коллоидно-осмотического давления. При повышенной проницаемости капилляров фильтрация может происходить при меньших величинах давления. Попадая в альвеолы, транссудат затрудняет газообмен между альвеолами и кровью. Возникает альвеолярно-ка-
518
пиллярная блокада. На этом фоне развивается гипоксемия, резко ухудшается оксигенация тканей сердца, возникает его остановка при общих расстройствах кровообращения и дыхании типа асфиксии.
Отек легких может возникнуть при быстром внутривенном вливании большого количества жидкости (физиологический раствор, кровезаменители). Это происходит в результате «разведения» альбуминов крови, снижения онкотического давления и повышения гидростатического давления крови.
При микробном поражении легких развитие отека связано с поражением системы сурфактанта микробными агентами. При этом повышается проницаемость альвеоляр-но-капиллярной мембраны, что способствует развитию внутриальвеолярного отека и снижению диффузии кислорода. Это происходит не только в очаге воспалительного отека, а диффузно в легких в целом.
Токсические вещества различной природы также повышают проницаемость аль-веолярно-капиллярных мембран. Отек легких может развиваться при диссеминированном внут-рисосудистом свертывании крови, осложняющем течение тяжелых заболеваний.
Аллергический отек легких развивается вследствие гиперреактивности организма немедленного типа. Механизм его заключается в резко возникающем повышении проницаемости капилляров в результате действия гуморальных факторов, высвобождающихся из тучных и других клеток при анафилаксии.
Введение больших количеств катехоламинов (адреналина), а также стрессовые ситуации, которые сопровождаются выделением большого количества норадренали-на в кровь, вызывают сужение артериол во многих частях тела и увеличение кровенаполнения легких за счет перераспределения крови между большим и малым кругом кровообращения. Этот процесс лежит в основе развития отека легких вследствие легочной гипертензии и застоя крови в малом круге кровообращения. Подобный отек вызывается экспериментально при введении адреналина в больших дозах в кровь животных (как внутривенно, так и внутриартериаль-но).
Особенностью патогенеза отека легких по
сравнению с отеком других органов является то, что транссудат преодолевает в развитии этого процесса два барьера: 1) гистогематический (из сосуда в межтканевое пространство) и 2) гисто-альвеолярный (через стенку альвеол в их полость). Переход жидкости через первый барьер приводит к интерстициальному отеку, а через второй - к альвеолярному отеку легких.
Клинически отек легких проявляется тяжелой инспираторной одышкой или удушьем. При альвеолярном отеке определяются влажные хрипы и пенистая жидкая с кровью мокрота. При интерстициальном отеке хрипов нет. Степень гипоксемии зависит от тяжести клинического синдрома. При интерстициальном отеке более характерна гипокапния в связи с гипервентиляцией легких. В тяжелых случаях развивается гиперкапния.
15.1.5. Нарушение регуляции дыхания
Регуляция дыхания осуществляется дыхательным центром, расположенным в ретикулярной формации продолговатого мозга. Различают центр вдоха и центр выдоха. Деятельность дыхательного центра регулируется вышележащими отделами мозга.
Большое влияние на деятельность дыхательного центра оказывает кора головного мозга, что проявляется в произвольной регуляции дыхательных движений, возможности которой ограничены. Нормальное дыхание называют эупноэ.
Нарушения регуляции дыхания могут быть обусловлены различными причинами и наблюдаются при многих патологиях: сосудистых заболеваниях мозга (атеросклероз сосудов, васку-литы), нейроинфекции, опухоли мозга (первичные, метастатические), отравлениях алкоголем, морфином и другими наркотиками, снотворными, транквилизаторами. Кроме того, нарушения регуляции дыхания могут быть при нейроцир-куляторной дистонии различного происхождения, при психических и многих соматических заболеваниях. При хронических заболеваниях легких и выраженных нарушениях вентиляционной функции также имеют место определенные нарушения регуляции дыхания, часто опасные для жизни (например, при бронхиальной астме).
519
Синдром Пиквика - снижение функции системы регуляции дыхания центрального происхождения, обусловливающее альвеолярную ги-повентиляцию, гипоксемию и гиперкапнию. Далее развивается легочное сердце с последующей его декомпенсацей. К наиболее характерным симптомам у больных с синдромом Пиквика следует отнести сонливость, цианоз и ожирение.
Синдром нарушения ночного сна заключается в кратковременных остановках дыхания (при этом 5 приступов за 1 час представляет угрозу жизни). Синдром проявляется беспорядочным громким храпом, чередующимся с длительными паузами от 10 с до 2 мин. При этом развивается гипоксемия. Часто у пациентов отмечается ожирение, иногда гипотиреоз. Различают 2 типа синдрома: 1) центральный (нарушение регуляции дыхания); 2) обструктивный (за-падение мягкого неба, корня языка, гиперплазия небных миндалин, аденоиды, дефекты развития нижней челюсти).
Под влиянием рефлекторных и гуморальных воздействий могут изменяться частота, глубина и ритм дыхательных движений.
Брадипноэ - редкое дыхание. Рефлекторное уменьшение частоты дыхания наблюдается при повышении артериального давления (рефлекс с барорецепторов дуги аорты), при гипероксии в результате выключения хеморецепторов, чувствительных к понижению ра02. При стенозиро-вании крупных дыхательных путей возникает редкое и глубокое дыхание, называемое стено-тическим. В этом случае рефлексы поступают от межреберных мышц и ослабевает тормозящее действие рефлекса Геринга - Брейера. Брадипноэ возникает при гипокапнии, развивающейся при подъеме на большую высоту (горная болезнь). Угнетение дыхательного центра может иметь место при длительной гипоксии (пребывание в условиях разреженной атмосферы, недостаточность кровообращения и др.), при действии наркотиков, при органических поражениях головного мозга.
Полипноэ (тахипноэ) - частое поверхностное дыхание. Этот вид дыхания наблюдается при лихорадке, при функциональных нарушениях деятельности центральной нервной системы, при поражениях легких (пневмония, застой в легких, ателектаз). В происхождении тахипноэ имеет значение большая, чем в норме, стимуляция дыхательного центра. При снижении ра-
стяжимости легких усиливаются импульсы от проприорецепторов дыхательных мышц. Здесь следует учитывать один из важнейших принципов регуляции механических движений легких - регуляторная система «выбирает» наиболее экономичные с точки зрения затраты работы дыхания глубину и частоту дыхания. При увеличении эластического сопротивления глубокое дыхание оказывается неэкономичным. Напротив, при обструктивной патологии неэкономичной является высокая частота дыхания. Считается также, что при ателектазе усиливаются импульсы с легочных альвеол, находящихся в спавшемся состоянии. Выдох же стимулируется от большего, чем в норме, растяжения непораженных легочных структур. Как указывалось ранее, тахипноэ способствует развитию альвеолярной ги-повентиляции в результате преимущественной вентиляции мертвого пространства. Тахипноэ может возникать при болях в грудной клетке (щадящее дыхание), где механизм его возникновения является чисто рефлекторным.
Гиперпноэ - глубокое и частое дыхание. Оно наблюдается при повышении основного обмена: при физической нагрузке, при тиреотоксикозе, при эмоциональной нагрузке, лихорадке. Если гиперпноэ вызвано рефлекторно и не связано с повышением потребления кислорода и выведения С02, то гипервентиляция приводит к алкалозу, резкому падению Р„С02. Гиперпноэ возникает также при анемии и ацидозе, снижении содержания кислорода во вдыхаемом воздухе.
Апноэ - отсутствие дыхания. Подразумевается временная остановка дыхания. Она может возникнуть рефлекторно при быстром подъеме артериального давления (рефлекс с барорецепторов), после пассивной гипервентиляции пациента под наркозом (снижение раС02). Апноэ может быть связано с понижением возбудимости дыхательного центра (гипоксия, поражения головного мозга при интоксикациях и др.). Торможение дыхательного центра вплоть до его остановки может возникать при действии наркотических препаратов (эфир, хлороформ, барбитураты и др.), при понижении содержания кислорода во вдыхаемом воздухе.
Кашель тоже относят к нарушениям дыхания, хотя это справедливо лишь отчасти, когда соответствующие изменения дыхательных движений носят не защитный, а патологический характер. Наиболее типичными рефлексогенными зонами кашлевого рефлекса являются гор-
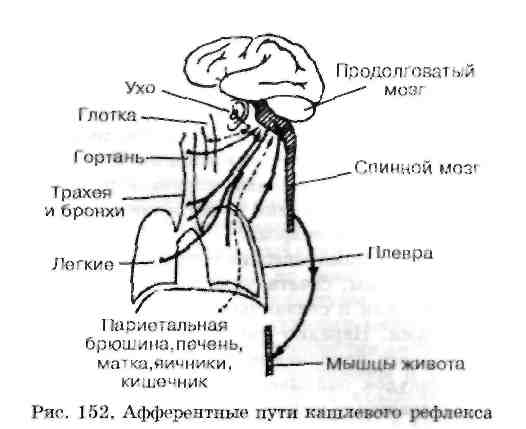
Наличие особого кашлевого центра не получило научного подтверждения. Механизм кашля рассматривается с позиции теории точек равного давления. Вначале (1-я фаза) происходит вдох различной глубины и продолжительности в зависимости от последующей силы кашлевого толчка. Далее смыкается голосовая щель и развивается напряжение мышц, обеспечивающих выдох (2-я фаза). При этом резко повышается внут-риплевральное давление, в том числе и давление воздуха в дыхательных путях. 3-я фаза -открытие голосовой щели, в результате чего воздух с большой силой и скоростью выходит из дыхательных путей вместе с содержимым бронхов (бронхиальный секрет, гной, частицы пыли, инородные тела и др.), которое после откашливания называется мокротой.
При медленном и спокойном вдохе отрицательное внутриплевральяое давление соответствует эластической тяге легких и составляет в нормальных условиях 17-35 см вод. ст. При форсированном вдохе внутриплевральяое давление может снижаться на 100 мм рт. ст. Во вторую фазу кашля положительное внутриплевраль-ное давление может достигать 150 мм рт. ст. При этом давление в дыхательных путях больше, чем в плевральной полости, на величину эластической тяги легких. В 3-ю фазу, когда открывается голосовая щель, в дыхательных путях возникает сильный поток воздуха и статическое давление в них снижается.
Наибольшая скорость потока - в трахее и крупных бронхах, поэтому здесь большее динамическое и меньшее статическое давление. Просвет трахеи и крупных бронхов становится минимальным в результате их сжатия высоким внутри-грудным давлением, что способствует еще большему увеличению скорости потока воздуха. От полного закрытия просвета эти дыхательные пути защищает хрящевая основа и функция мем-бранозной части стенок. На уровне средних брон-
хов в связи со снижением скорости воздушного потока в меньшей степени падает статическое давление, при этом оно может выравниваться с внутриплевральным давлением. В этом случае бронхи среднего калибра не сжимаются, так как здесь находится точка равного давления - статического давления в бронхах и давления, окружающего бронхи. В мелких бронхах движение воздуха незначительное, и давление в них больше, чем в плевральной полости. При эмфиземе эластическая тяга легких снижена (7-12 см вод. ст.), поэтому точка равного давления смещается по направлению к мелким бронхам. При кашле в таком случае происходит сужение средних бронхов. Это является причиной неэффективности кашля при эмфиземе легких.
Чихание - рефлекторный акт, аналогичный кашлю. Оно вызывается раздражением нервных окончаний тройничного нерва, расположенных в слизистой оболочке носа. Форсированный поток воздуха при чихании направлен через носовые ходы.
И кашель, и чихание являются физиологическими защитными механизмами, направленными на очищение в первом случае бронхов, а во втором - носовых ходов. Длительный, изнуряющий пациента кашель при патологии может нарушать газообмен и кровообращение в легких и требует определенного терапевтического вмешательства, направленного на облегчение кашля и улучшение дренажной функции бронхов.
Зевота представляет собой глубокий вздох при резко открытой голосовой щели, затем усилие на вдохе продолжается при закрытой и вновь открытой голосовой щели. Полагают, что зевота
521
Икота - спазматические сокращения (судороги) диафрагмы, сочетающиеся с закрытием голосовой щели и связанными с этим звуковыми явлениями. Нередко икота развивается после чрезмерного наполнения желудка (переполненный желудок оказывает давление на диафрагму, раздражая ее рецепторы). Икота может иметь центрогенное происхождение и развивается при гипоксии мозга.
Нарушения ритма дыхательных движений
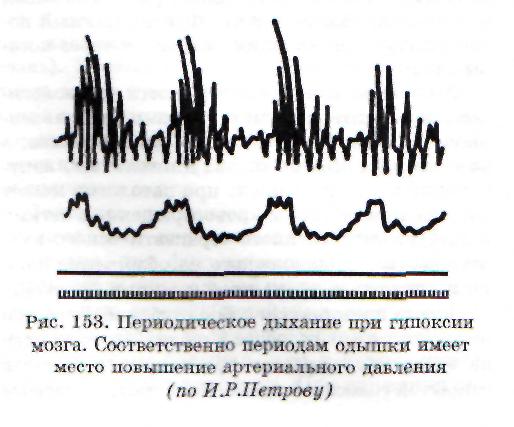
Типы периодического дыхания. К ним относятся дыхание Чейна - Стокса и дыхание Био-та. При дыхании Чейна - Стокса паузы чередуются с дыхательными движениями, которые сначала нарастают по глубине, затем убывают (рис. 153). При дыхании Биота паузы чередуются с дыхательными движениями нормальной частоты и глубины. В основе патогенеза периодического дыхания лежит понижение возбудимости дыхательного центра. Оно может возникать при органических поражениях головного мозга - травмах, инсультах, опухолях, воспалительных процессах при ацидозе, диабе-
тической и уремической комах, при эндогенных и экзогенных интоксикациях. Возможен переход в терминальные типы дыхания. Иногда периодическое дыхание наблюдается у детей и людей старческого возраста во время сна. В этих случаях нормальное дыхание легко восстанавливается при пробуждении.
Механизм периодического дыхания, впрочем как и других видов патологического дыхания, во многом остается неизученным. Предполагают, что на фоне пониженной возбудимости дыхательный центр не реагирует на нормальную концентрацию углекислого газа и Н+-ионов в крови. Для возбуждения дыхательного центра требуются большие их концентрации. Время накопления этих раздражителей до пороговой дозы определяет длительность паузы. Дыхательные движения создают вентиляцию легких, С02 вымывается из крови, и дыхательные движения вновь замирают. Убедительного толкования различий механизма дыхания Чейна - Стокса и Биота нет.
Терминальные типы дыхания. К ним относятся дыхание Куссмауля (большое дыхание), апнейстическое дыхание и гаспинг-дыхание. Есть основания предполагать существование определенной последовательности фатального нарушения дыхания до его полной остановки: сначала возбуждение (дыхание Куссмауля), апней-зис, гаспинг-дыхание, паралич дыхательного центра. При успешных реанимационных мероприятиях возможно обратное развитие нарушений дыхания до его полного восстановления.
Дыхание Куссмауля - шумное глубокое дыхание, характерное для пациентов с нарушением сознания при диабетической, уремической комах. Дыхание Куссмауля возникает в результате нарушения возбудимости дыхательного центра на фоне гипоксии мозга, ацидоза, токсических явлений.
Апнейстическое дыхание характеризуется продолжительным судорожным усиленным вдохом, изредка прерывающимся выдохом. Такой вид дыхательных движений возникает в эксперименте после перерезки у животного обоих блуждащих нервов и ствола на границе между верхней и средней третью моста.
Гаспинг-дыхание (от англ. gasp - ловить воздух, задыхаться) возникает в самой терминальной фазе асфиксии. Это единичные, глубокие, редкие, убывающие по силе «вздохи». Источни-
