
- •51. Статистический и термодинамический методы исследования вещества.
- •52. Основные положения молскулярно-кинетичсской теории.
- •53. Максвелловский закон распределения молекул газа по их скоростям.
- •54. Больцмановский закон распосделсния молекул газа по их энергиям.
- •55. Закон равномерного распределения энергии по степеням свободы молекул газа.
- •56. Молекулярно-кинстическое толкование абсолютной температуры
- •57. Первое начало термодинамики.
- •58. Адиабатический процесс.
- •59. Политропические процессы
- •60. Второе начало термодинамики.
- •61. Изопроцессы. Запишите уравнения состояния идеального газа для этих процессов и начертите их графики в координатах р и V, р и t, t и V.
- •62. Дайте определение полной, молярной и удельной тсплоемкостей газа.
- •63Дайте определение равновесного и неравновесного состояния системы.
- •64. Дайте определение обратимого и необратимого процесса.
- •65. Дайте определение кругового процесса (цикла). Объясните принцип действия тепловых машин.
- •66. Начертите цикл Карно в координатах р и V
- •67. Дайте определение энтропии. Чему равно изменение энтропии для обратимых и необратимых процессов.
- •Энтропия и второе начало термодинамики
- •73. Приведите барометрическую формулу. Для чего она служит?
- •74. Получите формулу для средней длины свободного пробега молекул газа.
- •75. Какое явление переноса в идеальном газе описывается выражением
- •78. Получите выражения для молярных теплоемкостей всех изопроцессов в идеальном газе. 79Получите соотношение Манера
- •Соотношение Майера
- •Соотношение Майера
- •94. Начертите изотерму Ван-дер-Ваальса и сравните ее с экспериментальной изотермой реального газа.
- •95. Дайте определение критического состояния газа. Получите выражения для параметров критического состояния газа.
- •96. Получите формулу для внутренней энергия реального газа.
- •97. В чем заключается эффект Джоуля-Томсона?
- •98. Получите уравнение Клапейрона-Клаузиуса для фазового превращения реального газа.
- •99. Нарисуйте диаграмму равновесных давлений и температур для двухфазной системы "жидкость - пар".
- •100Нарисуйте обобщенную диаграмму состояний для трехфазной системы "твердое тело - жидкость - газ". Дайте определение тройной точки.
- •Фазовые превращения реального газа
- •Уравнение Клапейрона-Клаузиуса и фазовая диаграмма для превращения жг
- •Уравнение Клайперона-Клаузиуса и Рис. 6 фазовая диаграмма для превращения тж
- •Уравнение Клайперона-Клаузиуса и фазовая диаграмма для превращения тг. Тройная точка. Диаграмма состояния.
58. Адиабатический процесс.
Адиабатический процесс - это процесс, протекающий без теплообмена с окружающей средой.
59. Политропические процессы
60. Второе начало термодинамики.
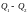 ,
,
где
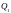 – теплота, получаемая рабочим телом
при расширении, а
– теплота, получаемая рабочим телом
при расширении, а
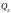 – теплота, отдаваемая при сжатии. Работа
– теплота, отдаваемая при сжатии. Работа
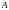 ,
совершаемая за цикл, равна площади
цикла. Таким образом, первое начало
термодинамики, написанное для цикла,
имеет вид
,
совершаемая за цикл, равна площади
цикла. Таким образом, первое начало
термодинамики, написанное для цикла,
имеет вид
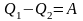
Как
следует из этого выражения, не вся
получаемая извне теплота
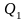 используется для получения полезной
работы.
используется для получения полезной
работы.
Коэффициентом
полезного действия
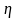 (сокращённо КПД) тепловой машины
называется отношение совершаемой за
цикл работы
(сокращённо КПД) тепловой машины
называется отношение совершаемой за
цикл работы
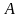 к полученной за цикл теплоте
к полученной за цикл теплоте
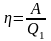 .
.
Приняв во внимание соотношение (1), выражение для КПД можно записать в виде
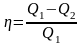 .
.
Второе начало термодинамики:
Невозможно
построить периодически действующую
тепловую машину, которая бы всю подводимую
к ней теплоту превращала в работу, т.е.
всегда
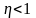 .
.
61. Изопроцессы. Запишите уравнения состояния идеального газа для этих процессов и начертите их графики в координатах р и V, р и t, t и V.
Изопроцессами называются термодинамические процессы, происходящие в системе с постоянной массой при каком либо одном постоянном параметре состояния.
Идеальным газом называется газ, молекулы которого не взаимодействуют друг с другом на расстоянии и имеют исчезающе малые собственные размеры. Состояние заданной массы m идеального газа определяется значениями трёх параметров: давления P, объёма V, и температуры Т. Соотношение, устанавливающее связь между этими параметрами, имеет вид:
уравнение состояния идеального газа
(уравнение Менделеева-Клапейрона)
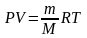 -
-
где
М
- масса 1 моля газа, R
= 8,31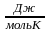 - универсальная газовая постоянная.
- универсальная газовая постоянная.
Для одного моля газа уравнение состояния идеального газа примет вид:
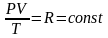 -
уравнение
Клапейрона.
-
уравнение
Клапейрона.
Рассмотрим теперь изопроцессы для идеального газа:

T = const – изотермический процесс.
PV = const – закон Бойля-Мариотта.
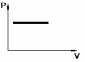
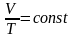 -
закон
Гей-Люссака.
-
закон
Гей-Люссака.
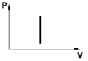
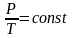 -
закон
Шарля.
-
закон
Шарля.
Запишем уравнение состояния идеального газа в другой форме.
Введем новую постоянную величину:
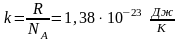 -
постоянная
Больцмана
-
постоянная
Больцмана
и перепишем уравнение Менделеева-Клапейрона в виде:
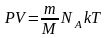 .
.
Учитывая,
что
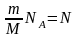 - число молекул в газе массы m,
получим
- число молекул в газе массы m,
получим
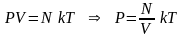 .
.
Т
другая форма записи уравнения
состояния идеального газа.
ак как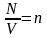 - число молекул в единице объема или
концентрация
молекул, то
- число молекул в единице объема или
концентрация
молекул, то
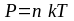 -
-
62. Дайте определение полной, молярной и удельной тсплоемкостей газа.
Молярная
теплоёмкость газа
– это количество теплоты, сообщённой
1 молю газа, для увеличения его температуры
на
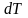 .
.
Тогда формула для подсчёта теплоты будет иметь вид
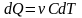 -
теплота,
сообщённая газу для
-
теплота,
сообщённая газу для
увеличения его температуры на dT.
