
- •Часть 1
- •Тема 1. Основные и технологические понятия и определения.
- •§ 1. Классификация моделей хтс.
- •1) Функциональная (принципиальная)
- •1) Основные операторы:
- •Вспомогательные операторы:
- •§ 2. Типы технологических связей хтп.
- •1) Последовательная; 2) Параллельная; 3) Обводная (байпас); 4) Рециркуляционная;
- •§ 3 Классификация химических реакций применяемых в промышленности.
- •1) Гомо и гетерофазные процессы.
- •2) Гомо и гетерогенные процессы.
- •3) Простые и сложные реакции.
- •4) Элементарные и неэлементарные реакции.
- •§ 4 Безразмерные характеристики материального баланса.
- •§ 5 Материальный баланс и его характеристики (простые реакции).
- •§ 6 Тепловой баланс и хтп и его характеристика.
- •Тема 2. Прикладная термодинамика химических процессов.
- •§ 1. Расчет тепловых эффектов химических реакций.
- •§ 2. Термодинамическая вероятность протекания химических реакций.
- •§ 3. Расчет равновесия обратимых химических реакций.
- •Закон действующих масс.
- •§ 4. Экспериментальное определение равновесного состава реакционной массы и константы равновесия.
- •§ 6. Законы смешения равновесия.
- •I) Давление.
- •II) Концентрация веществ.
- •III) Температура.
- •Тема 3: Кинетика гомогенных химических процессов.
- •§ 1 Скорость химических процессов.
- •Зависимость скорости химической реакции от концентрации исходных веществ. Основной закон кинетики.
- •1) Метод.
- •2) Метод
- •Зависимость скорости химической реакции от температуры. Общее кинетическое уравнение.
- •§2 Исследование кинетики гомогенных химических реакций.
- •Исследование гомогенных химических реакций в реакторах периодического действия емкостного типа.
- •Интегральный метод анализа кинетической зависимости.
- •Тема 4: Особенности кинетики гетерогенных каталитических процессов (гкп).
- •§1 Основные стадии гкп. Общее уравнение кинетики.
- •1) Внешнедиффузионная.
- •2) Внутренняя диффузия.
- •4) Химическое превращение.
- •§2 Внешнедиффузионная и внутредиффузионная области, лимитирующие в гетерогенном каталитическом процессе.
- •§3 Адсорбция на поверхности катализатора.
- •Основные положения теории:
- •§5. Кинетика реакции на поверхности катализаторов (кинетическая область, как лимитирующая гкп).
- •§6 Исследование кинетики гкп.
- •§7 Определение лимитирующей стадии гкп.
- •Часть 2 Основы расчета химических реакторов. Классификация химических реакторов.
- •Тема 1. Расчет изотермических реакторов для проведения гомогенных реакций..
- •§ 1. Реактор рис-п.
- •§ 2. Реактор идеального смешения рис-н.
- •§ 3. Реактор идеального вытеснения рис-в.
§7 Определение лимитирующей стадии гкп.
Обычно интерпретация кинетических
данных значительно затрудняется, если
скорость процесса одновременно зависит
от массы передачи и скорости химической
реакции. Чтобы избежать этого, необходимо
при помощи предварительных опытов
определить границы кинетической области,
а влияние процессов массы передачи
изучить отдельно, для этого используют
следующие основные приемы: 1)
Температурный коэффициент. Принято
считать, что каталитические реакции
протекают в области химической кинетики,
если с изменением температуры на 100
С суммарная скорость изменяется в
2-а или более раз. Кинетическая область:
![]() .
Если суммарная ск5оросчть изменяется
меньше чем в 2-а раза. Лимитирующая стадия
– диффузионная область (массобмен):
.
Если суммарная ск5оросчть изменяется
меньше чем в 2-а раза. Лимитирующая стадия
– диффузионная область (массобмен):
![]() .
2) Энергия активации (Е акт). а) Реакциям
протекающим в кинетической области
обычно соответствует энергии активации
равной 20-30 ккал/моль. Кинетическая
область:
.
2) Энергия активации (Е акт). а) Реакциям
протекающим в кинетической области
обычно соответствует энергии активации
равной 20-30 ккал/моль. Кинетическая
область:
![]() .
б) Реакция протекающая в диффузионной
области соответственно Еакт < 7 ккал/моль
(массобмен). в) В интервале от 10 до 20
ккал/моль.
.
б) Реакция протекающая в диффузионной
области соответственно Еакт < 7 ккал/моль
(массобмен). в) В интервале от 10 до 20
ккал/моль.
![]() диффузионно-кинетическая область. 3)
Влияние диффузии. Для определения
влияния условий массобмена на суммарную
скорость процесса используют следующие
приемы: а) Влияние внешней диффузии. Для
этого проводят несколько опытов при
различных массовых скоростях подачи
реагентов Yм и различных
массах слоях катализатора Мк , то
отношение Yм/ Мк
постоянно. В каждом опыте на выходе из
реактора измеряют концентрацию i-ого
реагента Ci и рассчитывают
степень превращения xi
при одинаковом составе реагентов на
входе в реактор. Ci,0
= const. Экспериментальные
данные оформляются в виде графика
xi=f(Yм).
диффузионно-кинетическая область. 3)
Влияние диффузии. Для определения
влияния условий массобмена на суммарную
скорость процесса используют следующие
приемы: а) Влияние внешней диффузии. Для
этого проводят несколько опытов при
различных массовых скоростях подачи
реагентов Yм и различных
массах слоях катализатора Мк , то
отношение Yм/ Мк
постоянно. В каждом опыте на выходе из
реактора измеряют концентрацию i-ого
реагента Ci и рассчитывают
степень превращения xi
при одинаковом составе реагентов на
входе в реактор. Ci,0
= const. Экспериментальные
данные оформляются в виде графика
xi=f(Yм).

В первой области, влияние внешней диффузии существенно, так как степень превращения xi зависит от скорости подачи реагентов Yм. Во второй области влияние внешней диффузии не существенно, так как степень превращения xi остается постоянным. Б) Влияние внутренней диффузии. Для изучения влияния внутренней диффузии перенос веществ в порах катализатора исследуется на зернах различной крупности.
 На основе проведенных экспериментов
определяем текущую концентрацию реагента
на выходе из реактора и рассчитывают
достигнутую степень превращения.
Экспериментальные данные оформляются
в виде графика. xi = 1/R.
R – радиус катализатора.
На основе проведенных экспериментов
определяем текущую концентрацию реагента
на выходе из реактора и рассчитывают
достигнутую степень превращения.
Экспериментальные данные оформляются
в виде графика. xi = 1/R.
R – радиус катализатора.
 Если сопротивление диффузии в порах
катализатора ничтожно, то степень
превращения должна быть одинакова для
опытов с частицами катализатора различных
размеров (область 2). Если сопротивление
внутри диффузии велики, то скорость
процесса на зернах катализатора различных
размеров не постоянна, а степень
превращения зависит от размеров зерна
катализатора.
Если сопротивление диффузии в порах
катализатора ничтожно, то степень
превращения должна быть одинакова для
опытов с частицами катализатора различных
размеров (область 2). Если сопротивление
внутри диффузии велики, то скорость
процесса на зернах катализатора различных
размеров не постоянна, а степень
превращения зависит от размеров зерна
катализатора.
Часть 2 Основы расчета химических реакторов. Классификация химических реакторов.
Тема 1. Расчет изотермических реакторов для проведения гомогенных реакций..
§ 1. Реактор рис-п.
Реакторы идеального смешения периодического действия (РИС-П) представляет собой снабженный мешалкой и рубашкой при помощи теплообмена через рубашку поддерживается требуемая температура реакционной массы. Загрузка реагентов и выгрузка продуктов осуществляется периодически.
 В РИС-П входе химической реакции при
постоянной температуре параметры
процесса концентрация и степень
превращения изменяются только во
времени.
В РИС-П входе химической реакции при
постоянной температуре параметры
процесса концентрация и степень
превращения изменяются только во
времени.
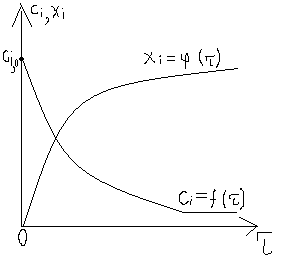
В реакторе концентрации:

Однако, во всем объеме реактора в любой момент времени, эти параметры, за счет интенсивного перемешивания остаются одинаковыми и они тем ниже, чем больше времени пребывания реагентов в реакторе. Периодические химические процессы по своей природе всегда являются нестационарными, так как входе химических реакций изменяются концентрации реагента и его степень превращения, то есть происходит накопление продуктов. Поэтому основой для получения проектного уравнения РИС-П является уравнение материального баланса в дифференциальной форме.
![]()
Ci – концентрация i-ого реагента в реакционной массе. x, y, z – пространственные координаты; Ux, Uy, Uz – составляющие скорости потока. Д – коэфициент молекулярной конвективной диффузии. υr – скорость химической реакции.
Это уравнение может быть преобразовано исходя из того, что в РИС-П в следствии интенсивного перемешивания все параметры технологического режима (Ci, xi) одинаковы во всем объеме реактора в любой момент времени, в этом случае производные любого порядка от концентрации по осям x, y, z будут равны нулю.

Тогда уравнение материального баланса
для РИС-П будет выглядеть:
![]() ,
Если принять, что в уравнении (5),
,
Если принять, что в уравнении (5),
 ,то
,то
![]() .
.
С учетом того, что
![]() ,
получим
,
получим
![]() .
.
После разделения переменных получим:
 -
проектное уравнение реактора РИС-П. Это
уравнение дает возможность определить
время реакции, необходимое для достижения
заданной степени превращения xi
в изотермических процессах и поэтому
является основным для расчета РИС-П.
Отметим, что объем реакционной массы V
в уравнении (9) входит под знак интеграла,
так как в общем случае объем реакционной
массы может быть переменным. Для некоторых
случаев уравнение (9) принимает вид:
-
проектное уравнение реактора РИС-П. Это
уравнение дает возможность определить
время реакции, необходимое для достижения
заданной степени превращения xi
в изотермических процессах и поэтому
является основным для расчета РИС-П.
Отметим, что объем реакционной массы V
в уравнении (9) входит под знак интеграла,
так как в общем случае объем реакционной
массы может быть переменным. Для некоторых
случаев уравнение (9) принимает вид:
Если V постоянно, то
 ,
в случае, когда реакции при которых
объем реакционной массы меняется,
уравнение (9) принимает вид:
,
в случае, когда реакции при которых
объем реакционной массы меняется,
уравнение (9) принимает вид:
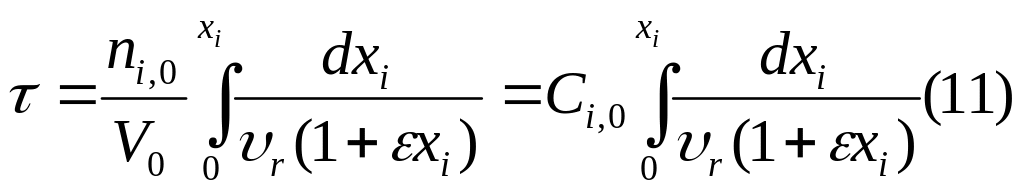
В тех случаях, когда в реакторе идеального смешения периодического действия проводится реакция, порядок которой отличается от 0 и 1, интегрирование уравнения (11) связано с определенными трудностями, поэтому расчет рабочего времени химической реакции τ производят методом графического интегрирования.
 Время
химической реакции τ = ni,0S,
в это же время реакционный объем:
Время
химической реакции τ = ni,0S,
в это же время реакционный объем:
 .
.
Реакторы РИС-П просты по конструкции, требуют небольшого вспомогательного оборудования, они удобны для проведения медленно протекающих реакций. Замечание: В периодически работающем реакторе, продолжит реакции можно измерить непосредственно по часам, так как Ci и степень превращения xi меняются во времени.
Для непрерывных реакторов используют
среднее время пребывания.

