
- •Особенности термодинамики как науки.
- •Основные определения термодинамики.
- •Координаты и потенциалы.
- •Пример 3. Химические реакции и фазовые превращения.
- •Правило знаков для потенциалов:
- •Теплота и работа. Внутренняя энергия.
- •Работа на деформацию (деформационная работа).
- •Взаимодействия равновесное и неравновесное. Процессы статические и нестатические.
- •Уравнения состояния системы.
- •Уравнения состояния реальных газов.
- •Работа и теплота. Свойства работы и теплоты.
- •Характеристические функции.
- •Дифференциальные соотношения термодинамики.
- •Отличительные особенности типов дифференциальных соотношений.
- •2. Теория теплоёмкости разнородных систем.
- •2.1. Виды теплоемкостей.
- •2.2. Общая формула для теплоемкостей однородных систем.
- •2.3. Теплоёмкость идеального газа.
- •2.4. Зависимость теплоёмкости от давления, объёма и температуры.
- •2.5.Исследование теплоемкостей идеального газа.
- •2.6.Исследование зависимости изохорной и изобарной теплоёмкостей идеального газа от величины температуры.
- •2.7.Зависимость теплоёмкости от температуры. Истинная и средняя теплоёмкости.
- •3.Вычисление энтропии.
- •3.1.Энтопия. Общие формулы для энтропии идеального а реального газов.
- •3.2.Уравнение адиабаты реального газа в общем виде.
- •4.Исследование термодинамических процессов.
- •4.1.Политропный (политропический) процесс.
- •4.2.Метод определения показателя политропы по двум точкам.
- •4.3.Теплоемкость в политропном проессе.
- •4.4.Работа, теплота и внутренняя энергия в политропном процессе.
- •Исследование изопроцессов. Работа, теплота и внутренняя энергия в изопроцессах.
- •Второй закон термодинамики.
4.2.Метод определения показателя политропы по двум точкам.
Е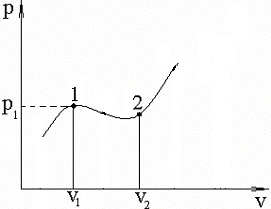 сли
для процесса известны значения
термодинамических параметров только
в двух точках, то можно приближенно
найти показатель политропы по следующему
методу:
сли
для процесса известны значения
термодинамических параметров только
в двух точках, то можно приближенно
найти показатель политропы по следующему
методу:
Известно,
P1,v1,P2,v2
из уравнения политропы ![]() для этих двух точек можно записать
равенство:
для этих двух точек можно записать
равенство:
p1v1n = p2v2n, прологарифмируем последнее выражение:
ln p1 + n ln v1 = ln p2 + n ln v2
приведем подобные и выразим n:
n (ln v2 - ln v1)= ln p2 - ln p1
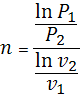
Примечание: Для определения показателя политропы могут использоваться не только индикаторные Pv-диаграммы, но и Tv и TP – диаграммы.
Поскольку политропный процесс это приближенное описание реального процесса, то и газ в политропном процессе для простоты считается идеальным:
=>
![]() ;
;
=>![]() ;
;
=>![]() .
.
(121)
(121)- уравнение политропы
4.3.Теплоемкость в политропном проессе.
Из общей формулы теплоёмкости однородных систем имеем:
![]() (62)
(62)
Была поучена:
![]() (64)
(64)
Здесь
Cn- массовая теплоемкость в политропном
процессе ![]() .
.
Так как газ в политропном процессе полагается идеальным, то
![]()
![]()
![]()
![]()
Подставим в уравнение (64)
![]() подставим
в уравнение
подставим
в уравнение
![]()
Здесь
по уравнению Майера R=Cp-Cv
, ![]()
![]() (122)
(122)
(122)- массовая теплоемкость в политропном процессе.
Так как k>1, то при 1<n<k – имеем cn<0. С точки зрения физики это трудно объяснимо, поэтому продолжим процесс вычисления с этим значением:
В силу универсальности уравнения можно формально рассмотреть изопроцессы как частные случаи политропного процесса:
При n=0 →p=const, np = 0
При n=0 → pv=const (T=const), nT = 1
При n=k →S=const(pvk=const), nA = k
При n=
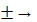 (v=const),
nv
= .
(v=const),
nv
= .
Изобразим процессы на pv-диаграмме, для кривых возьмём общую точку:
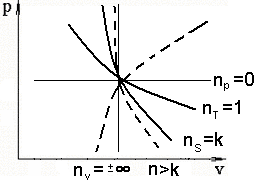
пунктирной линией изображены процессы не относящиеся к простейшим.
4.4.Работа, теплота и внутренняя энергия в политропном процессе.
Абсолютная работа термодеформационной системы определяется:
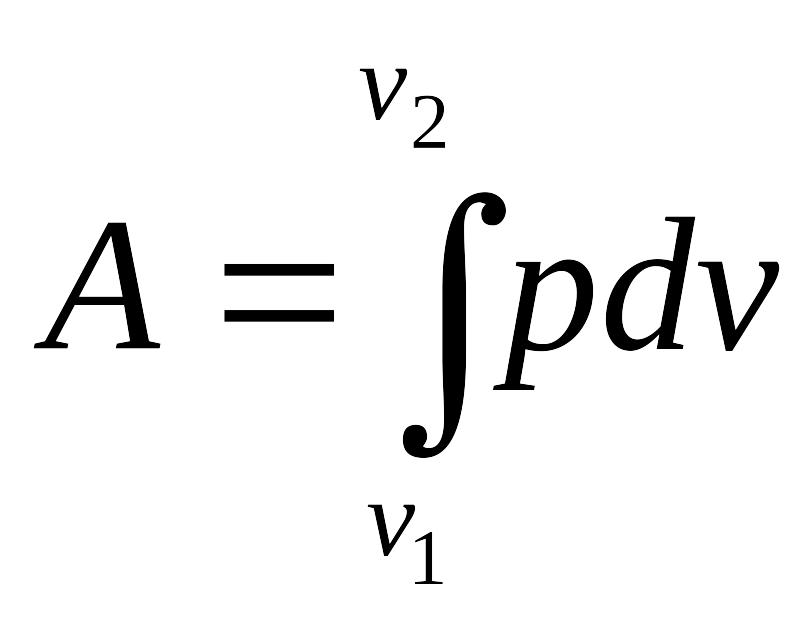
Для того чтобы взять интеграл надо знать связь между P и v. Найдем связь из уравнения политропы:
pvn=const,
![]()
![]()
![]()
![]() (123)
(123)
Получим ещё несколько формул для вычисления работы. Преобразуем формулу (123):
![]()
Окончательно:
![]() (124)
(124)
Выразим
отношение ![]() из уравнения политропы
из уравнения политропы
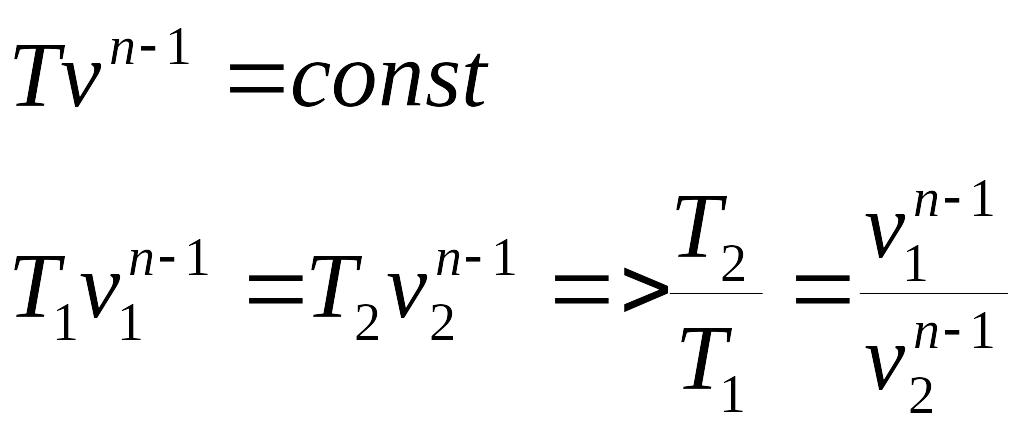
![]()
Выразим отношение температур из уравнения:
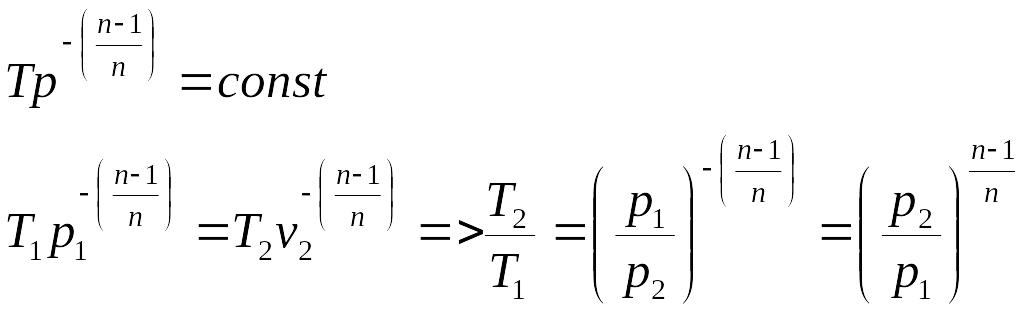

(125)
Или
![]() (126) (125), (126) широко используются
в теории газовых турбин, теории
компрессоров, газовой динамике
(126) (125), (126) широко используются
в теории газовых турбин, теории
компрессоров, газовой динамике
В
политропном процессе газ считается
идеальным, а для идеального газа ![]() ,
и
,
и ![]() для любого процесса, в том числе и для
политропного.
для любого процесса, в том числе и для
политропного.
Теплота в политропном процессе определяется:
![]()
После подстановки
dQ = T dS
dQ = c dT
c
dT
= T
dS
=> dS
=
![]() => dSn
= cn
=> dSn
= cn
![]() =
=
![]() ,
проинтегрировав, получим
,
проинтегрировав, получим
![]() .
.
Если за начало отсчета S взять нормальные физические условия, то можно получить формулу для энтропии:
![]() .
.
Получим ещё несколько формул:
![]() =>
=>
![]() =>
=>
![]()
![]()
![]() ,
при нормальных физических условиях
получим
,
при нормальных физических условиях
получим
![]() .
.
