
- •Особенности термодинамики как науки.
- •Основные определения термодинамики.
- •Координаты и потенциалы.
- •Пример 3. Химические реакции и фазовые превращения.
- •Правило знаков для потенциалов:
- •Теплота и работа. Внутренняя энергия.
- •Работа на деформацию (деформационная работа).
- •Взаимодействия равновесное и неравновесное. Процессы статические и нестатические.
- •Уравнения состояния системы.
- •Уравнения состояния реальных газов.
- •Работа и теплота. Свойства работы и теплоты.
- •Характеристические функции.
- •Дифференциальные соотношения термодинамики.
- •Отличительные особенности типов дифференциальных соотношений.
- •2. Теория теплоёмкости разнородных систем.
- •2.1. Виды теплоемкостей.
- •2.2. Общая формула для теплоемкостей однородных систем.
- •2.3. Теплоёмкость идеального газа.
- •2.4. Зависимость теплоёмкости от давления, объёма и температуры.
- •2.5.Исследование теплоемкостей идеального газа.
- •2.6.Исследование зависимости изохорной и изобарной теплоёмкостей идеального газа от величины температуры.
- •2.7.Зависимость теплоёмкости от температуры. Истинная и средняя теплоёмкости.
- •3.Вычисление энтропии.
- •3.1.Энтопия. Общие формулы для энтропии идеального а реального газов.
- •3.2.Уравнение адиабаты реального газа в общем виде.
- •4.Исследование термодинамических процессов.
- •4.1.Политропный (политропический) процесс.
- •4.2.Метод определения показателя политропы по двум точкам.
- •4.3.Теплоемкость в политропном проессе.
- •4.4.Работа, теплота и внутренняя энергия в политропном процессе.
- •Исследование изопроцессов. Работа, теплота и внутренняя энергия в изопроцессах.
- •Второй закон термодинамики.
3.2.Уравнение адиабаты реального газа в общем виде.
Из уравнения (110) при S=const (dS=0) получим
![]() .
.
Преобразуем уравнение к виду:
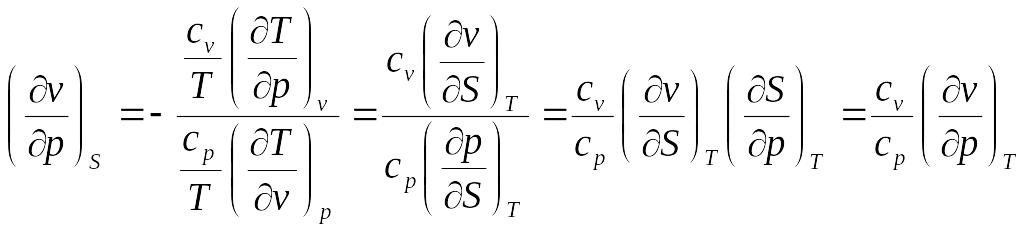
![]() (120)
(120)
Уравнение (120)-уравнение адиабаты в общем виде.
Из полученного уравнения можно сделать следующий вывод:
т.к.
![]() ,
где k>1,
то адиабатная сжимаемость
,
где k>1,
то адиабатная сжимаемость
![]() в k
раз больше изотермической сжимаемости
.
в k
раз больше изотермической сжимаемости
.
Это объясняется тем, что при адиабатном сжатии температура газа повышается, что в соответствии с уравнением состояния приводит к повышению давления, т.е. к увеличению сопротивления системы к её сжатию.
4.Исследование термодинамических процессов.
4.1.Политропный (политропический) процесс.
В целом ряде случаев реальные процессы не соответствуют ни одному из изопроцессов.
Пример:
В
таких случаях при выполнении тепло
технических расчётов, пусть даже в ущерб
точности, реальный процесс заменяется
гипотетическим, имеющим удобную форму
уравнения. Из математики известно, что
уравнение вида
![]() удобно в различного вида преобразованиях.
Т.к. это уравнение должно описывать всё
многообразие реальных процессов, то в
этом уравнении должен присутствовать
коэффициент согласования (идентификации).
Этим коэффициентом в вышеприведённом
уравнении является показатель степени
n,
называемый показателем
политропы.
Т.к. n
коэффициент согласования, то, в отличие
от уравнения адиабаты идеального газа
,
k>1,
показатель политропы принимает любые
значения в интервале (,+).
Конкретные значения n
для данного процесса определяются в
результате обработки опытных данных
(пример приведённой выше pv-диаграммы).
удобно в различного вида преобразованиях.
Т.к. это уравнение должно описывать всё
многообразие реальных процессов, то в
этом уравнении должен присутствовать
коэффициент согласования (идентификации).
Этим коэффициентом в вышеприведённом
уравнении является показатель степени
n,
называемый показателем
политропы.
Т.к. n
коэффициент согласования, то, в отличие
от уравнения адиабаты идеального газа
,
k>1,
показатель политропы принимает любые
значения в интервале (,+).
Конкретные значения n
для данного процесса определяются в
результате обработки опытных данных
(пример приведённой выше pv-диаграммы).
Алгоритм определения показателя политропы n.
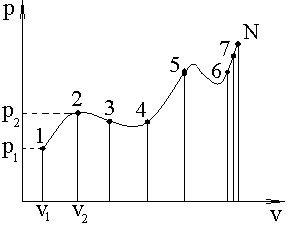
Разбиваем pv-диаграмму реального процесса на N точек (чем больше точек, тем точнее).
Снимаем с pv-диаграммы рельного процесса значение давления удельного объёма в каждой точке и заносим в таблицу.
Для каждой точки находим lnp и lnv.
Перестраиваем pv-диаграмму в логарифмических координатах: lnp – Oy; lnv – Ox.
Используем метод наименьших квадратов. Аппроксимируем точки на графике в логарифмических координатах к одной прямой, если это удаётся без значительных погрешностей, то тангенс угла наклона к прямой Ox(lnv) является показателем политропы в уравнении , используемом в описании данного процесса. Если не удаётся, то используем метод линейно-кусочной аппроксимации.
№ ячейки |
p, Па |
v,
|
lnp |
lnv |
1 |
p1 |
v1 |
lnp1 |
lnv1 |
2 |
p2 |
v2 |
lnp2 |
lnv2 |
… |
… |
… |
… |
… |
N |
pN |
vN |
lnpN |
lnvN |
Аппроксимация всех точек одной прямой:
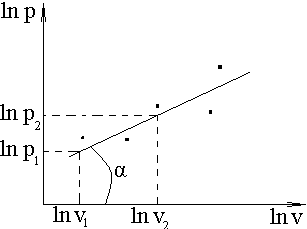
tg α – показатель политропы.
Линейно-кусочная аппроксимация:
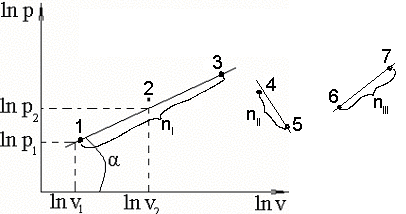
В последнем случае реальный процесс рассчитывается по уравнению pvn = const, n последовательно принимает значения nI, nII, nIII и т.д.
Результаты вычисления A,Q,U,S на различных участках затем суммируется, так как они являются аддитивными величинами.
